 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| ��ҵ2����ҵ����ͼ�� | |
|---|---|
| �����������⣺49 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||||||||||||
���� |
2022�����߿� | |||||||||||||
| ��� | ij�������û����(��Ҫ�ɷ�ΪBi2S3������FeS2��SiO2����)�����̿�(��Ҫ�ɷ�ΪMnO2)���ϱ��շ��Ƹ�BiOCl��MnSO4�������������£�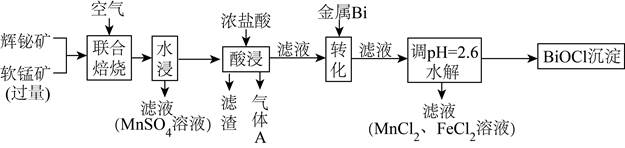 ��֪���ٱ���ʱ������MnO2�ֽ�ΪMn2O3��FeS2ת��ΪFe2O3�� �ڽ�����ԣ�Fe��(H)��Bi��Cu�� ����ؽ��������γ����������pH��Χ���£�
��1��Ϊ��߱���Ч�ʣ��ɲ�ȡ�Ĵ�ʩΪ_______�� a.��һ�������ʯ�������� b.�����ʵ������Ŀ����������� c.���ͱ����¶� ��2��Bi2S3�ڿ����е�����������Bi2O3����Ӧ�Ļ�ѧ����ʽΪ_______�� ��3����������й���Ũ���������Ϊ���ٳ�ֽ���Bi3+��Mn2+����_______�� ��4����������Ҫ�ɷ�Ϊ_______(�ѧʽ)�� ��5����������A�����ӷ���ʽΪ_______�� ��6���������Bi��Ŀ����_______�� ��7����100kg�����������ϱ��գ�ת��ʱ����1.1kg����Bi���������������ʧ���ƣ���������BiOCl��Ʒ����Ϊ32kg���ζ���ò�Ʒ��Bi����������Ϊ78.5%���������BiԪ�ص���������Ϊ_______�� |
|||||||||||||
�� |
��1��ab��������2��2Bi2S3+9O2 2Bi2O3+6SO2 2Bi2O3+6SO2��3�����ƽ�������ˮ�⡡���� ��4��SiO2��������5��Mn2O3+6H++2Cl����2Mn2++Cl2��+3H2O ��6����Fe3+ת��ΪFe2+������ ��7��24.02% |
|||||||||||||
| ��� | 2 |
|
||
���� |
2022�ӱ��߿� | |||
| ��� | LiBr��Һ����Ϊ�������������ɫ��������ϳ�LiBr�����������£� ����˵��������� A����ԭ�����ݳ���Br2��NaOH��Һ���գ�����Һֱ�ӷ��ػ�ԭ���� B�����ӹ����в�������������ú�ͽ�����ַ��� C���к����еĻ�ѧ��ӦΪLi2CO3+2HBr��CO2����2LiBr+H2O D�����뷴Ӧ��n(Br2):n(BaS):n(H2SO4)Ϊ1��1��1 |
|||
�� |
A |
|||
| ��� | 3 |
|
||
���� |
2023�ӱ��߿� | |||
| ��� | �ջ�ѭ�������������Դ�����ʺ�ʵ����ɫ��ѧ��Ŀ�ꡣ���ð�����ȡ��ʵ�ַ�����ͭ���ֵ���Ч���룬ͬʱ�õ���CuCl�����ڴ���ҽҩ��ұ�����Ҫ�������������£� ��֪�������µ�Ksp(CuCl)��10��6.8�� �ش��������⣺ ��1���״ν�ȡ��������ɫ��Һ����ͭë˿������Һ�������������ᷴӦ�õ�������Ҫ�ɷ�Ϊ_______(�ѧʽ)�� ��2����������Ҫ�ɷ�Ϊ_______(�ѧʽ)�� ��3����ȡ����IJ���Ϊ[Cu(NH3)2]Cl���ù�������Ӧ�Ļ�ѧ����ʽΪ_______����ȡ����Һ��һ�뾭��������ɵ�����ɫ��Һ�٣�������������Ӧ�����ӷ���ʽΪ_______�� ��4����ȡ��������30��40��֮����У��������¶Ƚϵ�ʱ����ȡҺ�������������ȼ��ɽ��н�ȡ��ԭ����_______�� ��5����ȫ�к���������Ӧ�����ӷ���ʽ[Cu(NH3)2]++2H++Cl��=H _______+_______�� ��6����ո����Ŀ��Ϊ_______�� |
|||
�� |
��1��[Cu(NH3)4]Cl2���� �� ��2��Fe������ ��3����[Cu(NH3)4]Cl2+Cu��2[Cu(NH3)2]Cl ��8NH3+4[Cu(NH3)2]����O2+4H+��4[Cu(NH3)4]2��+H2O ��4�������Һ����Ӧ���ȡ����� ��5����CuCl����������2NH4+������ ��6����ֹ���������CuCl�������е�O2���� |
|||
| ��� | 4 |
|
||||||||||
���� |
2023���� | |||||||||||
| ��� | ij�����������¹��մ������ܿ������ȡҺ����Ni2+��Co2+��Fe2+��Fe3+��Mg2+����Mg2+��)��ʵ�������ܡ�þԪ�صĻ��ա�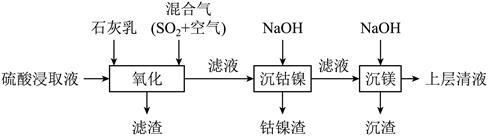 �� �� ��֪��
��1���������ȡ���ܿ�ʱ����߽�ȡ���ʵķ���Ϊ_______(���һ������)�� ��2�����������У�������ڽ������ӵĴ������²�������ǿ�����ԵĹ�һ����(H2SO5)��1mol H2SO5�й���������ĿΪ_______�� ��3�����������У���ʯ�������pH��4��Mn2+��H2SO5����ΪMnO2���÷�Ӧ�����ӷ���ʽΪ_______( H2SO5�ĵ����һ����ȫ���ڶ�����)�������ijɷ�ΪMnO2��_______(�ѧʽ)�� ��4�����������б��ֿ���ͨ�����ʲ��䣬Mn (��)��������ʱ��Ĺ�ϵ���¡�SO2�������Ϊ_______ʱ��Mn (��)�����������������SO2�������ʱ��Mn(��)�������ʼ�С��ԭ����_______�� 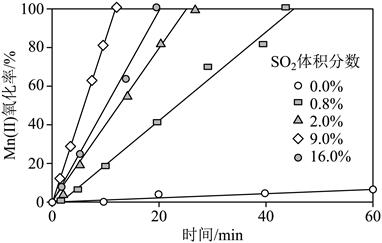 �� �� ��5�������������еõ���Co (��)�ڿ����пɱ�������CoO(OH)���÷�Ӧ�Ļ�ѧ����ʽΪ_______�� ��6������þ����ΪʹMg2+������ȫ��25�棩�������pH������_______(��ȷ��0.1)�� |
|||||||||||
�� |
��1���ʵ���������Ũ�Ȼ��ʵ������¶Ȼ����ܿ��������Ӵ���� ��2��NA ��3����H2O+Mn2++HSO5-=MnO2+SO42-+3H+������ ��CaSO4��Fe(OH)3������ ��4����9.0% ��SO2�л�ԭ�ԣ����ཫ�ή��H2SO5��Ũ�ȣ�����Mn(��)�������ʡ����� ��5��4Co(OH)2+O2=4CoO(OH)+2H2O������ ��6��11.1 |
|||||||||||
| ��� | 5 |
|
||
���� |
2023���� | |||
| ��� | ��ҵ�Ʊ��ߴ������Ҫ�������£� ʯӢɰ  �ֹ� �ֹ�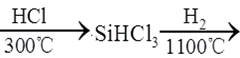 �ߴ��� �ߴ�������˵��������� A.�Ʊ��ֹ�ķ�Ӧ����ʽΪSiO2+2C  Si+2CO�� Si+2CO��B. 1molSi��Si��Si������ĿԼΪ4��6.02��1023 C.ԭ����HCl��H2Ӧ���ȥ��ˮ������ D.����SiHCl3�ķ�ӦΪ�ؼ����� |
|||
�� |
B |
|||
| ��� | 6 |
|
||
���� |
2023�걱�� | |||
| ��� | �����̾���(��Ҫ��Ag2S��MnS��FeS2)�������̿�(��Ҫ��MnO2)Ϊԭ��������ȡ�����̵�һ������ʾ��ͼ���¡�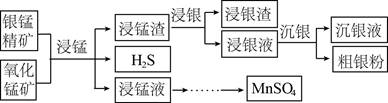 �� �� ��֪�����������£�MnO2��������ǿ��Fe3���� ��1�������̡���������H2SO4��Һ��ʹ��ʯ�е���Ԫ�ؽ�����ͬʱȥ��FeS2�������ں������Ľ�������ʯ�е�����Ag2S����ʽ�����ڽ������С� �١����̡������У�������ӦMnS��2H����Mn2����H2S��������ƶϣ�Ksp(MnS) __________(�>����<��)Ksp(Ag2S)�� ����H2SO4��Һ�У����̾����е�FeS2�������̿��е�MnO2������Ӧ�������Һ����Ҫ�Ľ�����������__________�� ��2����������ʱ��ʹ�ù���FeCl3��HCl��CaCl2�Ļ��Һ��Ϊ����������Ag2S�е�����[AgCl2]����ʽ������ �ٽ�����������Ӧ�����ӷ���ʽ����������__________�� Fe3����Ag2S����������������  ������������2[AgCl2]����S ������������2[AgCl2]����S�ڽ��ƽ���ƶ�ԭ�������ͽ�������Cl����H�������ã�____________________�� ��3������������������Ҫ������������Ϊ��ԭ���� �ٸò���Ӧ�����ӷ���ʽ��______________________________�� ��һ���¶��£�Ag�ij������淴Ӧʱ��ı仯��ͼ��ʾ������t���Ӻ�Ag�ij�������С��ԭ��______________�� �� 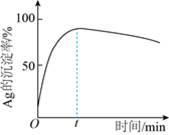 ��4����ϡ����̡����̣������ֿ�ʯ�и��������õĽǶȣ�����������ȡ�����̵����ƣ�________�� |
|||
�� |
��1����>��������Fe3����Mn2�������� ��2����2Fe3����Ag2S��4Cl��  2Fe2����2[AgCl2]����S 2Fe2����2[AgCl2]����S��������Cl����Ϊ����Ag2S�������Ag���������[AgCl2]����ʹƽ�������ƶ������Ag2S�Ľ����ʣ�H����Ϊ������Fe3��ˮ�⣬��ֹ����Fe(OH)3���������� ��3����2[AgCl2]����Fe��Fe2����2Ag��4Cl����2Fe3����Fe��3Fe2�� ��������Fe2������������ΪFe3����Fe3����Ag����ΪAg�������� ��4���ɽ����ֿ�ʯ�е���Ԫ��ͬʱ��ȡ������Һ�У��õ�MnSO4��ͬʱ����Ԫ�غ���Ԫ�ط��뿪�����ɵ�Fe3�����������ڽ�������Լ������ |
|||
| ��� | 7 |
|
||||||||||
���� |
2023���� | |||||||||||
| ��� | �Ͻ���ͭ�ܿ�ұ�����̵��м���һ�ִӰϽ���Ҫ��Fe3O4��CoO��CuS��Cu2S ������SiO2������ȡ����������������£�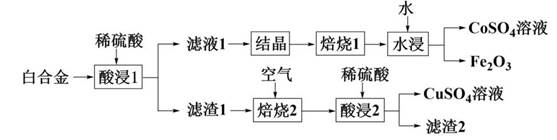 �� ����1������� 1���У����Լӿ컯ѧ��Ӧ���ʵĴ�ʩ��_________����д����һ�֣��� CoO ������Ӧ�����ӷ���ʽ_________�� ��2��������1���У�����[Fe2(SO4)3•xH2O��CoSO4•yH2O ]���������¶����ߵı仯������£�
566 ~ 600�淢���ֽ��������__________���ѧʽ���� ��Ϊ��Ч����������Ԫ�أ�������1�����¶�Ӧ����Ϊ__________�档 ��3��25��ʱ��K sp (CuS) = 6.3��10−36��H2S ��Ka1 =1.1��10−7 ��Ka2 =1.3��10��13 ��ӦCuS(s)+2H (aq+)��Cu2+(aq)+H2S(aq) ��ƽ�ⳣ��K=__________���г�����ʽ���ɣ��� ��������ж�CuS������ϡ���ᡣ ��4��ͭ������ṹ��������Ȼ��ͭ�׳�ͭ�����侧���ṹ��ͼ��  �� ���ٻ�̬Cu2+�ļ۵����Ų�ʽΪ__________�� �ھ����к���__________��S22−��N (Cu +): N (Cu2+)=__________�� �۾�����������������__________�����ţ��� a����������� b�����Ӽ������� c�����ۼ������� d�������� ��5��������2����CuS2 ������Ӧ�Ļ�ѧ����ʽΪ__________��������2����__________���ѧʽ���� |
|||||||||||
�� |
��1������Ͻ𡢽��衢�ʵ����¡��ʵ�����ϡH2SO4Ũ�ȵȺ����� ע�������������ϡH2SO4���������� ��2����ʧȥ�ᾧˮ��Fe2 (SO4)3 ע��Fe2 (SO4)3д��Fe2 (SO4)3 xH O2 �����֣�д�����Ʋ����֡� ��600��~ 630�� ע���¶����������ֵ��ֳ������д�ɺ��ֶ����֡� ��3��  ��(4.4-4.5)10֮����һ���� ��(4.4-4.5)10֮����һ������1��3d9��������2��2��2:1��4:2��2��bc ��3��CuS2+2O2  2CuO+SO2��SiO2 2CuO+SO2��SiO2 �裺Cu+Ϊx��Cu2+Ϊy ����ԭ���غ㣺x+y=6 ���ݵ���غ㣺x+2*y=8 |
|||||||||||
| ��� | 8 |
|
||
���� |
2023���� | |||
| ��� | �����ַ۳�����Ҫ��Fe2O3 ��Fe3O4��ZnO������ȡп���������£� �� �����ν�������ZnOת��Ϊ[Zn(NH3)4]2+ ����������Fe2����Fe3+ ����������˵��������ǣ��������� A�����ν�����������ҺpH�½����貹��NH3 B��������������Ҫ�ɷ�ΪFe(OH)3 C������п�����̷�����Ӧ[Zn(NH3)4]2++4H2O+S2����ZnS����4NH3•H2O D��Ӧ��������(NH4 )2 S�������Ա���Һѭ��ʹ�� |
|||
�� |
B�� | |||
| ��� | 9 |
|
||
���� |
2023ɽ�� | |||
| ��� | һ���Ʊ�Cu2O�Ĺ���·����ͼ��ʾ����Ӧ��������ҺpH��3~4֮�䣬��Ӧ���輰ʱ����NaOH�Ա��ַ�Ӧ��pH��5�����½��С������£�H2SO3�ĵ���ƽ�ⳣ��Ka1��1.3��10��2��Ka2��6.3��10��8������˵����ȷ���� A����Ӧ���Ϊ������ԭ��Ӧ B���������������ҪĿ���Ƿ�ֹNaHSO3������ C����ҺY��ѭ�����ڷ�Ӧ�����ڲ�����Ԫ��������� D����Cu2O�������䣬���뷴Ӧ���X��CuSO4���ʵ���֮��n(x):n(CuSO4)����ʱ���貹��NaOH�������� |
|||
�� |
CD | |||
| ��� | 10 |
|
||||||||
���� |
2023���� | |||||||||
| ��� | Fe3O4��һ����;�㷺�Ĵ��Բ��ϣ���FeCl2Ϊԭ���Ʊ�Fe3O4����ø�����CaCl2ˮ����Ĺ������¡� ����  �� ��25��ʱ�������ܶȻ����±���
��1��Fe3O4��FeԪ�صĻ��ϼ��ǣ�2��______�� O2���ĺ�������Ų�ʽΪ__________________�� ��2����Ӧ��1�еķ�Ӧ���ڸ������������½��У���ԭ����_______________�� ��3����Ӧ��2�У�����CaO�ͷ�ɢ����ͬʱͨ������� �ٷ�Ӧ�����ӷ���ʽΪ______________________________________�� ��Ϊ�ӿ췴Ӧ���ʣ��ɲ�ȡ�Ĵ�ʩ��__________________��д������ɣ��� ��4���ٷ�Ӧ��3�У�25��ʱ��Ca2��Ũ��Ϊ5.0 mol��L��1��������pH������______���ڳ�ȡCaCl2ˮ����1.000 g����ˮ�ܽ⣬�������Na2C2O4�������ó�������ϴ�Ӻ������ȵ�ϡ�����У���0.1000 mol��L��1KMnO4����Һ�ζ�������24.00mL���ζ��ﵽ�յ������Ϊ_________________________________���ø�������CaCl2����������Ϊ_______�� |
|||||||||
�� |
��1����+3��������1s22s22p6������ ��2����ֹ����������������������Ϊ������������ ��3����4CaO+6H2O+4Fe2++O2��4Fe(OH)3+4Ca2+���������ʵ������¶ȡ����衡���� ��4����11������������α�Һ�������Һ��Ϊ��ɫ���Ұ�����ڲ���ɫ��������66.6% |
|||||||||
| ��� | 11 |
|
||
���� |
2023���� | |||
| ��� | V2O5��WO3/TiO2�����ܴ�NH3�ѳ������е�NO����ӦΪ ��������4NH3(g)��O2(g)��4NO(g)��4N2(g)��6H2O(g)���� ��H����1632.4 kJ��mol��1 ��1���������Ʊ�����Ԥ���Ʊ���һ������WO3/TiO2��ĩ����80���ˮ�У��ڽ����¼���һ������NH4VO3��Һ�������������յȹ���õ�����״V2O5��WO3/TiO2��������ˮ��Һ��VO3��ˮ��ΪH3VO4���������ӷ���ʽΪ������������������������Ӧѡ��NH4VO3��Һ����ѡ��NaVO3��Һ��ԭ�������������������������� ��2��������Ӧ�á���һ�����ʵ���Ũ�ȵ�NO��O2��NH3(����ΪN2)��������ͨ��װ��V2O5��WO3/TiO2�����ķ�Ӧ�������NO��ת�������¶ȵı仯����14ͼ��ʾ����Ӧ�¶���320~360�淶Χ�ڣ�NOת�������¶ȱ仯�����Ե�ԭ����������������������������������������������������������������������������Ӧ�¶ȸ���380�棬NOת�����½�������Ϊ���뷴Ӧ����NO����ԭ���������⣬���������������� ���û�ѧ����ʽ��ʾ���� 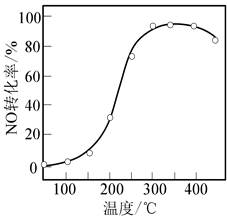 ��3���ϴ����Ļ��ա�����V2O5��WO3/TiO2�������Ʊ�NH4VO3�Ĺ��̿ɱ�ʾΪ 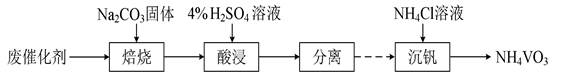 �����ʱ��������ɺ���һ�����ʽ��跴Ӧ����߷�Ԫ�ؽ����ʵķ����������������������������������������������� ��ͨ����ȡ�ɷ��뷰���٣��ڵõ��ķ����к���H4V4O12����֪H4V4O12���а�Ԫ���ṹ����ṹʽ�ɱ�ʾΪ���������������������������������������� ����pH��8��NaVO3��Һ�м��������NH4Cl��Һ������NH4VO3��������֪ Ksp(NH4VO3)��1.7��10��3���ӹ���NH4Cl��Ŀ�������������������������������������������� |
|||
�� |
��1��VO3����2H2O��H3VO4����OH�� ��VO3����NH+4��H2O��80��H3VO4����NH3�ƵõĴ����в���Na+ ��2���ڸ��¶ȷ�Χ�ڣ������Ļ��Ա仯��������NO�ķ�Ӧ����������NO�ķ�Ӧ�������¶����߶�����NOת���ʵ�Ӱ������� ���� 4NH3��5O2������380��4NO��6H2O ��3������߷�Ӧ�¶ȣ��ӳ�����ʱ�� �� 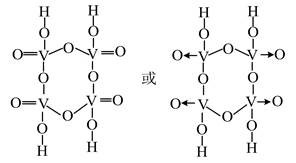 �۴ٽ�NH4VO3��ֳ��� |
|||
| ��� | 12 |
|
||
���� |
2023ȫ���¿α� | |||
| ��� | ���ͷ����й㷺��;���������и��ͷ��Եͼ�̬����������ʽ���ڣ���Ҫ����Ϊ���������衢�ȵĻ�����Ӹ������з�����ȡ���ͷ���һ����������ͼ��ʾ��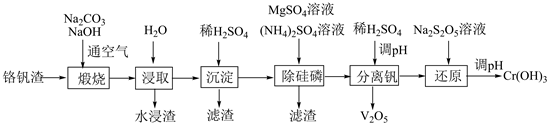 �� �� ��֪����۸���������Խ�������Cr2O72�����ڣ��ڼ��Խ�������CrO42�����ڡ� �ش��������⣺ ��1�����չ����У�����������Ϊ��Ӧ����ۺ������Σ����к�����������ҪΪ___________(�ѧʽ)�� ��2��ˮ��������Ҫ��SiO2��___________�� ��3���������������pH�������ԣ���Ҫ��ȥ��������___________�� ��4���������ס������У�ʹ�衢�ֱ���MgSiO3��MgNH4PO4����ʽ�������ò���Ҫ������Һ��pH��9�Դﵽ��õij���Ч������pH<9ʱ���ᵼ��___________��pH>9ʱ���ᵼ��___________�� ��5�������뷰�������У�����ҺpH����1.8���ҵõ�V2O5������V2O5��pH<1ʱ���ܽ�ΪVO2+��VO3+�ڼ��������£��ܽ�ΪVO3����VO43������������˵��V2O5����___________(����)�� A�����ԡ����������������� B�����ԡ��������������� C������ ��6������ԭ�������м��뽹��������(Na2S2O5)��Һ����Ӧ�����ӷ���ʽΪ___________�� |
|||
�� |
��1��Na2CrO4������ ��2��Fe2O3��������3��Al(OH)3������ ��4���٣����������H+��Ӧʹ��Ũ�Ƚ��͵���MgNH4PO4����ȫ������ͬʱ���ܲ������ὺ״�������˴����������ڣ��ᵼþ��������������þ�����������γ�MgSiO3���������²�Ʒ�л������ʣ�ͬʱ��Һ��笠�����Ũ�Ƚ��͵���MgNH4PO4����ȫ���������� ��5��C��6��2Cr2O72��+3S2O52��+10H+��4Cr3++6SO42��+5H2O |
|||
| ��� | 13 |
|
||
���� |
2024Ȫ��һ�� | |||
| ��� | NaClO2(��������)����ֽ��ҵ�г�����Ư�������ȼ��Ӵ��ױ�ը��һ���Ʊ�NaClO2��������ͼ��ʾ������˵���������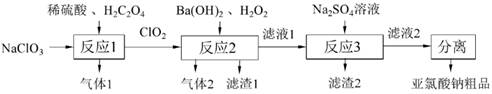 A��NaClO2��Ư��ԭ����O3 ���� B������1������2�ֱ���CO2��O2 C����Ӧ3�����ӷ���ʽ��Ba2+ + SO24����BaSO4�� D�������롱�������̰����ᾧ�����ˡ��Ҵ�ϴ�ӵ� |
|||
�� |
D | |||
| ��� | 14 |
|
||
���� |
2024Ȫ��һ�� | |||
| ��� | ��Ǹ��ܵ�ص���Ҫԭ���ϡ���ҵ����Li2CO3Ϊ�Դ�Ʊ�LiFePO4�����κ�ˮ������NaCl��LiCl��MgCl2��Na2B4O7�����ʣ�������Li2CO3�Ĺ���������ͼ��ʾ�� ����Na2CO3��ҺCa(OH)2����Na2CO3��Һ 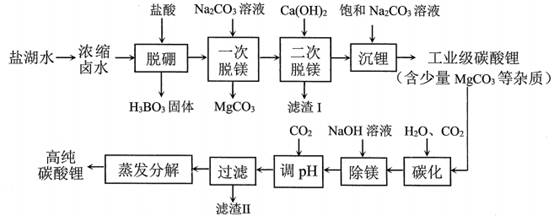 ��֪H3BO3������NaOH��Һ��Ӧ����Na[B(OH)4]����H3BO3Ϊ�������� Ԫ�ᡣ ����I�ijɷ������������������� ���ѧʽ����̼������̼���ת��Ϊ�������������������� ���ѧʽ�� ��֪�ڲ�ͬ�¶��¡������ֽ⡱��̼��﮵IJ�����̼����ܽ�ȹ�ϵ��ͼ�� 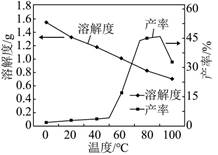 90�����£����¶����ߣ�̼��﮲������ߵ�ԭ��������������������������������������� . ��ҵ���Ըߴ�̼��ﮡ���������̿��(C)Ϊԭ�ϣ�ͨ���������յķ����Ƶ�LiFePO4��Ӧ�Ļ�ѧ����ʽΪ������������������ ���� LiFePO4������ӵ����Ҫ�������ϣ������ṹʾ��ͼ��ͼ(a)��ʾ�����Ч�Χ��Fe�ͧ��ֱ��γ���⼋������������壬����ͨ�������㡢�����γɿռ����ṹ��ÿ�������к���LiFePO4�ĵ�Ԫ������������ ���� 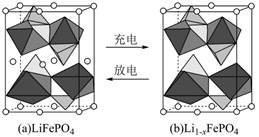 ��س��ʱ��LiFePO4�ѳ�����Li+���γ�Li1-xFePO4����ṹʾ��ͼ��ͼ(b)��ʾ����x������������������ �� |
|||
�� |
��1��B4O72- + 2H+ + 5H2O��4H3BO3�� ��2��һ Mg(OH)2��CaCO3 LiHCO3�� ̼����﮷ֽ������¶����߶����ӣ�̼��﮵��ܽ�����¶����߶����� Li2CO3 + 2FePO4 + 2C  2LiFePO4 + 3CO �� 2LiFePO4 + 3CO ����2Li2CO3 + 4FePO4 + C  ��4LiFePO4 + 3CO2�� ��4LiFePO4 + 3CO2����7��4��0.5 |
|||
| ��� | 15 |
|
||||||||||||||||||||||||
���� |
2024�人���µ��� | |||||||||||||||||||||||||
| ��� | ������أ�KClO4)��һ������ˮ�İ�ɫ��ĩ������ǿ�����ԣ��������̻����������Ʊ��Ĺ�ҵ��������ͼ��ʾ�� �ش��������⣺ ��1)����⡱�����У���������ʹ���������������������� ������������������ӽ���Ĥ��������������Ҫ���������� �� ��2)���ᾧ�������У����û����ᾧ��Ŀ������������������������������������������������������������ �� ��3)�����·ֽ⡱�Ļ�ѧ����ʽΪ�������������� �� ��4)��֪������ʵ��ܽ�����±���ʾ��
�ڡ�ת����������Ӧ�����ӷ���ʽΪ���������������� . ��5)��ĸҺ�������ʳɷ������������������� ���ѧʽ���� |
|||||||||||||||||||||||||
�� |
��1)����H2��������2)�õ���������壬���ڹ��˷��� ��3)4NaClO3  3NaClO4+NaCl 3NaClO4+NaCl��4)��0.014��0.015��2�֣���K++C1O4-=KC1O4�� ��5)NaCl��KClO4(��KC1��NaClO4���۷֣� |
|||||||||||||||||||||||||
| ��� | 16 |
|
|||||||||||||||
���� |
2023���ϸ߿� | ||||||||||||||||
| ��� | ����ijͭұ����ˮ(��Cu2+��Fe3+��Zn2����Al3+)�IJ����������£�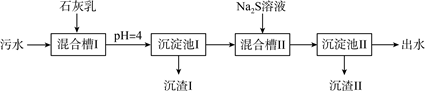 �� �� ��֪������Һ�н������ӿ�ʼ��������ȫ������pH���±���ʾ��
����˵��������� A. ���������к���Fe(OH)3��Al(OH)3 B. Na2S��Һ�ʼ��ԣ�����Ҫԭ����S2��+H2O  HS��+OH�� HS��+OH��C. �������آ��У���Cu2+��Zn2����ȫ����ʱ����Һ�� 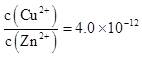 D. ����ˮ���������ӽ�����֬����������������ҵ��ȴѭ����ˮ |
||||||||||||||||
�� |
D |
||||||||||||||||
| ��� | 17 |
|
||||||||||
���� |
2023���ϸ߿� | |||||||||||
| ��� | ����Ga(CH3)3���Ʊ��������뵼���֧��Դ����֮һ�����������ҹ��Ƽ������߿����˳������������������ͳ�����װһϵ�и��¼����������Ƴ���Ga(CH3)3����ȡ���������ɹ�����ҵ���Դ���Ϊԭ�ϣ��Ʊ�����Ga(CH3)3�Ĺ����������£�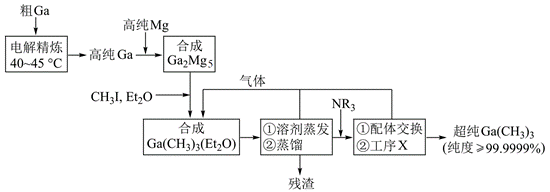 �� �� ��֪���ٽ���Ga�Ļ�ѧ���ʺ�Al���ƣ�Ga���۵�Ϊ29.8�棻 ��Et2O (����)��NR3 (��������)�����������п���Ϊ���壻 ��������ʵķе㣺
��1������Ga(CH3)3�ľ���������_______�� ��2������⾫����װ����ͼ��ʾ�������¶ȿ�����40��45���ԭ����_______�������ĵ缫��ӦʽΪ_______��  �� �� ��3�����ϳ�Ga(CH3)3(Et2O)�������еIJ��ﻹ����MgI2��CH3MgI��д���÷�Ӧ�Ļ�ѧ����ʽ��_______�� ��4��������������ˮ�������ܲ�����ȼ�����壬��������Ҫ�ɷ���_______�� ��5������˵���������_______�� A.������Et2O�õ���ѭ������ B.�����У����ϳ�Ga2Mg5����������X��������ˮ�����������½��� C. ������X���������ǽ���Ga(CH3)3(NR3)��������Ga(CH3)3 D.�ú˴Ź������ײ�������Ga(CH3)3��CH3I ��6��ֱ�ӷֽ�Ga(CH3)3(Et2O)�����Ʊ�����Ga(CH3)3���������̲��á����彻���������Ʊ�����Ga(CH3)3��������_______�� ��7���ȽϷ����е�C��Ga��C���Ǵ�С��Ga(CH3)3_______ Ga(CH3)3(Et2O) (�>����<����=��)����ԭ����_______�� |
|||||||||||
�� |
��1�����Ӿ��塡���� ��2���������ٱ�֤GaΪҺ�壬���ڴ�Ga������������GaO2��+3e��+2H2O=Ga+4OH������[Ga(OH)4]��+3e��=Ga+4OH���������� ��3��8CH3I+2Et2O+Ga2Mg5=2 Ga(CH3)3(Et2O)+3MgI2��2CH3MgI�������� ��4��CH4��������5��D������ ��6��NR3�е�ϸߣ�����Ga(CH3)3���룬Et2O�ķе����Ga(CH3)3��һ�����������Եõ�����Ga(CH3)3������ ��7����>����Ga(CH3)3��GaΪsp2�ӻ�������Ϊƽ��ṹ����Ga(CH3)3(Et2O)��GaΪsp3�ӻ�������Ϊ������ṹ���ʼнǽ�С |
|||||||||||
| ��� | 18 |
|
||||||||||||||
���� |
2023���ݲ��Զ� | |||||||||||||||
| ��� | ������(GaN)��������Ĺ�����ܡ�һ��������п����[��Ҫ��������Ga2(Fe2O4)3������пZnFe2O4��SiO2]�Ʊ�GaN�Ĺ����������£� ��֪�� ��Ga��Alͬ���壬��ѧ�������ơ� �ڳ����£�Ksp[Zn (OH)2]��10��16.6��Ksp[Ga(OH)3]��10��35.1��Ksp[Fe(OH)3]��10��38.5�� ��Ga3+��Fe3+�ڸù��������µķ���ȡ��(����ˮ���н������ӵİٷ���)������Ũ�ȵĹ�ϵ���±���
��1���������ʱGa2(Fe2O4)3������Ӧ�����ӷ���ʽΪ____�������ܡ�������������Ҫ�ɷ���________(�ѧʽ)�� ��2������������ý���Һ��Ga3+��Zn2+Ũ�ȷֱ�Ϊ0.21g��L��1��65g��L��1�������£�Ϊ�����ܶ����ȡGa3+��ȷ��������Zn(OH)2������pH��ʱ����CaO��pH��_________(�����pHʱ��Һ�������)�� ��3�����������͡�����ȡ��ʱ�����������Ũ��a��________��b��_______(ѡ���ϱ��������Ũ��)�� ��4�������ء�ʱ��������NaOH�������࣬�ᵼ��Ga3+�ij����ʽ��ͣ�ԭ����_____________(�����ӷ���ʽ��ʾ)�� ��5������CVD(��ѧ�������)���������ȷֽ�õ���Ga2O3��NH3�ڸ����·�Ӧ���Ƶ�GaN��ͬʱ������һ�ֲ���÷�Ӧ��ѧ����ʽΪ__________________�� ��6����GaN���۵�Ϊ1700�棬GaCl3���۵�Ϊ77.9�棬���ǵľ�����������Ϊ_________��_________�� ��GaN�����һ������������ͼ��ʾ���þ�������Gaԭ�Ӿ����������ȵ�Nԭ�Ӹ���Ϊ________���þ����ܶ�Ϊ��g��cm��3��GaN��ʽ��ΪMr�����߳�Ϊ________nm��(�г�����ʽ��NAΪ�����ӵ�������ֵ)  |
|||||||||||||||
�� |
��1���� ��Ga2(Fe2O4)3+24H+=2Ga3++6Fe3++12H2O�������ڣ�CaSO4������ ��2����С��5.7��������3���������٣�6mol/L�������ڣ�2mol/L������ ��4��Ga(OH)3+OH��=GaO2��+2H2O������ ��5��Ga2O3+2NH3  2GaN+3H2O������ 2GaN+3H2O������ ��6���٣����۾��塡�����ڣ����Ӿ��塡�����ۣ�4�������ܣ�  |
|||||||||||||||
| ��� | 19 |
|
||||||||||||
���� |
2022Ȫ����� | |||||||||||||
| ��� | ijʪ����п������Һ�к���Na+��Zn2+��Fe2+��Mn2+��Co2+��Cd2+��30 ~60g��L-1 H2SO4�ȣ������м�ֵ��������ȡ��������п�Ĺ���������ͼ�� ��֪��
��1�����к�����ˮ�⡱ʱ���ȼ���������ʯ��ʯ������Һ��pHΪ1.0������һ������Na2S2O8���ټ���ʯ��ʯ������Һ��pHΪ4.0�� ��������ʱ��Mn2+ת��ΪMnO2��ȥ����Ӧ�����ӷ���ʽΪ_______�� �ڡ�����������Ҫ�ɷֳ�MnO2���_______�� �ۡ�������ʱ�������������Na2S2O8����Ԫ�ؽ�����롰�������У���ˮ������Һ�к�������Ũ��Ϊ_______mol��L-1�� ��2�������ӡ�ʱ����Ҫ��Ӧ�����ӷ���ʽΪ_______�� ��3������п��ʱ���ڽ����������¼���Na2CO3�ɵü�ʽ̼��п[ZnCO3��2Zn(OH)2��H2O]���壬ͬʱ�������������塣 �ٲ������������ԭ����_______�� ��ZnCO3��2Zn(OH)2��H2O��ϴ�ӣ������Ƿ�ϴ�����Լ���_______�� ��4����ͬ����������Na2SO4��Һ�ڲ�ͬ�¶�������Na2SO4�����������ͼ��ʾ�����Ӻ�20% Na2SO4�������ʵġ���п��Һ����ֱ��������ˮNa2SO4��������a��Ϊ_______��  |
|||||||||||||
�� |
��1����S2O82��+ Mn2++2H2O= MnO2��+ 2SO42��+4H+��������Fe(OH)3��CaSO4��������1.6 ��10-14������ ��2��Zn+Cd2+= Zn2++Cd������ ��3����Zn2+��CO32������˫ˮ�⣬��ٽ�������ZnCO3��2Zn(OH)2��H2O��CO2���塡������. BaCl2��Һ������ ��4������Ũ�������ȹ��� |
|||||||||||||
| ��� | 20 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | ���������㷺Ӧ����ԭ���ܡ����졢���ӡ��մɵ���������Ҫ��ս�����ʡ���������ʯ(��Ҫ��ѧ�ɷ�Ϊ(Be3Al2Si6O18��������һ������FeO��Fe2O3)����BeO��һ�ֹ����������¡�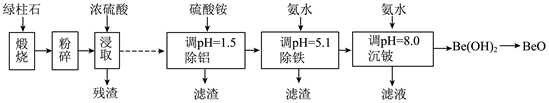 �� �� �ش����⣺ ��1��Be3Al2Si6O18��Be�Ļ��ϼ�Ϊ_______�� ��2�������Ŀ����_______��������Ҫ�ɷ���_______(�ѧʽ)�� ��3������������ѭ��ʹ�õ�������_______(�ѧʽ)�� ��4����ˮBeCl2�������ۺϷ�Ӧ�Ĵ�����BeO��Cl2������C��600~800���Ʊ�BeCl2�Ļ�ѧ����ʽΪ_______�� ��5������ʱ����pH��8.0��ߵ�8.5���������ʧ������ԭ����_______%�� |
|||
�� |
��1��+2��������2���������٣�����Ӧ��ĽӴ�����ӿ췴Ӧ���ʣ���߽�ȡ�ʡ������ڣ�SiO2������ ��3��(NH4)2SO4������ ��4��BeO+Cl2+C 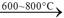 CO+BeCl2������ CO+BeCl2������ ��5��10 |
|||
| ��� | 21 |
|
||
���� |
Ȫ����� | |||
| ��� | H2O2�������Ʊ��������£� ����˵��������� A��2H2O2��2H2O��O2�����Է����У��������淽���Ʊ�H2O2 B������I��������������NO2��O2 C������III�з������ֽⷴӦ D������V��������Ϊ��ѹ���� |
|||
�� |
A | |||
| ��� | 22 |
|
||
���� |
Ȫ����� | |||
| ��� | �Ժ����������Ѱ���Ϊԭ����ȡ����ʵ�֡��Է��ηϡ��������������£� ��֪��������������Ҫ��CaO��Fe2O3������SiO2��V2O3���Ѱ����к�H+��Fe2+��TiO2+��SO42-�����ӡ��ش��������⡣ ��֪��������������Ҫ��CaO��Fe2O3������SiO2��V2O3���Ѱ����к�H+��Fe2+��TiO2+��SO42-�����ӡ��ش��������⡣��1���ڿ����С����ա�ʱ��V2O3ת��ΪNaVO3��д����Ӧ�Ļ�ѧ����ʽ���������������� �� ��2����������Ҫ�ɷ����������������� ���������������� ��H2TiO3�� ��3�����ܽ������̣���һ����VO3��ת��ΪVO2+�����ܵ�ԭ������������������ �� ��4�������������̣�VO2+��������VO2+�����뷴Ӧ��VO2+��H2O2���ʵ���֮��Ϊ�������������� �� ��5������ȡ���͡�����Һ��pH��ͬ������ɷ��Ĵ�����̬��ͬ����VO2+��V2O74���ȣ���������Һ��pH���������������������� ���VO2+����V2O74���������γɡ� ��6�������¡�������������NH3��NH4Cl��Һ����Ũ��Ϊcmol��L��1��pH��6�� �١������������У�VO2+ת��ΪNH4VO3�����ӷ���ʽ�������������� �� ����֪Kb(NH3��H2O)��a��Ksp(NH4VO3)��b��������������Һ��c(VO3��)������������ mol��L��1�����м���ʽ�� ��7��NH4VO3�����յõ�V2O5������������Է������������� ���գ��������ԭ�ϡ� |
|||
�� |
��1��V2O3+Na2CO3+O2 2NaVO3+CO2 2NaVO3+CO2 ��2��CaSO4��H2SiO3��CaSiO3�� ��3���Ѱ����к�Fe2+����VO3����ԭΪVO2+ ��4��2:1�� ��5��V2O74�� ��6����VO2+ + NH4��+ H2O = NH4VO3��+ 2 H+���� ��˵����VO2+ + NH3��H2O = H+ + NH4VO3����VO2+ + NH3+H2O = H+ + NH4VO3�������֣��������������� ��  �� ����7�������� |
|||
| ��� | 23 |
|
||
���� |
2023ȫ���Ҿ� | |||
| ��� | LiMn2O4��Ϊһ������﮵�����������ܵ��㷺��ע�������̿�MnCO3����������Si��Fe��Ni��Al��Ԫ�أ��Ʊ�LiMn2O4���������£� �� �� ��֪��Ksp[Fe(OH)3]=2.8��10-39��Ksp[Al(OH)3]=1.3��10-33��Ksp[Ni(OH)2]=5.5��10-16�� �ش��������⣺ ��1�������ܿ���Ҫ��Ӧ�Ļ�ѧ����ʽΪ_______��Ϊ����ܿ����ʣ��ɲ�ȡ�Ĵ�ʩ_______(��1��)�� ��2����������MnO2��������_______������ʹ��H2O2���MnO2��ԭ����_______�� ��3���ܿ�Ӧ��ɺ�Ӧ������ҺpH=4����ʱc(Fe3+)=_______mol��L-1����ʯ���������pH��7����ȥ�Ľ���������_______�� ��4����������BaS��Һ��ȥNi2+�����ɵij�����_______�� ��5���ڵ����У�������ⷴӦ�����ӷ���ʽΪ_______�����ŵ�ⷴӦ���У�Ϊ���ֵ��Һ�ɷ��ȶ���Ӧ����_______������Һ���ڷ�Ӧ����ѭ�����á� ��6������Ҥ�У�����LiMn2O4��Ӧ�Ļ�ѧ����ʽ��_______�� |
|||
�� |
��1����MnCO3+H2SO4=MnSO4+H2O+CO2���������ڷ������̿��� ��2���ٽ�Fe2+����ΪFe3+��������Fe3+���Դ�H2O2�ֽ⡡���� ��3���� 2.8��10-9��������Al3+������ ��4��BaSO4��NiS������ ��5����Mn2++2H2O  H2��+MnO2��+2H+�������ڼ���MnSO4������ H2��+MnO2��+2H+�������ڼ���MnSO4������ ��6��2Li2CO3+8MnO2  4LiMn2O4+2CO2��+O2�� 4LiMn2O4+2CO2��+O2�� |
|||
| ��� | 24 |
|
||
���� |
2023ȫ���� | |||
| ��� | BaTiO3��һ��ѹ����ϡ���BaSO4Ϊԭ�ϣ���������·�߿��Ʊ���״BaTiO3�� �� �� �ش��������⣺ ��1�������ա�������̼�۵���Ҫ������_______�� ��2�������ա�����������BaCl2��������ˮ��BaS������ˮ��CaS������ȡ��ʱ��Ҫ��Ӧ�����ӷ���ʽΪ_______�� ��3�����ữ������Ӧѡ�õ�����_______(����)�� a��ϡ���ᡡ���� b��Ũ���ᡡ���� c�����ᡡ���� d������ ��4��������պ�IJ���ֱ�������ȡ���Ƿ���У�_______����ԭ����_______�� ��5��������������������BaTiO(C2O4)2�Ļ�ѧ����ʽΪ_______�� ��6�����ȷֽ⡱���ɷ�״���ᱵ��������n(CO2):n(CO)= _______�� |
|||
�� |
��1������ԭ������BaSO4��ԭ������ ��2��S2����Ca2+��CaS�� ��3��c������ ��4���ٲ����С������ڲ����е��������ᷴӦ���ɵ��ж�����H2S����Ⱦ����������CaS�����ᷴӦ���ɿ�����ˮ��CaCl2������BaCl2��Һ�л���CaCl2��������ȥ���������ò�Ʒ�Ĵ��Ƚ��͡����� ��5��BaCl2+TiCl4+H2O��2(NH4)2C2O4��BaTiO(C2O4)2��+4NH4Cl+2HCl ��6��1:1 |
|||
| ��� | 25 |
|
||||||||||||||||||||||||||||||||||||||
���� |
2022�����߿� | |||||||||||||||||||||||||||||||||||||||
| ��� | ����ʯ����Ҫ��ѧ�ɷ�ΪCaMg(CO3)2����������������ԼΪ2.1%��Fe2O3��1.0%��SiO2�����ð���ʯ�Ʊ��ߴ��ȵ�̼��ƺ�����þ������ʾ��ͼ���¡� ��֪��
��2��NH4Cl������̼��Ʋ�Ʒ��Ӱ�����±���ʾ��
����CaCO3���ȼ���ֵΪ��ҺA�иơ�þȫ����̼������ʽ����ʱ������IJ�Ʒ��CaCO3���ȡ� �ٽ��͡����ơ���������Ҫ����CaO��ԭ����___________�� �ڳ��Ʒ�Ӧ�����ӷ���ʽΪ___________�� �ۡ����ơ����̲�����ѡ��n(NH4Cl):n(CaO)�ı���Ϊ___________�� �ܲ�Ʒ��CaCO3���ȵ�ʵ��ֵ���ڼ���ֵ��ԭ����___________�� ��3������þ�������У�ȡ����B��һ��Ũ�ȵ�(NH4)2SO4��Һ��ϣ���ַ�Ӧ��MgO�Ľ����ʵ���60%����������MgO�Ľ����������Һ���������������տɴ�98.9%���ӻ�ѧƽ��ĽǶȽ��ͽ����������ԭ����___________�� ��4������C�к��е�������___________�� ��5���������п�ѭ�����õ�������___________�� |
|||||||||||||||||||||||||||||||||||||||
�� |
��1��CaMg(CO2)2 CaO+MgO+2CO2�� CaO+MgO+2CO2����2����������Ksp[Ca(OH)2]��Ksp[Mg(OH)2]����һ����NH4Cl��Һ�У��������ƻ���Ȼ�立�Ӧ��������þ���ܣ���CaO�Ƚ��������� ��Ca2+2NH3��H2O+CO2��CaCO3��+2NH4++H2O ��2.4��1������ ��Ksp[CaCO3]��sp[MgCO3]��CaCO3������������������Ҳ��ת��Ϊ̼��ơ����� ��3��MgO+H2O=Mg(OH)2��Mg(OH)2+2NH4+=Mg2++2NH3+2H2O����������ݳ���ƽ�������ƶ������� ��4��Fe2O3��SiO2��CaSO4��MgO ��5��NH4Cl��(NH4)2SO4��CO2��NH3 |
|||||||||||||||||||||||||||||||||||||||
| ��� | 26 |
|
||
���� |
2022ɽ���߿� | |||
| ��� | ʵ�����Ʊ�KMnO4����Ϊ�ٸ�����������ǿ���Խ�������KClO3����MnO2�Ʊ�K2MnO4����ˮ�ܺ���ȴ������ҺpH�������ԣ�K2MnO4�绯����KMnO4��MnO2���ۼ�ѹ���ˣ�����Һ����Ũ������ȴ�ᾧ���ټ�ѹ���˵�KMnO4������˵����ȷ���� A�������ô���������Ӧ�� B��������NaOH��ǿ���Խ��� C������K2MnO4ֻ���������� D��MnO2ת��ΪKMnO4������ת����ԼΪ66.7% |
|||
�� |
D | |||
| ��� | 27 |
|
||||||||||||
���� |
2022ɽ���߿� | |||||||||||||
| ��� | ��ѹ�ԭ����ֱ�Ӵ���Һ����ȡ�����ۡ�����ͭ����(��Zn��FeԪ�ص�����)Ϊ��Ҫԭ���Ʊ�Cu�۵Ĺ����������£������õ������ݼ��±���
A������X��Ҫ�ɷ���Fe(OH)3��S������MΪZn B����ȡʱ������O2ѹǿ�ɴٽ��������ӽ��� C���к͵�pH�ķ�ΧΪ3.2~4.2 D����ԭʱ��������Һ���������Cu������ |
|||||||||||||
�� |
D | |||||||||||||
| ��� | 28 |
|
||
���� |
2022���ո߿� | |||
| ��� | ������һ�������Դ����ɫ�������⼼���о�������Ҫ���塣 (1)��CuCl��H2O�ȵ�ѭ�����⡱�����ܽ⡢��⡢��ˮ����ȷֽ�4�����裬�������ͼ��ʾ��  �ٵ�������ӽ���Ĥ�����н��С�������Ϊ����CuCl2����Һ��������Ϊ���ᣬ��������CuCl2��ת��ΪCuCl42�������ʱ������������Ҫ�缫��ӦΪ�� (�õ缫��Ӧʽ��ʾ)�� �ڵ�����ˮ����ȷֽ�����ʿ�ѭ��ʹ�á�����ˮ����ȷֽ�����У��������ϼ۱仯��Ԫ��������������(��Ԫ�ط���)���� (2)��Fe��HCO3����H2O��ѭ������ͼ��ᡱ��ԭ��Ϊ:���ܱ������У�����������CO2�Ƶõ�NaHCO3��Һ��Ӧ������H2��HCOONa��Fe3O4��Fe3O4�پ����������Ʒת��ΪFe�� ��ʵ���з��֣���300��ʱ���ܱ�������NaHCO3��Һ�����۷�Ӧ����Ӧ������FeCO3���ɲ��ų�H2���÷�Ӧ�����ӷ���ʽΪ�������������������� �����ŷ�Ӧ���У�FeCO3Ѹ��ת��Ϊ����Fe3O4��x������Fe3O4��x��HCO3��ת��ΪHCOO���Ĵ���������ܷ�Ӧ������ͼ��ʾ������Ԫ�ص縺�Եı仯���ɡ���ͼ��ʾ�ķ�Ӧ����������Ϊ��������������  ��������������ͬʱ�����Fe��ת���ʡ�HCOO���IJ�����c(HCO3��)�仯����ͼ��ʾ��HCOO���IJ�����c(HCO3��)���Ӷ�����Ŀ���ԭ����������  (3)������ת������Դ�ۺ����ýǶȷ�������Fe��HCO3����H2O��ѭ������ͼ��ᡱ���ŵ��������� |
|||
�� |
(1)��CuCl2��+2Cl����e��=CuCl42������Cu��O (2)��Fe+2HCO3��  FeCO3��+CO32��+H2������H�ĵ縺�Դ���Fe��С��O���ڻ���Fe3O4��x���棬H2����ΪHԭ�ӣ�һ�������ڴ������������ϣ��Դ����磬һ�������ڴ������������ϣ��Դ����磬ǰ����HCO3�����Դ������̼��ϣ�������HCO3�����Դ�������ǻ����������H2O��HCO3��ת��ΪHCOO��������c(HCO3��)���ӣ�����FeCO3��H2�����ʸ��졢������������HCOO�������ʸ��졢����Ҳ���� FeCO3��+CO32��+H2������H�ĵ縺�Դ���Fe��С��O���ڻ���Fe3O4��x���棬H2����ΪHԭ�ӣ�һ�������ڴ������������ϣ��Դ����磬һ�������ڴ������������ϣ��Դ����磬ǰ����HCO3�����Դ������̼��ϣ�������HCO3�����Դ�������ǻ����������H2O��HCO3��ת��ΪHCOO��������c(HCO3��)���ӣ�����FeCO3��H2�����ʸ��졢������������HCOO�������ʸ��졢����Ҳ����(3)��Ч�����á�ԭ�������ʸߡ�����Ⱦ |
|||
| ��� | 29 |
|
|||||||||||||||
���� |
2022�㶫�߿� | ||||||||||||||||
| ��� | ϡ��(RE)�����硢�Ƶ�Ԫ�أ��Ǹ߿Ƽ���չ�Ĺؼ�֧�š��ҹ��Ϸ����е�ϡ����������ӽ�����������һ�ִӸ����(����������Ԫ��)����ȡϡ���Ĺ������£� ��֪���¹���(C11H23COOH)�۵�Ϊ44��;�¹����(C11H23COO)3RE��������ˮ���ù��������£�ϡ�����ӱ���+3�۲���;(C11H23COO)2Mg��Ksp=1.8��10��8;Al(OH)3��ʼ�ܽ�ʱ��pHΪ8.8;�йؽ������ӳ��������pH���±���
(2)������1��ǰ����NaOH��Һ��pH�����������ķ�Χ�ڣ��ù�����Al3+������Ӧ�����ӷ���ʽΪ���������������������������������� (3)������2�����˱��м�ⲻ��MgԪ�أ���Һ2��Mg2+Ũ��Ϊ2.7 g��L��1��Ϊ�����ܶ����ȡRE3+��������¹����Ƶļ���������Ӧȷ��������2��ǰ����Һ��c(C11H23COO��)������������mol��L��1(������λ��Ч����)���� (4)�١����Ƚ��衱�����ڼӿ�RE3+�ܳ�����߲��ʣ���ԭ������������������������������ �ڡ�����X���Ĺ���Ϊ���������������������������ٹ�Һ���롣�� (5)�ù����У�������ѭ�����õ�����������������(д��ѧʽ)���� (6)ϡ��Ԫ����(Y)�������Ʊ����ԵĺϽ������Pt3Y�� �ٻ�ԭYCl3��PtCl4�������Ʊ�Pt3Yʱ������1 mol Pt3Yת������������mol���ӡ��� ��Pt3Y/C��������ȼ�ϵ�ص缫����ʱ�����ڼ�����Һ�и�Ч��O2�Ļ�ԭ�������ĵ缫��ӦΪ���������������������������������� |
||||||||||||||||
�� |
(1)Fe2+ (2)4.7��pH<6.2��Al3++3OH����Al(OH)3�� (3)4.0��10��4 (4)�ټ��ȿ�����߷�Ӧ�������˶��ٶȣ����������ܼ������ʵĽӴ������ʹ�ܳ������ף�����ܳ��ٶȣ���߲��ʡ�����ȴ�ᾧ (5)MgSO4 (6)��15����O2+4e��+2H2O��4OH�� |
||||||||||||||||
| ��� | 30 |
|
||
���� |
2022���ϸ߿� | |||
| ��� | ����⳧����������һ�ּ��������£� ����˵��������� A�������á��ա������������ڳIJ��� B��������Һ���ܷ����������������������Ч�� C���ϳɲ��в�����Ҫ��Na3AlF6��CO2�������������������� D����Һ�ɻ��ս���������ѭ������ |
|||
�� |
C | |||
| ��� | 31 |
|
||||||||||||
���� |
2022ȫ���� | |||||||||||||
| ��� | ����п(ZnSO4)���Ʊ����ֺ�п���ϵ�ԭ�ϣ��ڷ�������ơ�ҽѧ�������Ӧ�á�����п������п���Ʊ�����п�����Ҫ�ɷ�ΪZnCO3������ΪSiO2�Լ�Ca��Mg��Fe��Cu�ȵĻ�������Ʊ��������£� ���������漰���ӵ����������ܶȻ��������±���
(1)��п������������п�Ļ�ѧ����ʽΪ������������������������������������ (2)Ϊ�����п�Ľ�ȡЧ�����ɲ�ȡ�Ĵ�ʩ������������������������������������ (3)��������X����ҺpH=5��������ʹ�õ�X������������(����)���� A.NH3��H2O������B.Ca(OH)2������C.NaOH �����ٵ���Ҫ�ɷ��������������������������������������� (4)��80~90�����Һ���з�����������KMnO4��Һ��ַ�Ӧ����ˣ�����������MnO2���ò���Ӧ�����ӷ���ʽΪ���������������������������������� (5)��Һ���м���п�۵�Ŀ���������������������������������� (6)��������ŨH2SO4��Ӧ�����ͷ�HF��ѭ�����ã�ͬʱ�õ��ĸ��������������������������������� |
|||||||||||||
�� |
(1)ZnCO3 ZnO+CO2�� ZnO+CO2��(2)�����պ�IJ������顢�ʵ���������ϡ�����Ũ�ȡ����Ȼ�����(�����������ʩ����������) (3)B��SiO2��Fe(OH)3��CaSO4 (4)MnO4��+3Fe2++7H2O  MnO2��+3Fe(OH)3��+5H+ MnO2��+3Fe(OH)3��+5H+(5)��Cu2+�û���������ȥ��Һ�е�Cu2+ (6)CaSO4��MgSO4 |
|||||||||||||
| ��� | 32 |
|
|||||||||||||||||||||||||
���� |
2022ȫ���Ҿ� | ||||||||||||||||||||||||||
| ��� | �Ͼ�Ǧ���ص�Ǧ������Ҫ����PbSO4��PbO2��PbO��Pb����������Ba��Fe��Al���λ�������ȡ�Ϊ�˱����������������Ǧ��Դ��ͨ����ͼ����ʵ��Ǧ�Ļ��ա� һЩ���ܵ���ʵ��ܶȻ��������±���
(1)�ڡ�������PbSO4ת����Ӧ�����ӷ���ʽΪ�������������������������������ó����ܽ�ƽ��ԭ������ѡ��Na2CO3��ԭ���������������������������������� (2)�ڡ������У�����Na2CO3����ʹǦ����BaSO4��ȫת����ԭ�������������������������� (3)�ڡ�������У����������(CH3COOH)����Ҫ����H2O2�� (��)�ܱ�H2O2��������������������;�� (��)H2O2�ٽ��˽���Pb�ڴ�����ת��Ϊ(CH3COO)2Pb���仯ѧ����ʽΪ��������������������;�� (��)H2O2Ҳ��ʹPbO2ת��Ϊ(CH3COO)2Pb��H2O2�������������� (4)�����������Һ��pHԼΪ4.9����������Ҫ�ɷ��������������������������� (5)����Ǧ������Һ�У����������������������� |
||||||||||||||||||||||||||
�� |
(1)PbSO4(s)+CO32- (aq)��PbCO3(s)+SO42- (aq)��PbSO4������Һ�д���ƽ��PbSO4(s)  Pb2+(aq)+SO42-(aq)��������̼������Һʱ����ΪKsp(PbCO3)<Ksp(PbSO4)�����Կ�����PbCO3�������Ӷ�ʹ����ƽ�����ƣ��÷�Ӧ��ƽ�ⳣ�� Pb2+(aq)+SO42-(aq)��������̼������Һʱ����ΪKsp(PbCO3)<Ksp(PbSO4)�����Կ�����PbCO3�������Ӷ�ʹ����ƽ�����ƣ��÷�Ӧ��ƽ�ⳣ�� �����Լ���������ȫת�� �����Լ���������ȫת��(2)BaSO4(s)+CO32-(aq)  BaCO3(s)+SO42-(aq)��ƽ�ⳣ�� BaCO3(s)+SO42-(aq)��ƽ�ⳣ�� ��ԶС��105����˸÷�Ӧ���еij̶Ƚ�С������ʹBaSO4��ȫת�� ��ԶС��105����˸÷�Ӧ���еij̶Ƚ�С������ʹBaSO4��ȫת��(3)(��)Fe2+ (��)Pb+H2O2+2CH3COOH  (CH3COO)2Pb+2H2O (CH3COO)2Pb+2H2O(��)����ԭ�� (4)Al(OH)3��Fe(OH)3 (5)Na+��Ba2+ |
||||||||||||||||||||||||||
| ��� | 33 |
|
||||||||||
���� |
2022���� | |||||||||||
| ��� | ȫ������Դ����������,���κ���ﮡ�Խ��Խ�ܵ����ӡ�ij��ȤС��ȡ�κ�ˮ����Ũ���ͳ������Ӻ�,�õ�Ũ��±ˮ(����Na+��Li+��Cl-������Mg2+��Ca2+),���������������ͨ���Ʊ�̼�������ȡﮡ� 25��ʱ������ʵIJ�������: LiOH���ܽ��:12.4 g/100 g H2O
 ��������Li2CO3���ܽ������ �ش���������: (1)������1��Ϊ�������������� (2)����Һ1���м�����������Li2CO3��Ŀ������������������������������ (3)Ϊ���Li2CO3���������ʹ���,������A������Ϊ������������������������ϴ�ӡ��� (4)��ͬѧ�����á������Ƽ����ԭ���Ʊ�Li2CO3���������Ϻ�,�������Գ����µ�Li2CO3�в�ͬ������:���ǰ�ɫ����;����δ����Һ�з��������Ϊ̽��LiHCO3������,������LiCl��Һ�뱥��NaHCO3��Һ��������,��������Ա仯,�����Һ����Dz���������ð��,�������ɰ�ɫ��������������˵��,�ڸ�ʵ��������LiHCO3����������(��ȶ������ȶ���),�йط�Ӧ�����ӷ���ʽΪ�������������������������� (5)���ǽ��(4)��̽�����,�⽫ԭ����������Һ2������Na2CO3��Ϊͨ��CO2����һ�Ķ��ܷ�ﵽ��ͬ��Ч��,��������жϲ��������������������������������� |
|||||||||||
�� |
(1)Mg(OH)2�� (2)��Ca2+ת����CaCO3������ȥ,ͬʱ�����������ʡ� (3)����Ũ�������ȹ��ˡ� (4)���ȶ���Li++HCO3- =LiHCO3,2LiHCO3 =Li2CO3��+CO2��+H2O�� (5)�ܴﵽ��ͬЧ��,��Ϊ��Ϊͨ�������CO2,LiOHת��ΪLiHCO3,���(4)��̽�����,LiHCO3��ܿ�ֽ����Li2CO3,������һ�Ķ��ܴﵽ��ͬ��Ч�� |
|||||||||||
| ��� | 34 |
|
||
���� |
2022���� | |||
| ��� | �ø����Ͻ𣨺�����Ni��Co���ʣ�����������Ĺ����������£� ����˵��������� A�������������������庬��H2 B�������ӡ���Ŀ���dz�ȥNi��CoԪ�� C��������δ�������۸������� D��������2������Ҫ�ɷ���Fe₂(C2O4)3 |
|||
�� |
D | |||
| ��� | 35 |
|
||
���� |
2022���� | |||
| ��� | ��ú���ǻ�糧�Ĵ��ڹ̷ϡ���ij�糧�ķ�ú��Ϊԭ�ϣ���Ҫ��SiO2��Al2O3��CaO�ȣ������Ĺ����������£� �ش��������⣺ ��1����������ʱ�ʵ����µ���ҪĿ������������������ ��Al2O3������Ӧ�����ӷ���ʽΪ�������������� �� ��2��������������Ҫ�ɷֳ�����Al2O3�⣬������������������ ��ʵ���ã�5.0 g��ú�ң�Al2O3����������Ϊ30%���������������õ�3.0 g����������Al2O3����������Ϊ8%����Al2O3�Ľ�����Ϊ�������������� �� ��3����������ʱ����ϵ���������ʵ��ܽ����������ͼ��ʾ������K2SO4������Ŀ������������������ ��������������ѷ���Ϊ�������������� �� ��4�������ա�ʱ����Ҫ��Ӧ�Ļ�ѧ����ʽΪ�������������� �� ��5����ˮ������õ��ġ���Һ2���ɷ����������������� ����ѭ��ʹ�á�  |
|||
�� |
��1����߽����ʣ�����߽������ʣ���Al2O3+6H+ = 2Al3++3H2O�� ��2��SiO2��CaSO4��84%�� ��3��ʹ�������Ԫ��ת��Ϊ����������ͬʱ��֤���崿�ȣ������ܽ�����ȴ�ᾧ�� ��4��2KAl(SO4)2  K2SO4+Al2O3+3SO3����4KAl(SO4)2 K2SO4+Al2O3+3SO3����4KAl(SO4)2 2K2SO4+2Al2O3+6SO2��+3O2���� 2K2SO4+2Al2O3+6SO2��+3O2������5���������� |
|||
| ��� | 36 |
|
||
���� |
2022�人���� | |||
| ��� | ���ᣨH2WO4����һ����Ҫ�Ļ���ԭ�ϣ�����ýȾ�����������������ϵȡ�һ���Ժ��ٿ���Ҫ�ɷ���FeWO4��MnWO4��������Si��P��As��Ԫ�ص����ʣ�Ϊԭ���Ʊ�����Ĺ�ҵ��������ͼ��ʾ�� ��֪�� �١�����1���ijɷ���Mn3O4��Fe2O3�� �ڡ�ˮ��������Һ����Ҫ������ΪWO42����PO43����AsO43����AsO33����SiO32���� ��Ksp[(Mg3(PO4)2]��1.0��10��24�� �ش��������⣺ ��1����̬Mnԭ����δ�ɶԵĵ�����Ϊ�������������� �� ��2��FeWO4����������"ʱ�Ļ�ѧ��Ӧ����ʽΪ�������������� �� ��3��������2������Ҫ�ɷ����������������� ���������ᡰ����pH��Ҫ�ڼ�����������½��У���е�Ŀ������������������ �� ��4�������ס��顱������P��AsԪ����Mg3(PO4)2��Mg3(AsO4)2��ʽ�������������������м���NaClO��Һ��Ŀ������������������ �� ��5��������Һ1����c(Mg2+)��0.01mol��L��1ʱ����ʱPO43���Ƿ������ȫ����ʽ����˵���������������� �� ��6�������١�����Ҫ���ˡ�ϴ�ӣ���ϴ�ӵľ������Ϊ�������������� �� |
|||
�� |
��1��5 ��2��4FeWO4+O2+4Na2CO3  2Fe2O3+4CO2+4Na2WO4������ 2Fe2O3+4CO2+4Na2WO4������ ��3�������� ��.H2SiO3������ ��.ʹ��������ӳ�ַ�Ӧ����ֹ���ɹ��ὺ�塡���� ��4����P��AsԪ��ת��ΪPO43-��AsO43-�������ɳ�����ȥ������ ��5��c(Mg2+)��0.01mol��L��1ʱ������c3(Mg2+)c2(PO43-)��1.0��10��24����c(PO43-)=1.0��10��9��1.0��10��5��˵��PO43-������ȫ |
|||
| ��� | 37 |
|
|||||||||||||||
���� |
2022����һ�� | ||||||||||||||||
| ��� | ��(Sb)��������ȼ�����缫���ϡ�ֵ���������ʵ�ԭ���ϡ�һ���Ի����(��Ҫ�ɷ�ΪSb2S3��������Fe2O3��Al2O3��MgO��SiO2��)Ϊԭ����ȡ��Ĺ������£� ��֪����Һ�н������ӿ�ʼ��������ȫ������pH���±���ʾ��
��1�����ܽ���ʱ����������S��Sb2S3�������Ļ�ѧ����ʽΪ___________�� ��2������ԭ��ʱ����Sb��Ŀ���ǽ�___________��ԭ����߲���Ĵ��ȡ� ��3����ˮ�⡱ʱ�������ҺpH=2.5�� ��Sb3+����ˮ������ӷ���ʽΪ___________�� �������ܴٽ���ˮ�ⷴӦ�Ĵ�ʩ��___________(����ĸ)�� A�������¶ȡ��������������� B������c(H+) C������c(Cl��) D������Na2CO3��ĩ ��Ϊ����ˮ������л���Fe(OH)3��Fe3+Ũ��ӦС��___________mol��L��1�� ��4������Һ���к��еĽ�����������___________������Һ����ͨ������___________(�ѧʽ)���壬�ٽ���ҺpH����3.5��������Fe(OH)3����������������Ũ�������ɷ���___________����ѭ��ʹ�á� ��5��Sb����SbCl4������Ƶã������ĵ缫��ӦʽΪ___________�� |
||||||||||||||||
�� |
��1��Sb2S3+6FeCl3=3S+2SbCl3+6FeCl2������ ��2��Fe3+��������3�������� ��.Sb3++Cl��+H2O��SbOCl+2H+������ ��.ACD������ ��.10��2.9������ ��4�������� ��.Al3+��Fe2+��Mg2+������ ��.Cl2������ ��.�ܽ������� ��5��SbCl4-+3e��=Sb+4Cl�� |
||||||||||||||||
| ��� | 38 |
|
||
���� |
2020����12�� | |||
| ��� | �Էϴ������л��տ���Ч���ý�����Դ��ij�ϴ�����Ҫ����TiO2��V2O5��WO3��SiO2��Al2O3��һ�ֻ������ù��յ��������£� ��֪��25��ʱ��Ksp(CaWO4)��8.7��10��9��Ksp[Ca(OH)2]��5.5��10��6�� �ش��������⣺ ��1�������ա������к���NaVO3��NaAlO2��NaVO3��VԪ�صĻ��ϼ�Ϊ������������ ��Al2O3ת��ΪNaAlO2�Ļ�ѧ����ʽΪ���������������� �������ա�ʱ����ʹ���մ�������ԭ�������������������������� �� ��2����ˮ����������Һ�к��е������ӳ�OH����CO32����AlO2����VO3���⣬���������������������� �� ��3������pH��8����Ŀ�������������������������� ��c(CH3COO��)��c(NH4+)��c(NH3•H2O)c(OH��)c(H+) ��4������NH4VO3������V2O5��������һ�ּ������壬���������������������� �����Լ����ƣ����պ�ѭ�����á� ��5�������١������У�����Һ��c(OH��)���������������� ��д������ʽ��mol��L��1ʱ����Һ��WO42��ǡ����ȫ����������Ũ�ȵ���1��10��5mol��L��1����Ӧֹͣ����ʯ���顣 ��6������������ϴCaWO4���H2WO4�����ʵ��֤��CaWO4�Ѿ�ת����ȫ��ʵ�鷽����ȡ�������һ�ε���ϴҺ���Թ��У����������������������� �� |
|||
�� |
��1��+5��Al2O3+Na2CO3 2NaAlO2+CO2����̼�����ڸ��������մɵ���Ҫ�ɷֶ������跴Ӧ���ʲ������մɱ��ա� 2NaAlO2+CO2����̼�����ڸ��������մɵ���Ҫ�ɷֶ������跴Ӧ���ʲ������մɱ��ա���2��WO42����SiO32�� ��3����Al��Si�����ɹ������������������ ��4��ϡ���� ��5��  ��6�������м������̼������Һ���������ɣ���֤����ת����ȫ�� |
|||
| ��� | 39 |
|
||
���� |
2022Ȫ������ | |||
| ��� | �ؼ��仯�����������ȡ�������뵼����ϡ�Ga��Alͬ���壬��ѧ�������ơ���ij��������(��Ҫ��Ga2O3��Fe2O3)����ȡ�ز��Ʊ�GaN�Ĺ����������£� ����˵��������� A���������ʱ������ӦGa2O3��2NaOH=2NaGaO2��H2O B����������Ҫ�ɷ�ΪFe(OH)3 C������⡱�н���Ga���������� D���Ʊ�GaN�ķ�Ӧ�У�NH3�������� |
|||
�� |
B | |||
| ��� | 40 |
|
||
���� |
2022Ȫ������ | |||
| ��� | ���������Ҫ��MnSO4��MnO2��PbSO4��CaSO4��������SiO2��Fe2(SO4)3�����õ����������Ǧ�Ĺ�������ͼ��ʾ�� ��֪��Ksp(PbSO4)��2.6��10−8��Ksp(PbCO3)��7.4��10−14��Ksp(CaCO3)��2.8��10−9�� �ش��������⣺ ��1������ԭ�����ʱ��MnO2����ԭ�����ӷ���ʽΪ������������������ �� ��2��������Һ�����е�������Ҫ��MnSO4��������CaSO4�������������������� �������Ӻ�õ�����MnSO4��Һ����ͼΪMnSO4���ܽ�����¶ȵı仯���ߣ��Ӿ���MnSO4��Һ�л��MnSO4����ķ���Ϊ������������������ ��  ��3����ƽ���ƶ��ĽǶȣ���������Ǧ����ӦPbSO4 + 2CH3COO−  ��Pb(CH3COO)2 + SO42-��ԭ���������������������� �� ��Pb(CH3COO)2 + SO42-��ԭ���������������������� ����4��������Ǧ����������Һ��c(Pb2+)��c(Ca2+)��0.1mol��L−1��Ϊʵ��Ǧ��Ƶķ��룬Ӧ������Һ��c(CO32-)�ķ�ΧΪ���������������� mol��L−1��������Һ�н�������Ũ��С��10−5mol��L−1��������Ϊ�����ӳ�����ȫ���� ��5������Ǧ��ʱ������ͬŨ�ȵ�(NH4)2CO3��Һ����NH4HCO3��Һ��������Pb2(OH)2CO3��ԭ���������������������� �� ��6������Ǧ��ʱ��Һ��Ҫ����Ҫ�ɷֳ�CH3COONH4�⣬���������������������� �� |
|||
�� |
��1��MnO2+PbS+4H++SO42-��Mn2++PbSO4+S+2H2O ��2��FeSO4 �����ᾧ�����ȹ��ˣ�ϴ�ӣ���ϴ�ӡ��ɲ��� ��3��CH3COO−���Pb2+�γ��ѵ������ʣ�ʹPbSO4 (s)=Pb2+(aq)+ SO42-(aq)ƽ�������ƶ� ��4��7.4��10−9~2.8��10−8 ��5��(NH4)2CO3��Һ���Ը�ǿ�������������𰸣� ��6��(NH4)2SO4 |
|||
| ��� | 41 |
|
||
���� |
2022Ȫ�ݶ��� | |||
| ��� | ��ҵ��ͭ��ʯ����Ҫ�ɷ�ΪCuS��CuO����ȡ��������Ҫ������ͼ��ʾ������˵��������� A������XΪSO2 B������aΪ����Ũ������ȴ�ᾧ������ C�������еķ�Ӧ���漰������ԭ��Ӧ D���������е��������ͭ�������貹������ |
|||
�� |
D | |||
| ��� | 42 |
|
||||||||||||||||||
���� |
2022Ȫ�ݶ��� | |||||||||||||||||||
| ��� | ij��п���л������������븻���ܵĹ����������£� ��֪�� ��ԭ����������Ҫ�ɷ֣��ܵ��л���[ (C3H6NS2)2Co]��ZnSO4��6H2O��Fe4(OH)2(SO4)5�� �ڡ�������������Ԫ�ص���Ҫ�ɷ֣�CoO��Co3O4 ��CoSO4���۲���������������������ʽ����ʱ��Һ��pH���±���
��1��Fe4(OH)2(SO4)5 ����Ԫ�صĻ��ϼ�Ϊ���������������������������������� �� ��2���������Һ�У���Ҫ�Ľ���������Ϊ���������������������������������� �� ��3�������ա�����ҪĿ�������������������������������������� �� ��4������ԭ������ʱ����Ԫ�ط�����ԭ��Ӧ�����ӷ���ʽΪ���������������������������������� �� ��5����֪��λ��∆E��0ʱ����������������Ӧ���Է�����∆EԽ��ӦԽ�����С� ∆E=E(H2O2/H2O)�� E[Co(��)/Co(��)]��E(H2O2/H2O)��E[Co(��)/Co(��)]��pH�Ĺ�ϵ����ͼ��������������ʱ����ԭ����Һ�����Լ�����ȷ����Ϊ���������������������������������� ��ѡ����ţ������������������������������������������������������������������������������������������������������� �� a��ֱ�Ӽ���H2O2 b���ȼ���NaOH��Һ������pH���ټ���H2O2 c���ȼ���H2SO4 ��Һ������pH���ټ���H2O2  ��6������ϴ���ɳ�ȥ����������Fe(OH)3��Zn(OH)2 �����ʣ�Ӧ������Һ��pH��ΧΪ�� |
|||||||||||||||||||
�� |
��1��+3 ��2��Zn2+ ��Fe3+ ��3�����л���ת��Ϊ��̬�����ȥ������ת��Ϊ�ܵ������� ��4��Co3O4+ SO32�� + 6H+= 3Co2++ SO42�� + 3H2O������������ ��5��b��∆E��0����Ӧ�ܹ����У���pHԽ��∆E Խ��ӦԽ������ ��6��1.1~2.2 |
|||||||||||||||||||
| ��� | 43 |
|
||||||||||||
���� |
2022�人��� | |||||||||||||
| ��� | �Ժ��Ѹ�¯��(��Ҫ�ɷ�ΪTiO2������������CaO��CaO��Fe2O3��SiO2)Ϊԭ������BaTiO3�Ĺ����������£� ��ؽ�������c(Mn+)��0.1mol/Lʱ���γ��������������pH��Χ���£�
��2��������Һ����Ti��TiO2+��ʽ���ڣ������������Ҫ��Ӧ���ӷ���ʽΪ_______�� ��3��������Һ���м���Na2SO3��Ŀ����_______�� ��4������pH����pH��Χ��_______�� ��5�����˵õ�BaTiO(C2O4)2•4H2O��Ҫ����ϴ�ӡ���ѹ��ɣ���������Ƿ�ϴ���ķ�����__�� ��6���������������£�BaTiO(C2O4)2•4H2O��800�����յõ�BaTiO3���÷�Ӧ�Ļ�ѧ����ʽΪ_______�� |
|||||||||||||
�� |
��1��CaSO4������ ��2��TiO2+2H+=TiO2++H2O������ ��3����ԭFe3+��������4��0.5��1.5������ ��5�������һ��ϴ��Һ�м��������ữ��Ȼ���ټ�������������û�а�ɫ������������ϴ�Ӹɾ�����֮��û��ϴ�Ӹɾ������� ��6�������� BaTiO(C2O4)2•4H2O  BaTiO3+2CO+2CO2+4H2O BaTiO3+2CO+2CO2+4H2O |
|||||||||||||
| ��� | 44 |
|
||||||||||||||||||||||||||||||
���� |
2022����������ĩ | |||||||||||||||||||||||||||||||
| ��� | ��ҵ�����������ʵĸ���Ʒ���������Ʊ�����������NiSO4��6H2O�� ��1���Ʊ���Ni2+��Һ  ��֪��i.���������������Ͻ���Ԫ�صİٷֺ�����
���������ݣ���ת¯����������ҪĿ���ǣ�������Ԫ�أ���ȥ����___________�� �ڡ������Һ��ʱ���������Ͻ���������H2SO4��Һ���������Һ��������������������������___________�����һ��ʱ���������Ni������������Ϊ��ֹNi��������NiSO4��6H2O�IJ��ʣ�����������Һ�м���___________(���Լ�)�� ��2���Ʊ�NiSO4��6H2O  ��֪�������£�����������ȫת��Ϊ�������������pH��
����֪Ni(OH)2��KspΪ5.48��10��16����Һ1��c(Ni2+)=1.37mol/L���������˵������ͨ��������Һ��pH��ȥCu2+��ԭ��___________��(��֪��lg5=0.7) �۴���Һ3�л�ȡNiSO4��6H2O�IJ�����___________��ϴ�ӡ���� |
|||||||||||||||||||||||||||||||
�� |
��1������Ԫ�غ���Ԫ�ء����� ��.H2������ ��.CuSO4��Һ������ ��2����ClO��+2Fe2++2H+=2Fe3++Cl��+H2O������ ��.��c(Ni2+)=1.37mol/L��֪����Һ��c(OH��)=  =2��10��8mol/L����ҺpH=6.3��С��ͭ������ȫ������pH=6.7������ ��.����Ũ������ȴ�ᾧ������ =2��10��8mol/L����ҺpH=6.3��С��ͭ������ȫ������pH=6.7������ ��.����Ũ������ȴ�ᾧ������ |
|||||||||||||||||||||||||||||||
| ��� | 45 |
|
||
���� |
2021���� | |||
| ��� | �Ͼ�̫���ܵ��CIGS���нϸߵĻ������ü�ֵ������Ҫ���ΪCuIn0.5Ga0.5Se2��ij̽��С����մ���������ͼ�� �ش��������⣺ ��1����(Se)����Ϊͬ��Ԫ�أ�Se������������Ϊ___����(Ga)����(In)λ��Ԫ�����ڱ���IIIA�壬CuIn0.5Ga0.5Se2��Cu�Ļ��ϼ�Ϊ___�� ��2���������������������Ҫ������ԭ��Ӧ�Ļ�ѧ����ʽΪ____�� ��3��25��ʱ����֪��Kb(NH3��H2O)��2.0��10��5��Ksp[Ga(OH)3]��1.0��10��35��Ksp[In(OH)3]��1.0��10��33��Ksp[Cu(OH)2]��1.0��10��20��������Һ����c(Cu2+)=0.01mol��L��1��������������Ũ��С��1.0��10��5mol��L��1ʱ������ȫ��In3+ǡ����ȫ����ʱ��Һ��pHԼΪ___(����һλС��)������������6.0mol��L��1��ˮ���������۲쵽��ʵ��������������ɫ������Ȼ��___��Ϊ̽��Ga(OH)3�ڰ�ˮ���ܷ��ܽ⣬���㷴ӦGa(OH)3+NH3��H2O  [Ga(OH)4]��+NH4����ƽ�ⳣ��K=___�� [Ga(OH)4]��+NH4����ƽ�ⳣ��K=___��(��֪��Ga3++4OH��  [Ga(OH)4]��K��= [Ga(OH)4]��K��= ��1.0��1034) ��1.0��1034)��4������������SOCl2���ǰ��Ҫϴ�ӡ��������������SO42���Ƿ�ϴ�����Լ���___�����������ˡ���SOCl2�������ǽ���������ת��Ϊ�Ȼ����___�� ��5����������������������з����Ļ�ѧ��Ӧ����ʽΪ___�� |
|||
�� |
��1����6��������+1 ��2��Cu2O+H2O2+2H2SO4=2CuSO4+3H2O������ ��3����4.7����������ɫ�����ܽ⣬��Һ�������ɫ��������2.0��10��6 ��4����HCl��Һ��BaCl2��Һ�����������ܼ������� ��5��GaCl3+NH3  GaN+3HCl GaN+3HCl |
|||
| ��� | 46 |
|
||
���� |
2021���� | |||
| ��� | �ӷ����̿���(��Ҫ�ɷ�ΪV2O5��Cr2O3��MnO)�������һ�ֹ����������£� ��֪��pH�ϴ�ʱ��������[Mn(II)](�ڿ������ױ�����.�ش��������⣺ ��1��CrԪ��λ��Ԫ�����ڱ���_______����_______�塣 ��2����FeCl3��Һ�Ʊ�Fe(OH)3����Ļ�ѧ����ʽΪ_______�� ��3�������£�������̬��۷�������Ũ�ȵĶ���[lgc��(V)]��pH��ϵ��ͼ1����֪�����̿��������Һ��c����V��=0.01mol��L��1�������������̿���pH��3.0�����뽺�干��������۷����ӵĴ�����̬Ϊ_______(�ѧʽ)��  ��4��ij�¶��£�Cr(III)��Mn(II)�ij�������pH��ϵ��ͼ2�����������������pHΪ_______���ڸ���������ҺB��c(Ce3+)��_______mol��L��1��Kw����Ϊ1��10��14��Ce(OH)3��Ksp����Ϊ1��10��30���� ��5����ת��������������MnO2�����ӷ���ʽΪ_______�� ��6�����ᴿ��������Na2S2O3������Ϊ_______�� |
|||
�� |
��1����4��������VIB ��2��FeCl3+3H2O��3(����)+3HCl������ ��3��H3V2O7������ �� ��4����6.0��������1��10��6������ ��5��Mn2++H2O2+2OH��=MnO2+2H2O������ ��6����ֹpH�ϴ�ʱ��������[Mn(II)]������������������ת��ΪMnO2����Cr(OH)3�ı��棬ʹ���ﲻ�� |
|||
| ��� | 47 |
|
||
���� |
2021�����߿� | |||
| ��� | ������������ּ����������Ʊ�����ķ���������Ҫ���̣����ֲ�����ʡ�ԣ����£� ����˵��������� A��FeSO4�ķֽ����XΪFeO B���������漰���ֽⷴӦ C��HNO3�ķе��H2SO4�ĵ� D���Ʊ�ʹ�õ��������� |
|||
�� |
A | |||
| ��� | 48 |
|
||
���� |
2021�����߿� | |||
| ��� | �������������ӹ�����Ҫ�м��Ʒ�����й㷺����;����ҵ�����⾫����Ҫ��MoS2������Cu��Fe�Ļ����PSiO2�ȣ�Ϊԭ���Ʊ�������淋Ĺ�����������ͼ��ʾ�� ��  �ش��������⣺ ��1�������ա����������������������������������պ����ȡ���ʡ� ��2����������ʱ��MoO3ת��ΪMoO42������ߵ�λʱ����������ʵĴ�ʩ������������������д���֣����¶ȶ�90min��������ʵ�Ӱ������ͼ��ʾ���������¶ȳ���80�����Ľ����ʷ������ͣ���Ҫԭ�����¶�����ʹˮ��������������������������������  ��3����������ʱ������Һ�в�����Cu2+��Fe2+ת��Ϊ������ȥ���о�����������Һ��c(S2��)��pH�Ĺ�ϵΪ��lgc(S2��)��pH��15.1��Ϊ��ʹ��Һ�е���������Ũ��С��1.0��10��6mol��L��1��Ӧ������Һ��pH��С��������������֪��pKsp=��lgKsp��CuS��Fe��pKsp�ֱ�Ϊ35.2��17.2�� ��4��������������Һ���еͼ��⣨MoO32����ʾ�����ɼ�������H2O2��������ΪMoO42������Ӧ�����ӷ���ʽΪ������������������������ ��5����������ʱ������NH4NO3��Ŀ�������������������������������� ��6����������H2��ԭ(NH4)2Mo2O13���Ƶý����⣬��Ӧ�Ļ�ѧ����ʽΪ���������������� [��֪��(NH4)2Mo2O13���ȷֽ�����MoO3] |
|||
�� |
��1����ˮ ��2���ʵ����¡����衢����Na2CO3����������Na2CO3Ũ�ȣ��� Na2MoO4����������������� ��3��3.9 ��4��H2O2+MoO42��=MnO42��+H2O ��5���ṩNH4+��ʹMoO42�����ת��Ϊ�������� ��6��(NH4)2Mo2O13��12H2  4Mo+2NH3+13H2O 4Mo+2NH3+13H2O |
|||
| ��� | 49 |
|
||||||
���� |
2021�����߿� | |||||||
| ��� | ��ѧ��ȼ�գ�CLC�������������彫�����е���������ȼ�ϵ��¼������봫ͳȼ�շ�ʽ��ȣ������˿�����ȼ�ϵ�ֱ�ӽӴ��������ڸ�Ч����CO2������CuO/Cu2O������ļ��黯ѧ��ȼ�ռ���ʾϢͼ���¡� ������Ӧ����ȼ�Ϸ�Ӧ���з����ķ�Ӧ�ֱ�Ϊ�� ��2Cu2O(s)+O2(g)��4CuO(s)������H1=��277kJ��mol��1 ��8CuO(s)+CH4(g)��4Cu2O(s)+CO2(g)��2H2O(g) ������H2=��348kJ��mol��1 ��1����ӦCH4(g) +2O2(g)��CO2(g)��2H2O(g)������H=���������� kJ��mol��1 ��2����Ӧ�ڵ�ƽ�ⳣ������ʽK=������������ ��3����������������������1���������� ����">����"=����<����������� ��4����ʢ��CuO/Cu2O������ĸ����ܱ������г������[���������ʵ�������x(O2)Ϊ21%]��������Ӧ�١�ƽ��ʱx(O2)�淴Ӧ�¶�T�仯����������ͼ��ʾ��985��ʱO2��ƽ��ת���ʦ�(O2)������������������2λ��Ч���֣� ��5��������ͼ��x(O2)���¶����߶������ԭ��������������������������Ӧ�¶ȱ��������1030�����£�ԭ������������������������������  ��6����������Ӹ��ԣ��ɼӿ컯ѧ��ȼ�����ʣ�ʹ�ò�ͬ���ӵ�CuO/Cu2O�����壬��Ӧ�ڻ�����±���ʾ��
|
|||||||
�� |
��1����802 ��2��  ��3��> ��4��58% ��5����Ӧ��Ϊ���ȷ�Ӧ���¶�����ƽ�������¶� ����1030��ʱ��x��O2������21%�������������� ��6����������< |
|||||||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |