题干 |
某工厂采用如下工艺处理镍钴矿硫酸浸取液(含Ni2+、Co2+、Fe2+、Fe3+、Mg2+、和Mg2+和)。实现镍、钴、镁元素的回收。
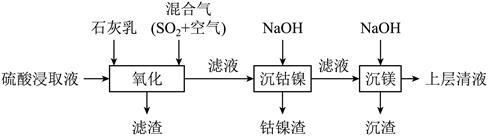
已知:
物质
| Fe(OH)3
| Co(OH)2
| Ni(OH)2
| Mg(OH)2
| Ksp
| 10-37.4
| 10-14.7
| 10-14.7
| 10-10.8
| 回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为_______(答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H2SO5),1mol H2SO5中过氧键的数目为_______。
(3)“氧化”中,用石灰乳调节pH=4,Mn2+被H2SO5氧化为MnO2,该反应的离子方程式为_______( H2SO5的电离第一步完全,第二步微弱);滤渣的成分为MnO2、_______(填化学式)。
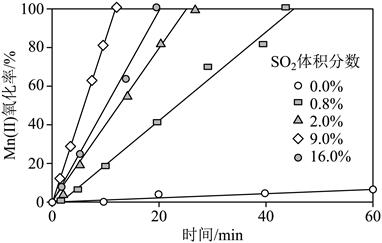
(4)“氧化”中保持空气通入速率不变,Mn (Ⅱ)氧化率与时间的关系如下。SO2体积分数为_______时,Mn (Ⅱ)氧化速率最大;继续增大SO2体积分数时,Mn(Ⅱ)氧化速率减小的原因是_______。
(5)“沉钴镍”中得到的Co (Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为_______。
(6)“沉镁”中为使Mg2+沉淀完全(25℃),需控制pH不低于_______(精确至0.1)。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出