 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 江苏省2023年普通高中学业水平选择性考试 | |
|---|---|
| 本卷共有试题:16 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
||
出处 |
2023江苏 | |||
| 题干 | 我国提出2060年实现碳中和的目标,体现了大国担当。碳中和中的碳是指 A.碳原子 B.二氧化碳 C.碳元素 D.含碳物质a |
|||
答案 |
B | |||
| 题号 | 2 |
|
||
出处 |
2023江苏 | |||
| 题干 | 反应NH4Cl+NaNO2=NaCl+N2↑+2H2O应用于石油开采。下列说法正确的是 A.NH4+的电子式为  B.NO2-中N元素的化合价为+5 B.NO2-中N元素的化合价为+5C.N2分子中存在N≡N D.H2O为非极性分子 |
|||
答案 |
C | |||
| 题号 | 3 |
|
||
出处 |
2023江苏 | |||
| 题干 | 实验室制取Cl2的实验原理及装置均正确的是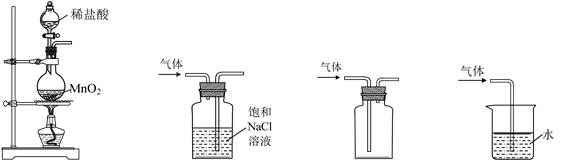 A.制取Cl2 B.除去Cl2中的HCl C.收集Cl2 D.吸收尾气中的Cl2 |
|||
答案 |
C | |||
| 题号 | 4 |
|
||
出处 |
2023江苏 | |||
| 题干 | 元素C、Si、Ge位于周期表中ⅣA族。下列说法正确的是 A.原子半径:r(C)>r(Si)>r(Ge) B.第一电离能:I1(C)<I1(Si)<I1(Ge) C.碳单质、晶体硅、SiC均为共价晶体 D.可在周期表中元素Si附近寻找新半导体 |
|||
答案 |
D | |||
| 题号 | 5 |
|
||
出处 |
2023江苏 | |||
| 题干 | 材料阅读下列材料,完成5~7题: 氢元素及其化合物在自然界广泛存在且具有重要应用。11H、21H、31H是氢元素的3种核素,基态H原子1s1的核外电子排布,使得H既可以形成H+又可以形成H-,还能形成H2O、H2O2、NH3、 N2H4、CaH2等重要化合物;水煤气法、电解水、光催化分解水都能获得H2,如水煤气法制氢反应中,H2O(g)与足量C(s)反应生成1 mol H2(g)和1 mol CO(g)吸收131.3 kJ的热量。H2在金属冶炼、新能源开发、碳中和等方面具有重要应用,如HCO 3-在催化作用下与H2反应可得到HCOO-。我国科学家在氢气的制备和应用方面都取得了重大成果。 5.下列说法正确的是 A.11H、21H、31H都属于氢元素 B.NH 4+和H2O的中心原子杂化轨道类型均为sp2 C.H2O2分子中的化学键均为极性共价键 D.CaH2晶体中存在Ca与H2之间的强烈相互作用 6.下列化学反应表示正确的是 A.水煤气法制氢:C(s)+H2O(g)=H2(g)+CO(g) ΔH=-131.3 kJ・mol-1 B.HCO 3催化加氢生成HCOO的反应:HCO3+H2  HCOO+H2O HCOO+H2OC.电解水制氢的阳极反应:2H2O-2e-=H2↑+2OH- D.CaH2与水反应:CaH2+2H2O=Ca(OH)2+H2↑ |
|||
答案 |
5.A 6.B | |||
| 题号 | 6 |
|
||
出处 |
2023江苏 | |||
| 题干 | 下列物质结构与性质或物质性质与用途具有对应关系的是 A.H2具有还原性,可作为氢氧燃料电池的燃料 B.氨极易溶于水,液氨可用作制冷剂 C.H2O分子之间形成氢键,H2O(g)的热稳定性比H2S(g)的高 D.N2H4中的N原子与H+形成配位键,N2H4具有还原性 |
|||
答案 |
A | |||
| 题号 | 7 |
|
||
出处 |
2023江苏 | |||
| 题干 | 氮及其化合物的转化具有重要应用。下列说法不正确的是 A.实验室探究稀硝酸与铜反应的气态产物: 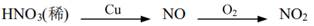 B.工业制硝酸过程中的物质转化: 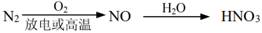 C.汽车尾气催化转化器中发生的主要反应:2NO+2CO  N2+2CO2 N2+2CO2D.实验室制备少量NH3的原理:2NH4Cl+Ca(OH)2  CaCl2+2NH3↑+2H2O CaCl2+2NH3↑+2H2O |
|||
答案 |
B | |||
| 题号 | 8 |
|
||
出处 |
2023江苏 | |||
| 题干 | 化合物Z是合成药物非奈利酮的重要中间体,其合成路线如下: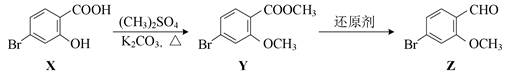 下列说法正确的是 A.X不能与FeCl3溶液发生显色反应 B.Y中的含氧官能团分别是酯基、羧基 C.1 mol Z最多能与3 mol H2发生加成反应 D.X、Y、Z可用饱和NaHCO3溶液和2%银氨溶液进行鉴别 |
|||
答案 |
D | |||
| 题号 | 9 |
|
||
出处 |
2023江苏 | |||
| 题干 | 金属硫化物(MxSy)催化反应CH4(g)+2H2S(g)=CS2(g)+4H2 (g),既可以去除天然气中的H2S,又可以获得H2。下列说法正确的是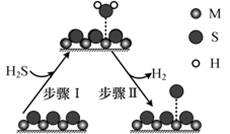 A.该反应ΔS<0 B.该反应的平衡常数 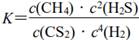 C.题10图所示的反应机理中,步骤Ⅰ可理解为H2S中带部分负电荷的S与催化剂中的M之间发生作用 D.该反应中每消耗1mol H2S,转移电子的数目约为2×6.02×1023 |
|||
答案 |
C | |||
| 题号 | 10 |
|
|||||||||||||||
出处 |
2023江苏 | ||||||||||||||||
| 题干 | 室温下,探究0.1 mol・L-1FeSO4溶液的性质,下列实验方案能达到探究目的的是
|
||||||||||||||||
答案 |
B | ||||||||||||||||
| 题号 | 11 |
|
||
出处 |
2023江苏 | |||
| 题干 | 室温下,用含少量Mg2+ 的MnSO4溶液制备MnCO3 的过程如题12图所示。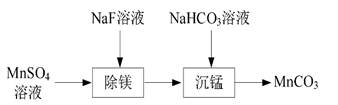 已知Ksp(MgF2)=5.2×10―11,Ka(HF)=6.3×10―4。下列说法正确的是 A.0.1 mol・L−1NaF溶液中:c(F―)=c(Na+)+c(H+) B.“除镁”得到的上层清液中: 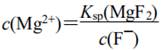 C.0.1 mol・L−1NaHCO3溶液中:c(CO23-)=c(H+)+c(H2CO3)-c(OH―) D.“沉锰”后的滤液中:c(Na+)+c(H+)=c(OH―)+c(HCO3-)+2c(CO23-) |
|||
答案 |
C | |||
| 题号 | 12 |
|
||
出处 |
2023江苏 | |||
| 题干 | 二氧化碳加氢制甲烷过程中的主要反应为 CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH=-164.7 kJ・mol-1 CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=41.2 kJ・mol-1 在密闭容器中,1.01×105 Pa、n起始(CO2)∶n起始(H2)=1∶4时,CO2平衡转化率、在催化剂作用 下反应相同时间所测得的CO2实际转化率随温度的变化如题13图所示。CH4的选择性可表示 为 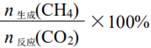 。下列说法正确的是 。下列说法正确的是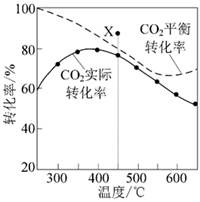 A.反应2CO (g)+2H2(g)=CO2(g)+CH4(g)的焓变ΔH=-205.9 kJ・mol-1 B.CH4的平衡选择性随着温度的升高而增加 C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃ D.450℃时,提高 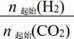 的值或增大压强,均能使CO2平衡转化率达到X点的值 的值或增大压强,均能使CO2平衡转化率达到X点的值 |
|||
答案 |
D | |||
| 题号 | 13 |
|
||
出处 |
2023江苏 | |||
| 题干 | V2O5-WO3/TiO2催化剂能催化NH3脱除烟气中的NO,反应为 4NH3(g)+O2(g)+4NO(g)=4N2(g)+6H2O(g) ΔH=-1632.4 kJ・mol-1 (1)催化剂的制备。将预先制备的一定量的WO3/TiO2粉末置于80℃的水中,在搅拌下加入一定量的NH4VO3溶液,经蒸发、焙烧等工序得到颗粒状V2O5-WO3/TiO2催化剂。在水溶液中VO3-水解为H3VO4沉淀的离子方程式为 ;反应选用NH4VO3溶液而不选用NaVO3溶液的原因是 。 (2)催化剂的应用。将一定物质的量浓度的NO、O2、NH3(其余为N2)气体匀速通过装有V2O5-WO3/TiO2催化剂的反应器,测得NO的转化率随温度的变化如题14图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是 ;反应温度高于380℃,NO转化率下降,除因为进入反应器的NO被还原的量减少外,还有 (用化学方程式表示)。 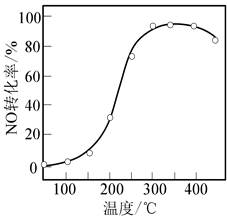 (3)废催化剂的回收。回收V2O5-WO3/TiO2催化剂并制备NH4VO3的过程可表示为 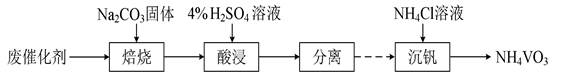 ①酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有 。 ②通过萃取可分离钒和钨,在得到的钒酸中含有H4V4O12。已知H4V4O12具有八元环结构,其结构式可表示为 。 ③向pH=8的NaVO3溶液中加入过量的NH4Cl溶液,生成NH4VO3沉淀。已知 Ksp(NH4VO3)=1.7×10―3,加过量NH4Cl的目的是 。 |
|||
答案 |
(1)VO3-+2H2O=H3VO4↓+OH- 或VO3-+NH+4+H2O=80℃H3VO4↓+NH3制得的催化剂中不含Na+ (2)在该温度范围内,催化剂的活性变化不大,消耗NO的反应速率与生成NO的反应速率随温度升高而增大,对NO转化率的影响相互抵消 催化剂 4NH3+5O2=高于380℃4NO+6H2O (3)①提高反应温度,延长浸出时间 ② 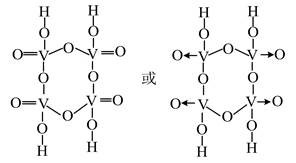 ③促进NH4VO3充分沉淀 |
|||
| 题号 | 14 |
|
||
出处 |
2023江苏 | |||
| 题干 | 化合物I是鞘氨醇激酶抑制剂,其合成路线如下: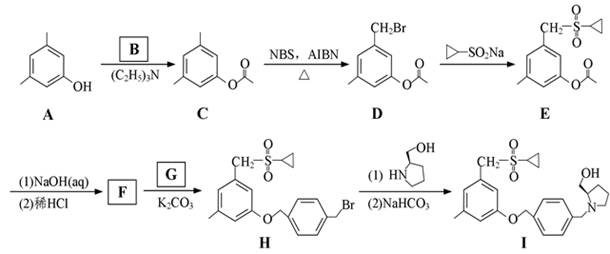 (1)化合物A的酸性比环己醇的 (填“强”或“弱”或“无差别”)。 (2)B的分子式为C2H3OCl,可由乙酸与SOCl2反应合成,B的结构简式为 。 (3)A→C中加入(C2H5)3N是为了结合反应中产生的 (填化学式)。(4)写出同时满足下列条件的C的一种同分异构体的结构简式: 。 碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%的酸性KMnO4溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机 产物的核磁共振氢谱中只有1个峰。 (5)G的分子式为C8H8Br2,F→H的反应类型为 。 (6)写出以  、 、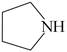 和CH2=CH2为原料制备 和CH2=CH2为原料制备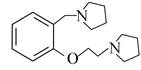 的合成路线流程图(须用NBS和AIBN无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。 的合成路线流程图(须用NBS和AIBN无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。 |
|||
答案 |
(1)强 (2)CH3COCl (3)HCl (4) 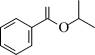 (5)取代反应 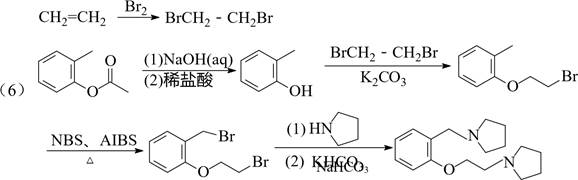 |
|||
| 题号 | 15 |
|
||
出处 |
2023江苏 | |||
| 题干 | 实验室模拟“镁法工业烟气脱硫”并制备MgSO4・H2O,其实验过程可表示为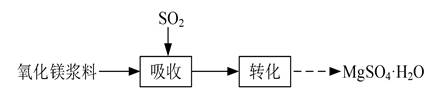 (1)在搅拌下向氧化镁浆料中匀速缓慢通入SO2气体,生成MgSO3,反应为 Mg(OH)2+H2SO3=MgSO3+2H2O其平衡常数K与Ksp[Mg(OH)2]、Ksp(MgSO3)、Ka1(H2SO3)、Ka2(H2SO3)的代数关系式为 K= ;下列实验操作一定能提高氧化镁浆料吸收SO2效率的有 (填序号)。 A.水浴加热氧化镁浆料 B.加快搅拌速率 C.降低通入SO2气体的速率 D.通过多孔球泡向氧化镁浆料中通SO2 (2)在催化剂作用下MgSO3被O2氧化为MgSO4。已知MgSO3的溶解度为0.57 g(20℃),O2氧化溶液中SO32-的离子方程式为 ;在其他条件相同时,以负载钴的分子筛为催化剂, 浆料中MgSO3被O2氧化的速率随pH的变化如题16图-1所示。在pH=6~8范围内,pH增大,浆料中MgSO3的氧化速率增大,其主要原因是 。 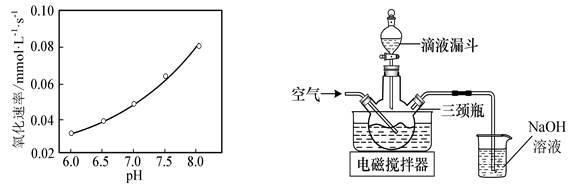 (3)制取MgSO4・H2O晶体。在如题16图-2所示的实验装置中,搅拌下,使一定量的MgSO3 浆料与H2SO4溶液充分反应。MgSO3浆料与H2SO4溶液的加料方式是 ;补充完整制取MgSO4・H2O晶体的实验方案:向含有少量Fe3+、Al3+的MgSO4溶液中 。[已知:Fe3+、Al3+在pH≥5时完全转化为氢氧化物沉淀;室温下从MgSO4饱和溶液中结晶出MgSO4・7H2O,MgSO4・7H2O在150~170℃下干燥得到MgSO4・H2O,实验中需要使用MgO粉末。] |
|||
答案 |
(1)①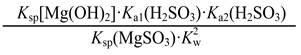 ②BD (2)①2SO23-+O2=催化剂2SO24- ②pH增大,c(SO23-)增大,氧化速率加快 (3)①用滴液漏斗向盛有MgSO3浆料的三颈烧瓶中缓慢滴加H2SO4溶液 ②分批加入少量MgO粉末,搅拌,至用pH试纸测得溶液的pH大于5,过滤;将滤液蒸发浓缩、降温至室温结晶,过滤,所得滤渣在150~170℃下干燥 |
|||
| 题号 | 16 |
|
||
出处 |
2023江苏 | |||
| 题干 | 空气中CO2含量的控制和CO2资源利用具有重要意义。(1)燃煤烟气中CO2的捕集可通过如下所示的物质转化实现。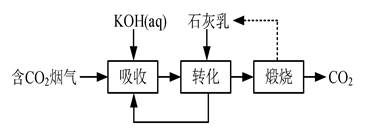 “吸收”后所得的KHCO3溶液与石灰乳反应的化学方程式为 ;载人航天器内,常 用LiOH固体而很少用KOH固体吸收空气中的CO2,其原因是 。 (2)合成尿素[CO(NH2)2]是利用CO2的途径之一。尿素 合成主要通过下列反应实现 反应Ⅰ:2NH3(g)+CO2(g)=NH2COONH4(l) 反应Ⅱ:NH2COONH4(l)=CO(NH2)2(l)+H2O(l) ①密闭体系中反应Ⅰ的平衡常数(K)与温度的关系如题17图-1所示,反应Ⅰ的ΔH (填“=0”或“>0”或“<0”)。 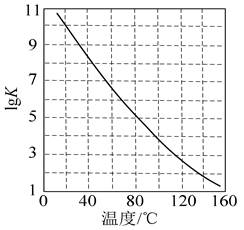 ②反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲[(NH2CO)2NH]和尿素转化为氰酸铵(NH4OCN)等副反应。尿素生产中实际投入NH3和CO2的物质的量之比为n(NH3)∶n(CO2)=4∶1,其实际投料比值远大于理论值的原因是 。 (3)催化电解吸收CO2的KOH溶液可将CO2转化为有机物。相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如题17图-2所示。 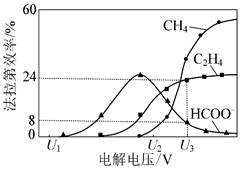 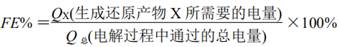 其中,QX=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。 ①当电解电压为U1时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为 (填化学式)。 ②当电解电压为U2时,阴极由HCO 3-生成CH4的电极反应式为 。 ③当电解电压为U3时,电解生成的C2H4和HCOO−的物质的量之比为 (写出计算 过程)。 |
|||
答案 |
(1)KHCO3+Ca(OH)2=CaCO3↓+H2O+KOH 相同质量的LiOH吸收CO2的量比KOH的多 (2)①<0 ②提高CO2的转化率,抑制尿素水解,抑制尿素缩合生成缩二脲 (3)①H2 ②10HCO3-+8e- =CH4↑+9CO23-+3H2O ③生成1 mol C2H4转移12 mol电子;生成1 mol HCOO-转移2 mol电子 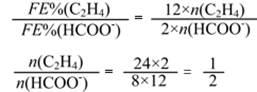 |
|||
| v福建省实践教学工作室 蔡实践 设计制作 v |