题干 |
空气中CO2含量的控制和CO2资源利用具有重要意义。(1)燃煤烟气中CO2的捕集可通过如下所示的物质转化实现。
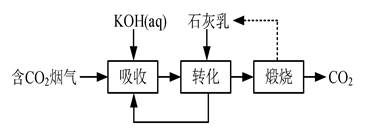
“吸收”后所得的KHCO3溶液与石灰乳反应的化学方程式为 ;载人航天器内,常
用LiOH固体而很少用KOH固体吸收空气中的CO2,其原因是 。
(2)合成尿素[CO(NH2)2]是利用CO2的途径之一。尿素
合成主要通过下列反应实现
反应Ⅰ:2NH3(g)+CO2(g)=NH2COONH4(l)
反应Ⅱ:NH2COONH4(l)=CO(NH2)2(l)+H2O(l)
①密闭体系中反应Ⅰ的平衡常数(K)与温度的关系如题17图-1所示,反应Ⅰ的ΔH (填“=0”或“>0”或“<0”)。
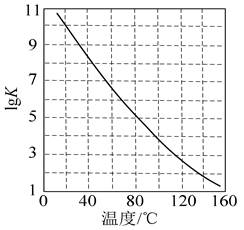
②反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲[(NH2CO)2NH]和尿素转化为氰酸铵(NH4OCN)等副反应。尿素生产中实际投入NH3和CO2的物质的量之比为n(NH3)∶n(CO2)=4∶1,其实际投料比值远大于理论值的原因是 。
(3)催化电解吸收CO2的KOH溶液可将CO2转化为有机物。相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如题17图-2所示。
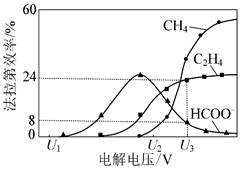
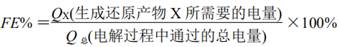
其中,QX=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
①当电解电压为U1时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为 (填化学式)。
②当电解电压为U2时,阴极由HCO 3-生成CH4的电极反应式为 。
③当电解电压为U3时,电解生成的C2H4和HCOO−的物质的量之比为 (写出计算
过程)。 |
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出