 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| 2017����ͨ�ߵ�ѧУ����ȫ��ͳһ���ԣ����վ�����ѧ | |
|---|---|
| �����������⣺22 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2017���ո߿� | |||
| ��� | 2017������������ҹ�������Ϊ����Լ��Լ������Դ,������ɫ��Լ�������������Ӧ�ᳫ���� ��A�������趨�յ��¶Ⱦ����ܵĵ͡���������B���ƹ�ʹ��һ�������ϴ���ֽ�� ��C���ٿ�˽�ҳ���˹�����ͨ���ߡ���������D������Ʒ���к�����װ�ٽ����� |
|||
�� |
C���������� | |||
| ��� | 2 |
|
||
���� |
2017���ո߿� | |||
| ��� | �����йػ�ѧ�����ʾ��ȷ���� ��A��������Ϊ31����ԭ��: 3115P ������������B����ԭ�ӵĽṹʾ��ͼ: 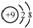 ��C��CaCl2�ĵ���ʽ: 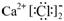 ������������D�������Ļ�ѧʽ: Al2(SO4)3 ������������D�������Ļ�ѧʽ: Al2(SO4)3 |
|||
�� |
A | |||
| ��� | 3 |
|
||
���� |
2017���ո߿� | |||
| ��� | �����й�������������;���ж�Ӧ��ϵ���� ��A��Na2O2����CO2����O2��������������߹����������� ��B��ClO2���л�ԭ�ԣ�����������ˮ��ɱ������ ��C��SiO2Ӳ�ȴ�����������ά ��D��NH3������ˮ������������� |
|||
�� |
A | |||
| ��� | 4 |
|
||
���� |
2017���ո߿� | |||
| ��� | ������ȡSO2����֤��Ư���ԡ��ռ�������β��������װ�ú�ԭ���ܴﵽʵ��Ŀ�ĵ��� 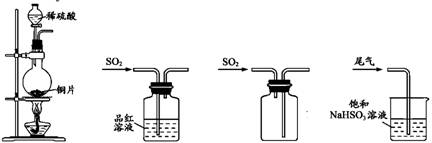 ��A����ȡSO2 ���������� B����֤Ư���ԡ�����C���ռ�SO2 ��������D��β������ |
|||
�� |
B | |||
| ��� | 5 |
|
||
���� |
2017���ո߿� | |||
| ��� | ����������Ԫ��X��Y��Z��Wԭ������������������ֻ��Y��Z����ͬһ���������ڣ�Z�ǵؿ��к�������Ԫ�أ�W�Ƕ������н�������ǿ��Ԫ�ء�����˵����ȷ���� ��A��ԭ�Ӱ뾶: r(X) < r(Y) < r(Z) < r(W) ���������� ��B��W������������ˮ������һ������ ��C��Y�ĵ��ʵ������Ա�Z��ǿ���������������������� ��D��X��Y��Z����Ԫ�ؿ�����ɹ��ۻ���������ӻ����� |
|||
�� |
D | |||
| ��� | 6 |
|
||
���� |
2017���ո߿� | |||
| ��� | ����ָ����Ӧ�����ӷ���ʽ��ȷ���� ��A������ˮ��Ӧ: Na +2H2O��Na++2OH�C + H2�� ��B����ⱥ��ʳ��ˮ��ȡ�ռ������: 2Cl�C+2H2O  H2��+ Cl2��+2OH�C H2��+ Cl2��+2OH�C ��C��������������Һ�м���ϡ����: Ba2++OH�C + H+ +SO42����BaSO4��+H2O ��D����̼�������Һ�м�������ʯ��ˮ: Ca2++HCO3��+OH�C��CaCO3��+H2O |
|||
�� |
B | |||
| ��� | 7 |
|
||
���� |
2017���ո߿� | |||
| ��� | �ڸ��������£�����ѡ����ʾ�����ʼ�ת������ʵ�ֵ��� ��  |
|||
�� |
C | |||
| ��� | 8 |
|
||
���� |
2017���ո߿� | |||
| ��� | ͨ�����·�Ӧ�ɻ��������Դ������(CH3OCH3 )������˵������ȷ���� ��C(s) + H2O(g)��CO(g) + H2 (g) �������� ��H1 = a kJ��mol��1 ��CO(g) + H2O(g)��CO2 (g) + H2 (g) ������ ��H 2 = b kJ��mol��1 ��CO2 (g) + 3H2 (g)����CH3OH(g) + H2O(g) �������� ��H 3 = c kJ��mol��1 ��2CH3OH(g)��CH3OCH3 (g) + H2O(g)���� ��H 4 = d kJ��mol��1 ��A����Ӧ�١���Ϊ��Ӧ���ṩԭ���� ��B����Ӧ��Ҳ��CO2��Դ�����õķ���֮һ ��C����ӦCH3OH(g)��CH3OCH3 (g) + 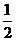 H2O(l)�Ħ�H = H2O(l)�Ħ�H =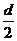 kJ��mol��1 kJ��mol��1��D����Ӧ2CO(g) + 4H2 (g)��CH3OCH3 (g) + H2O(g)�Ħ�H = ( 2b + 2c + d ) kJ��mol��1 |
|||
�� |
C | |||
| ��� | 9 |
|
||
���� |
2017���ո߿� | |||
| ��� | �����£����и���������ָ����Һ���ܴ���������� ��A����ɫ������Һ�У�Fe3+��Mg2+��SCN����Cl�� ��B��c(H+)/ c(OH��) = 1��10��12����Һ�У�K+��Na +��CO32����NO3�� ��C��c(Fe2+ ) =1 mol��L��1����Һ�У�K+�� NH4+��MnO4����SO42�� ��D����ʹ���ȱ�����Һ�У�Na+�� NH4+��SO42����HCO3�� |
|||
�� |
B | |||
| ��� | 10 |
|
||
���� |
2017���ո߿� | |||
| ��� | H2O2�ֽ������ܶ�������Ӱ�졣ʵ���� 70��ʱ��ͬ������H2O2Ũ����ʱ��ı仯��ͼ��ʾ������˵����ȷ����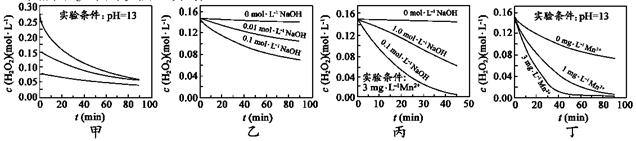 ��A��ͼ�ױ���������������ͬʱ��H2O2Ũ��ԽС����ֽ�����Խ�� ��B��ͼ�ұ���������������ͬʱ����ҺpHԽС��H2O2�ֽ�����Խ�� ��C��ͼ������������Mn2+����ʱ����Һ����Խǿ��H2O2�ֽ�����Խ�� ��D��ͼ����ͼ��������������Һ�У�Mn2+��H2O2�ֽ����ʵ�Ӱ��� |
|||
�� |
D | |||
| ��� | 11 |
|
||
���� |
2017���ո߿� | |||
| ��� | �������㷺�����ڶ�ֲ�����ڣ�����������������˵����ȷ����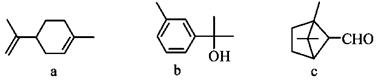 ��A��a��b�����ڷ����廯���� ��B��a��c����������̼ԭ�Ӿ�����ͬһƽ���� ��C��a��b��c����ʹ����KMnO4��Һ��ɫ ��D��b��c���������Ƶ�Cu(OH)2��Ӧ���ɺ�ɫ���� |
|||
�� |
C�� | |||
| ��� | 12 |
|
||
���� |
2017���ո߿� | |||
| ��� | ����˵����ȷ���� ��A����ӦN2(g) +3H2(g)  2NH3(g)�Ħ�H < 0����S >0 2NH3(g)�Ħ�H < 0����S >0 ��B�����¸����ܵ��õ�������п����Լ����ܵ��ĸ�ʴ ��C�������£�Ksp[Mg(OH)2]=5.6��10��12��pH=10�ĺ�Mg2+��Һ�У�c(Mg2+ )��5.6��10��4mol��L��1 ��D�����³�ѹ�£�п��ϡH2SO4��Ӧ���� 11.2 LH2����Ӧ��ת�Ƶĵ�����Ϊ6.02��1023 |
|||
�� |
BC | |||
| ��� | 13 |
|
|||||||||||||||
���� |
2021�Ͼ���Уһ�� | ||||||||||||||||
| ��� | ��������ʵ��������������õ��Ľ�����ȷ����
|
||||||||||||||||
�� |
B�� | ||||||||||||||||
| ��� | 14 |
|
||
���� |
2017���ո߿� | |||
| ��� | �����£�Ka (HCOOH)=1.77��10��4��Ka (CH3COOH)=1.75��10��5��Kb (NH3��H2O) =1.76��10��5������˵����ȷ���� ��A��Ũ�Ⱦ�Ϊ0.1 mol��L��1��HCOONa��NH4Cl��Һ�������ӵ����ʵ���Ũ��֮��:ǰ�ߴ��ں��� ��B������ͬŨ�ȵ�NaOH��Һ�ֱ�ζ������pH��Ϊ3��HCOOH��CH3COOH��Һ���յ㣬����NaOH��Һ�������� ��C��0.2 mol��L��1HCOOH��0.1 mol��L��1NaOH�������Ϻ����Һ��: c(HCOO��) + c(OH��) = c(HCOOH) + c(H+) ��D��0.2 mol��L��1CH3COONa��0.1 mol��L��1����������Ϻ����Һ��(pH<7): c(CH3COO��) > c(Cl��) > c(CH3COOH) > c(H+) |
|||
�� |
AD | |||
| ��� | 15 |
|
||
���� |
2017���ո߿� | |||
| ��� | �¶�ΪT1ʱ���������ݻ���Ϊ 1 L�ĺ����ܱ������н�������Ӧ: 2NO2(g) 2NO(g)+O2 (g) (����Ӧ����)��ʵ����: v��= v (NO2 )����= k��c2(NO2 )��v��= v(NO)����= 2v (O2 )����= k��c2(NO)��c(O2 )��k����k��Ϊ���ʳ��������¶�Ӱ�졣 2NO(g)+O2 (g) (����Ӧ����)��ʵ����: v��= v (NO2 )����= k��c2(NO2 )��v��= v(NO)����= 2v (O2 )����= k��c2(NO)��c(O2 )��k����k��Ϊ���ʳ��������¶�Ӱ�졣 ����˵����ȷ���� 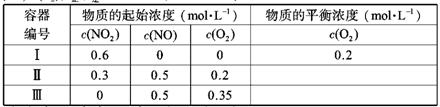 ��A����ƽ��ʱ�����������������е���ѹǿ֮��Ϊ4��5 ��B����ƽ��ʱ���������� c(O2)/c(NO2)���������еĴ� ��C����ƽ��ʱ����������NO���������С��50% ��D�����¶ȸı�Ϊ T2ʱ���� k��=k������ T2> T1 |
|||
�� |
CD | |||
| ��� | 16 |
|
||
���� |
2017���ո߿� | |||
| ��� | ����Ӧ�ù㷺�Ľ�������������(��Ҫ�ɷ�ΪAl2O3����SiO2��Fe2O3������)Ϊԭ���Ʊ�����һ�ֹ�����������: 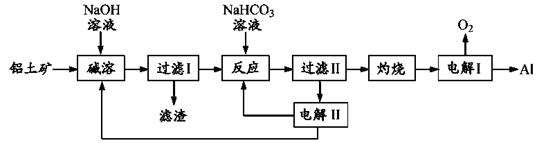 ע:SiO2�ڡ����ܡ�ʱת��Ϊ�������Ƴ����� ��1�������ܡ�ʱ����ƫ�����Ƶ����ӷ���ʽΪ_____________________�� ��2�����ˢ�������Һ�м���NaHCO3��Һ����Һ��pH_________ (����������䡱��С��)�� ��3���������ǵ������Al2O3������������������ʯī�����ģ�ԭ����___________�� ��4���������ǵ��Na2CO3��Һ��ԭ����ͼ��ʾ�� 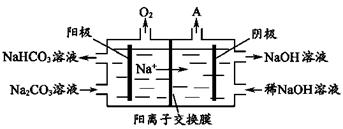 �����ĵ缫��ӦʽΪ_____________________����������������A�Ļ�ѧʽΪ____________�� ��5�������� 1000��ʱ����N2��Ӧ�Ʊ�AlN������������������NH4Cl���岢��ֻ�ϣ�������AlN���Ʊ�������Ҫԭ����_____________________�� |
|||
�� |
(1)Al2O3+ 2OH����2AlO2����+ H2O (2)��С (3)ʯī�缫�������ϲ�����O2���� (4)4CO32�� + 2H2O��4e-��4 HCO3��+O2���������� H2 (5)NH4Cl�ֽ������HCl�ܹ��ƻ�Al�����Al2O3��Ĥ |
|||
| ��� | 17 |
|
||
���� |
2017���ո߿� | |||
| ��� | ������H��һ�����ںϳɦ�-���ڵ��ڼ���ҩ���м��壬��ϳ�·������ͼ����: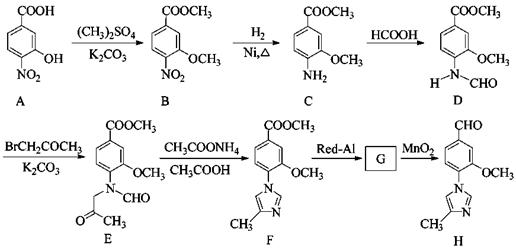 ��1��C�еĺ�������������Ϊ_________��__________�� ��2��D��E�ķ�Ӧ����Ϊ__________________________�� ��3��д��ͬʱ��������������C��һ��ͬ���칹��Ľṹ��ʽ:_____________________�� �ٺ��б������ҷ�������һ������̼ԭ�ӣ� ���ܷ���ˮ�ⷴӦ��ˮ�����֮һ�Ǧ�-�����ᣬ��һˮ����������ֻ��2�ֲ�ͬ��ѧ�������⡣ ��4��G�ķ���ʽΪC12H14N2O2���������õ�H��д��G�Ľṹ��ʽ:__________________�� ��5����֪: 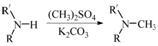 (R����������R|����������H)��д���� (R����������R|����������H)��д����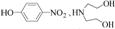 ��(CH3)2SO4Ϊԭ���Ʊ� ��(CH3)2SO4Ϊԭ���Ʊ�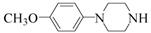 �ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)�� �ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)�� |
|||
�� |
(1)�Ѽ����������������������� (2)ȡ����Ӧ (3) 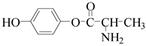 �� ��(4) 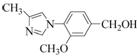 ��5�� 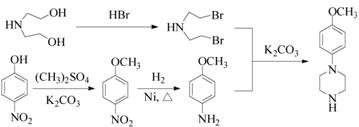 |
|||
| ��� | 18 |
|
||
���� |
2017���ո߿� | |||
| ��� | ��ʽ�Ȼ�ͭ����Ҫ����ɱ������ ��1����ʽ�Ȼ�ͭ�ж����Ʊ����� �ٷ���1: 45 ~ 50��ʱ����CuCl����Һ�г���ͨ������õ�Cu2(OH)2Cl2��3H2O���÷�Ӧ�Ļ�ѧ����ʽΪ_________________________�� �ڷ���2:���Ƶ�CuCl2������ʯ���鷴Ӧ���ɼ�ʽ�Ȼ�ͭ��Cu��ϡ�����ڳ���ͨ������������·�Ӧ����CuCl2��Fe3+�Ը÷�Ӧ�д�����,���ԭ����ͼ��ʾ��M|�Ļ�ѧʽΪ______��  ��2����ʽ�Ȼ�ͭ�ж������,�ɱ�ʾΪCua(OH)bClc��xH2O��Ϊ�ⶨij��ʽ�Ȼ�ͭ�����,��������ʵ��: �ٳ�ȡ��Ʒ 1.1160 g��������ϡHNO3�ܽ�����100.00 mL��ҺA�� ��ȡ25. 00 mL��ҺA����������AgNO3��Һ����AgCl 0.1722 g�� ����ȡ25. 00 mL��ҺA������pH 4 ~ 5����Ũ��Ϊ0.08000 mol��L-1��EDTA(Na2H2Y��2H2O)����Һ�ζ�Cu2+ (���ӷ���ʽΪCu2++ H2Y2-��CuY2-+2H+)���ζ����յ㣬���ı���Һ30.00 mL��ͨ������ȷ������Ʒ�Ļ�ѧʽ(д���������)�� |
|||
�� |
��1����4CuCl + O2+ 8H2O 2Cu2(OH)2Cl2��3H2O��������Fe2+ 2Cu2(OH)2Cl2��3H2O��������Fe2+ ��2��n(Cl��)=n(AgCl)�� 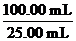 = =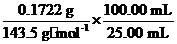 =4.800��10��3mol�� =4.800��10��3mol��n(Cu2+)=n(EDTA)�� 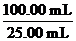 =0.08000 mol��L��1��30.00 mL��10�� 3L��mL��1�� =0.08000 mol��L��1��30.00 mL��10�� 3L��mL��1��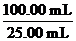 =9.600��10��3mol n(OH��)=2n(Cu2+)-n(Cl��)=2��9.600��10��3mol��4.800��10��3mol=1.440��10��2mol m(Cl��)=4.800��10��3mol�� 35.5 g�� mol��1= 0.1704 g m(Cu2+)=9.600��10��3mol�� 64 g�� mol��1�� = 0.6144 g m(OH��)=1.440��10��2mol�� 17 g�� mol��1= 0.2448 g�� n(H2O)= 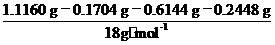 =4.800��10��3mol =4.800��10��3mol a��b��c��x= n(Cu2+)��n(OH��)��n(Cl��)��n(H2O)=2��3��1��1 ��ѧʽΪCu2 (OH)3Cl��H2O |
|||
| ��� | 19 |
|
||
���� |
2017���ո߿� | |||
| ��� | ij����С��������·�������һ�ֹ��̽������е�����Ag(������������������������,��ʵ���Ӱ��ɺ���)��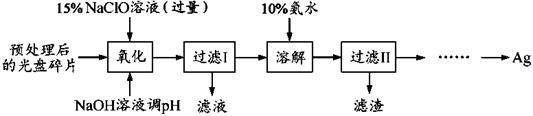 ��֪:��NaClO��Һ�����Ȼ������������ֽ�,��: 3NaClO=2NaCl+NaClO3 ��AgCl�����ڰ�ˮ:AgCl+2NH3��H2O  Ag(NH3)2++ Cl��+2H2O Ag(NH3)2++ Cl��+2H2O �۳���ʱN2H4��H2O(ˮ����)�ڼ����������ܻ�ԭAg(NH3)2+ : ���� ������4 Ag(NH3) 2++N2H4��H2O��4Ag��+ N2��+ 4NH4�� 4NH3��+H2O ��1���������������� 80�������½��У����˵ļ��ȷ�ʽΪ__________________�� ��2��NaClO��Һ��Ag��Ӧ�IJ���ΪAgCl��NaOH��O2���÷�Ӧ�Ļ�ѧ����ʽΪ________________��HNO3Ҳ������Ag���ӷ�Ӧ����ĽǶȷ�������HNO3����NaClO��ȱ����_____________________________�� ��3��Ϊ���Ag�Ļ����ʣ���ԡ����ˢ���������ϴ�ӣ���_______________________�� ��4����ʡ�ԡ����ˢ�ֱ������ȴ��ķ�Ӧ�����еμ�10%��ˮ������Ҫ���Ӱ�ˮ���������������NaClO��NH3��H2O��Ӧ��(��������NaClO3��NH3��H2O����Ӧ)������Ϊ_________________________�� ��5������ƴӡ����ˢ����Һ�л�ȡ����Ag��ʵ�鷽��:________________________(ʵ������ʹ�õ��Լ���: 2 mol��L��1ˮ������Һ��1 mol��L��1H2SO4 )�� |
|||
�� |
(1)ˮԡ���� (2)4Ag+4NaClO+2H2O��4AgCl+4NaOH+O2�� ���ͷų���������(��NO��NO2 )����ɻ�����Ⱦ (3)��ϴ�Ӻ����Һ�ϲ�����ˢ����Һ�� (4)δ���˵�����Һ��ϡ�ͼ���İ�ˮ�������к���һ��Ũ�ȵ�Cl����������AgCl�백ˮ��Ӧ (5)����Һ�еμ�2mol��L-1ˮ������Һ������ʹ���ַ�Ӧ,ͬʱ��1 mol��L��1H2SO4��Һ���շ�Ӧ�зų���NH3������Һ�������ݲ�����ֹͣ�μӣ����ã����ˡ�ϴ�ӣ���� |
|||
| ��� | 20 |
|
||
���� |
2017���ո߿� | |||
| ��� | ��(As)��һЩ�����Ϳ�ɽ��ˮ�е���ȾԪ��,ʹ����������ȥ��ˮ�������Ч��ʩ֮һ�� ��1���������̡�������������������Һ��һ���������,����ʹ���ַ�Ӧ���ɻ��һ����ĸ�Ч������X��������X�к���CO32������ԭ����___________________________________�� ��2��H3AsO3��H3AsO4ˮ��Һ�к���ĸ����ֵķֲ�����(ƽ��ʱij���ֵ�Ũ��ռ������Ũ��֮�͵ķ���)��pH�Ĺ�ϵ�ֱ�����20ͼ- 1����20ͼ- 2��ʾ�� 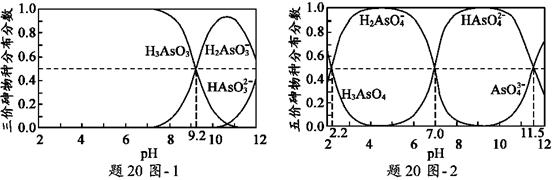 ���Է�̪Ϊָʾ��(��ɫ��ΧpH 8.0 ~ 10.0)����NaOH��Һ��μ��뵽H3AsO3��Һ�У�����Һ����ɫ��Ϊdz��ɫʱֹͣ�μӡ��ù�������Ҫ��Ӧ�����ӷ���ʽΪ_____________________�� ��H3AsO4��һ�����뷽��ʽH3AsO4  H2AsO4��+H+�ĵ��볣��ΪKa1����pKa1=_____________(pKa1 = -lg Ka1 )�� H2AsO4��+H+�ĵ��볣��ΪKa1����pKa1=_____________(pKa1 = -lg Ka1 )����3����Һ��pH��������X�������������Ӱ�졣pH =7.1ʱ��������X���治����ɣ�pH > 7.1ʱ������ɣ�pHԽ�ߣ��������������Խ�ࣻpH<7.1ʱ������ɣ�pHԽ�ͣ��������������Խ�ࡣpH��ͬʱ������X���������������ƽ��������(������ƽ��ʱ��λ����������X�����������)����20ͼ-3��ʾ�� 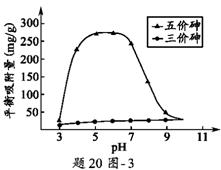 ����pH7~9֮�䣬������X��������ƽ����������pH���߶�Ѹ���½�����ԭ����_________________�� ����pH4~7֮�䣬������X��ˮ���������ȥ������Զ������������������Ϊ___________�����������X��������ȥ��Ч���ɲ�ȡ�Ĵ�ʩ��____________________________________�� |
|||
�� |
(1)������Һ�����˿����е�CO2 (2)��OH��+ H3AsO3��H2AsO3��+ H2O ����������2.2 (3)����pH7~9֮�䣬��pH����H2AsO4��ת��ΪHAsO42����������X����������������࣬����������� ����pH4~7֮�䣬������X��������磬�������Ҫ��H2AsO4����HAsO42�������Ӵ��ڣ����������ϴ���������Ҫ��H3AsO3���Ӵ��ڣ���������X��������ľ�������С ��������������������ת��Ϊ����� |
|||
| ��� | 21 |
|
||
���� |
2017���ո߿� | |||
| ��� | ����������(FexNy)�ڴż�¼�����������Ź㷺��Ӧ��ǰ����ijFexNy���Ʊ���������������ͪ���Ҵ����롣 ��1��Fe3+��̬��������Ų�ʽΪ____________________�� ��2����ͪ( 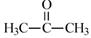 )������̼ԭ�ӹ�����ӻ�������_______________��1 mol��ͪ�����к��ЦҼ�����ĿΪ______________�� )������̼ԭ�ӹ�����ӻ�������_______________��1 mol��ͪ�����к��ЦҼ�����ĿΪ______________�� ��3��C��H��O����Ԫ�صĵ縺����С�����˳��Ϊ________________�� ��4���Ҵ��ķе���ڱ�ͪ��������Ϊ____________________�� ��5��ijFexNy�ľ�������21ͼ-1��ʾ��Cu������ȫ����þ�����aλ��Fe����bλ��Fe���γ�Cu����Ͳ���Fe(x-n) CunNy��FexNyת��Ϊ����Cu����Ͳ���������仯����21ͼ-2��ʾ�����и��ȶ���Cu����Ͳ���Ļ�ѧʽΪ___________�� 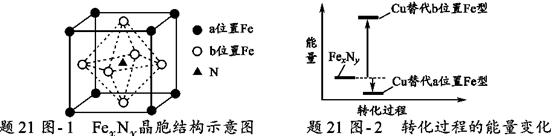 |
|||
�� |
(1)[Ar]3d5��1s22s22p63s23p63d5 (2)sp2��sp3 ������9 mol (3)H (5)Fe3CuN |
|||
| ��� | 22 |
|
||
���� |
2017���ո߿� | |||
| ��� | 1-�������һ����Ҫ���л��ϳ��м���,�е�Ϊ 71��,�ܶ�Ϊ 1.36 g��cm-3��ʵ�����Ʊ�����1-��������Ҫ��������: ����1:������A�м��������ӡ� 12 g��������20 mLˮ����ˮ��ȴ�»�������28 mLŨH2 SO4����ȴ�����£������¼��� 24 gNaBr�� ����2:��ͼ��ʾ�ʵ��װ��,��������,�� ֱ������״�����Ϊֹ�� ����3:�����Һת���Һ©�����ֳ��л��ࡣ ����4:���ֳ����л���ת���Һ©����������12 mL H2O��12 mL 5% Na2CO3��Һ��12 mL H2Oϴ�ӣ���Һ,�ôֲ�Ʒ����һ���ᴿ��1-����顣  ��1������A��������_____________�����������ӵ�Ŀ���ǽ����___________________�� ��2����Ӧʱ���ɵ���Ҫ�л���������2-������__________________________________�� ��3������2���������ƿ�ڼ���������ˮ�����ڱ�ˮԡ�е�Ŀ����___________________�� ��4������2���軺������ʹ��Ӧ������ƽ�Ƚ��У�Ŀ����______________________________�� ��4������4����5%Na2CO3��Һϴ���л���IJ��������Һ©����С�ļ���12 mL 5% Na2CO3��Һ����____________�����ã���Һ�� |
|||
�� |
(1)������ƿ������������ֹ���� (2)��ϩ�������� (3)����1-�����Ļӷ� (4)����HBr�ӷ� (5)����Һ©���¿�������б�������ų����� |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |