 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| Ȫ����2013��2014ѧ��ȸ����¿γ̸�һ��ڶ�ѧ��ģ��ˮƽ���� | |
|---|---|
| �����������⣺28 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ����������һ���������ܹ����磬���Dz����ڵ���ʵ��� ��A�������������������� B.ʳ�Ρ��������������� C.�����ᡡ������������ D.���� |
|||
�� |
A | |||
| ��� | 2 |
|
||||||||||||||||||||
���� |
2014Ȫ�ݲ��� | |||||||||||||||||||||
| ��� | ������Ʒ����Ч�ɷּ���;��Ӧ�������
|
|||||||||||||||||||||
�� |
B | |||||||||||||||||||||
| ��� | 3 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ��������������� ��A���Ͻ�����п��ܺ��зǽ���Ԫ�� ��B�����ά����Ҫ�ɷ��Ƕ������� ��C�������������Ϊ���������� ��D������Ҫͨ����ѧ��Ӧ���ܴӺ�ˮ�л��ʳ�κ͵�ˮ |
|||
�� |
C | |||
| ��� | 4 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ����������������ɢϵ��ʵ������ǡ� ��A����۳��塢������������B����������ֱ����1��100nm֮�䡡���� ��C���������������������D����ɢ������������Ĥ |
|||
�� |
B | |||
| ��� | 5 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ij��Һ�д��ڴ�����H+��Cl����SO42��������Һ�л����ܴ������ڵ��� ��A��HCO3������������B����Ba2������������C��Ag������������D��Al3�� |
|||
�� |
D | |||
| ��� | 6 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | �������ʷ����ȷ���� ��A���������ڼ��ࡡ�������������� B��Ư�����ڻ���� ��C������ͭ������������������� D����������������� |
|||
�� |
A | |||
| ��� | 7 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ����˵��������� ��A��Ħ�������ʵ����ĵ�λ ��B�������Ϲ涨�� 0.012kg 12Cԭ�������е�̼ԭ����Ŀ�����ʵ���Ϊ1Ħ ��C��1 mol H2�������� 2 g������ռ������� 22.4 L ��D����������ӵ�Ħ�������ĵ�λ�� 96g/mol |
|||
�� |
C | |||
| ��� | 8 |
|
||
���� |
2003ȫ������ | |||
| ��� | ����̽�������֣�������������к��нϷḻ��������Ϊ3�ĺ�����������Ϊδ���˾۱����Ҫԭ��֮һ�����ĸ���ͬλ��Ӧ��ʾΪ ��A�� 34He������ B�� 32He������ C�� 24He������ D�� 33He |
|||
�� |
B | |||
| ��� | 9 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ���г�ȥ���ʵķ���������ǡ������������������������������������������������������� ��A����ȥKCl�л��е�KI������ˮͨ����������������ᾧ ��B����ȥBaSO4�����л��е�BaCO3���ӹ���������� ��C����ȥFeCl2��Һ�л��е�FeCl3������������ۣ����� ��D����ȥCuO�л��е�Al2O3���ӹ���������� |
|||
�� |
C | |||
| ��� | 10 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ���������к��������ƶ���Cl�����ǡ� ��A��KClO3��Һ������������B��KCl��Һ������������ C��Һ̬HCl���������� ��D��NaCl���� |
|||
�� |
B | |||
| ��� | 11 |
|
||
���� |
δ֪ | |||
| ��� | 30mL 1mol/L NaCl��Һ��40mL 0.5mol/L CaCl2��Һ��Ϻ��Һ��Cl��Ũ��Ϊ ��A��0.5mol/L�������������������� B��0.6mol/L ��C��1.00mol/L������������������ D��2mol/L |
|||
�� |
C | |||
| ��� | 12 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | �������ӷ���ʽ��ȷ���� ��A��������NaOH��Һ��Al+2OH��=AlO2��+H2�� ��B��ϡ�����еμ�����������Һ��H+ + OH��= H2O ��C��̼��þ�еμ�ϡ���CO32��+2H+ =CO2��+ H2O ��D��п������ͭ��Һ��Ӧ��Zn+Cu2+��Zn2++Cu |
|||
�� |
D | |||
| ��� | 13 |
|
||
���� |
2013���ո߿� | |||
| ��� | �ù�����Ʒ����һ�����ʵ���Ũ�ȵ���Һ���辭���������ܽ⡢ת����Һ�����ݵȲ���������ͼʾ��Ӧ�IJ����淶���� ����  ��������������A������������������ B���ܽ⡡������C��ת�ơ�������D������ |
|||
�� |
B | |||
| ��� | 14 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | �������ʸ����������ᶼ��Ӧ���Ҷ��õ�ͬһ�ֲ������ ��A��KI���� B��Cu���� C��Fe����������D��NaOH |
|||
�� |
D | |||
| ��� | 15 |
|
|||||||||||||||
���� |
2007�����߿� | ||||||||||||||||
| ��� | ��4����Һ����ʵ�飬�±��С������������롰��Һ����Ӧ��ϵ�������
|
||||||||||||||||
�� |
B | ||||||||||||||||
| ��� | 16 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ���ڹ輰�仯����������У�������� ��A����Ļ�ѧ���ʲ����ã��ڳ����²���������Ӧ ��B��SiO2��CO2�������������������ǿ����Һ��Ӧ ��C��SiO2��CO2��������ˮ����ˮ��Ӧ������Ӧ���� ��D�������ڷǽ����������õİ뵼����� |
|||
�� |
C | |||
| ��� | 17 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ���й�����ͬʱ���������ε��� ��A��Na2O2Ͷ��ˮ�С�����������������B��ͭƬͶ�뵽FeCl3��Һ�� ��C��NaHCO3��Һ��NaOH��Һ��ϡ����� D��������ˮ���뵽AlCl3��Һ |
|||
�� |
B | |||
| ��� | 18 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ��NAΪ�����ӵ���������ֵ������˵����ȷ���� ��A�������£�18gH2O�к���2NA����ԭ�� ��B����״���£� 22.4LBr2����NA������� ��C��1mol Na������ˮ��Ӧת��2NA������ ��D��0.1 mol��L��1CH3COOH��Һ�к���0.1NA��CH3COO�� |
|||
�� |
A | |||
| ��� | 19 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | �����йؽ����Ĺ�ҵ�Ʒ��У�������� ��A�����ƣ��Ժ�ˮΪԭ���Ƶ�NaCl���ٵ������NaCl���� ��B���������Խ�̿������ʯΪԭ�ϣ���CO��ԭ����ʯ���� ��C���ƹ裺�ý�̿��ԭ��������ù� ��D����þ���Ժ�ˮΪԭ�ϣ���һϵ�й����Ƶ��Ȼ�þ����H2��ԭMgCl2��þ |
|||
�� |
D | |||
| ��� | 20 |
|
||
���� |
δ֪ | |||
| ��� | ��MgSO4��Al2(SO4)3�Ļ����Һ��, ��μ���NaOH��Һ������ͼ����, ����ȷ��ʾ������Ӧ����(�������ʾ����NaOH��Һ�����, �������ʾ��Ӧ���ɳ���������)  |
|||
�� |
D | |||
| ��� | 21 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ij��ɫ��Һ���ܺ���Na+��Ba2+��Al3+��Fe3+��Br����CO32�������ӣ�ȡ���������еμ���ˮ������ɫ��ζ�����������Һ��Ϊ��ɫ����ȡ������ε���NaOH��Һ���������������ڸ���Һ���Ʋ���ȷ���� ��A����Һ�п��ܴ���Al3+�������� B����Һ�п��ܴ���Br�� ��C����Һ��һ������CO32����������D����Һ���ܴ���Ba2�� |
|||
�� |
C | |||
| ��� | 22 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ��100 mL 0.10 mol/L��AgNO3��Һ�м���100 mL����2.08 gBaCl2����Һ����ַ�Ӧ������˵���д������ ��A���ɵõ���0.02mol�İ�ɫ���� ��B��Ba2+��NO3���������Ӷ�û�в��뷴Ӧ ��C���ڵõ�����Һ�У�Ba2+�����ʵ���Ũ��Ϊ0.05 mol/L ��D���ڵõ�����Һ�У�����Cl���������ʵ���Ϊ0.01 mol |
|||
�� |
A | |||
| ��� | 23 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | �����仯����������������ȷ�������Ҫ��Ӧ�á��ش��������⣺ ��1�����к����������������ε��������������ǵ���ʵ��������������� ����A��NH3���� B��NH3•H2O�������� C��NH4NO3������ D��HNO3������ E��N2 ��2��д��NH4NO3���뷽��ʽ������������������ �������������� ��3��0.1 mol��N2H4�����0.2molNH3���壬������ͬ�¡�ͬѹ�µ�������������������� ��������ԭ���������������������� ��4��0.5mol 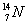 ԭ���У��������ӵ���ĿΪ���������������� ԭ���У��������ӵ���ĿΪ������������������5����״���½�����������LNH3��������ˮ�У����500mL��Һ�����ð�ˮ��Һ�����ʵ���Ũ��Ϊ1mol/L�� |
|||
�� |
��1��C������ A ��2��NH4NO3 = NH4+�� +�� NO3�� ��3��1�U2������ 3�U4 ��4��3.5NA��3.5��6.02��1023 ��5��11.2 |
|||
| ��� | 24 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ����Ҫ��Br����ʽ�����ں�ˮ�У��ӵ�����ˮ����ȡ����������£� ���������գ� ��1��д������I�з�Ӧ�����ӷ���ʽ���������������������������� ��2������I��Ӧ��ͨ����н��У�Ŀ������������������������������ ��3������II�������з�Ӧ����������з�Ӧʽ�� ����3Br2+3Na2CO3���������� ��NaBrO3 + 3CO2�� ��4������III�������·�Ӧ����˫�߷��������ת������� 3H2SO4+5NaBr+NaBrO3=3Na2SO4+3Br2+3H2O �÷�Ӧ���������������������������������� ��5������IV�IJ�������������������������� A����Һ������B���ᾧ������C�����ˡ���D������ ��6��ÿ���1 mol Br2��������5mol/L����������������L�� |
|||
�� |
��1��Cl2 + 2Br��+ = 2Cl��+ Br2 ��2����ֹ��Ⱦ���� ��3��5NaBr��4��  ������ NaBrO3 ������ NaBrO3��5��A ��6��0.2 |
|||
| ��� | 25 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ��ѧ��������A��B�ͼס��ҡ������ֻ���������ͼ��ʾ��ת����ϵ�����ֲ���δ�г���������A����ΪʳƷ��װ���ϣ��������������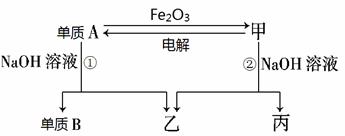 ����ͼʾת����ϵ�ش� ��1��д���������ʵĻ�ѧʽ������A_______________����_______________�� ��2��д������A��Fe2O3��Ӧ�Ļ�ѧ����ʽ���������������������������������������������������������������������������� �� ���ø÷�Ӧ��ԭ����������______________________________�� ��3���õ���A���ɵ��������Դ��������Ũ�����ԭ����____________________________�� ��4��д����Ӧ�ڵ����ӷ���ʽ��_____________________________________________�� |
|||
�� |
��1��Al������ NaAlO2 ��2��2Al + Fe2O3��  ��Al2O3 + 2Fe ��Al2O3 + 2Fe���Ӹֹ������������ ��3��Al������Ũ���ᷢ���ۻ� ��4��Al2O3 + 2OH��= 2AlO2��+ H2O |
|||
| ��� | 26 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | ijNaHCO3��Ʒ�к���NaCl���ʣ�Ϊ�ⶨ������NaHCO3������������ijͬѧ��������ַ����� ����һ��ȡ 5g��Ʒ����ˮ�������ʵ�ָʾ������ε���1mol/L���ᣬ����ȫ��Ӧʱ���ⶨ�����ĵ����������� �ش��������⣺ ��1�������ⶨ������100mL 1mol/L��� ������18mol/LŨ����������Һ������ȡŨ������������ mL�� �����ƹ����в���Ҫ�õ����������������� ��  �����ƹ����г����������������������ҺŨ����Ӱ������������� �� A��û��ϴ���ձ��Ͳ������� B�������ˮ�����˿̶��ߣ�ȡ��ˮʹҺ��ǡ�õ��̶��ߡ� C������ƿû�и�� ��2�������������������Ϊ25mL����Ʒ��NaHCO3����������Ϊ������������������ �� ���������������������̽��вⶨ��  �ش��������⣺ ��3��������������������������� ��4�������г����������������� �������ѧʽ���� ����������ȡwg��Ʒ����ͼװ�ý��вⶨ��  ��5��װ��A�з�Ӧ�Ļ�ѧ����ʽΪ���������������������������������������� ��6��װ��B���������������������� �������������� |
|||
�� |
��1����5.6mL����D����C ��2��84% ��3�������ᾧ ��4��NaCl ��5��2NaHCO3  ��Na2CO3 + H2O + CO2�� ��Na2CO3 + H2O + CO2����6������CO2��������ˮ������ |
|||
| ��� | 27 |
|
||||||
���� |
2014Ȫ�ݲ��� | |||||||
| ��� | ij�о���ѧϰС��̽��FeSO4�Ļ�ѧ���ʺ���;���ش��������⣺ ��һ��̽��FeSO4��Һ������ԣ� ��1��ȡ����FeSO4���壬����ʯ����Һ����FeSO4��Һ������ԣ�����ѡ�õ������н�ͷ�ιܡ�ҩ������������ ������A����������������B���Թܡ���������C����ƽ��������D����Ͳ ������������ͼװ��̽��FeSO4���ȶ���  ��2��II���а�ɫ�������ɣ�˵��FeSO4����ֽ��������������������������� �� A��Fe2O3���������������� B��FeO���������������� C��SO3 ���������������� D��SO2 ��3��III����ˮ�����������Ƿ���SO2�������ɣ�����SO2���ɣ���ˮ����ɫ��ʵ���У��۲쵽��ˮ��ɫ���ݴ��Ʋ�FeSO4�ֽ����п��ܱ�������Ԫ������������ ��4��NaOH������������SO2���壬��д����Ӧ��ѧ����ʽ���������������������������������������� �� ������̽��FeSO4��Fe2+��ԭ�ԣ� ��5��֤��FeSO4�н�ǿ�Ļ�ԭ�ԣ�����±���
��6��ȱ����ƶѪ�����ڷ������������������������Ƴ�ҩƬʱ���������һ����������£����������������������������������� �������������������������������������� |
|||||||
�� |
��1��B ��2��C ��3��Fe ��4��2NaOH + SO2 = Na2SO3 + H2O ��5��
|
|||||||
| ��� | 28 |
|
||
���� |
2014Ȫ�ݲ��� | |||
| ��� | Ӧ�û�ѧԭ�����Ʊ�һЩ������ش��������⣺ ��1����ŨH2O2��Һ�м�����ˮ�Ȼ��ƣ����Ƶù������ƣ�CaO2�����÷�Ӧ����������������Ӧ���������Ӧ���ͣ��� ��2����ͭ��Cu2S���ɷ�����Ӧ2Cu2S+2H2SO4+5O2==4CuSO4+2H2O������ȡCuSO4���÷�Ӧ�Ļ�ԭ��������������1mol O2������Ӧʱ����ԭ����ʧ���ӵ����ʵ���Ϊ���������� mol�� ��3�����ȸʯ��һ�ֺ�ͭ�Ŀ�ʯ����ͭ��̬ΪCuCO3��Cu(OH)2��CuSiO3��2H2O��ͬʱ����SiO2��FeCO3��Fe2O3��Al2O3�����ʡ����ù��ȸʯ��ȡCuSO4•5H2O���������£� 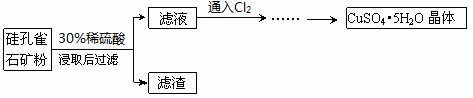 ��������Ҫ�ɷ���������������ͨ��Cl2ʱ���������������������������� д���ڿ���м���30%ϡ����ʱCuCO3��Cu(OH)2������Ӧ�����ӷ���ʽ������������������������������������������������������������������ ��4��ͭ���ܽ���ϡ�����ϡŨ������Һ�У�������Ӧ�����ӷ���ʽΪ�� ���� 3Cu+2NO3��+8H+==3Cu2++2NO��+4H2O ȫ���ܽ�������ᾧ�����õ��ľ����������������� ���ѧʽ���� |
|||
�� |
��1�����ֽⷴӦ ��2��Cu2S������ 4 ��3��SiO2������ Fe2+ CuCO3��Cu(OH)2 + 4H+ =2Cu2+ + CO2��+ 3H2O ��4��CuSO4•5H2O |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |