题干 |
应用化学原理可制备一些化合物。回答下列问题:
(1)在浓H2O2溶液中加入无水氯化钙,可制得过氧化钙(CaO2)。该反应属于 反应(填基本反应类型)。
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2==4CuSO4+2H2O用于制取CuSO4,该反应的还原剂是 ,当1mol O2发生反应时,还原剂所失电子的物质的量为
mol。
(3)硅孔雀石是一种含铜的矿石,含铜形态为CuCO3・Cu(OH)2和CuSiO3・2H2O,同时含有SiO2、FeCO3、Fe2O3、Al2O3等杂质。利用硅孔雀石制取CuSO4•5H2O的流程如下:
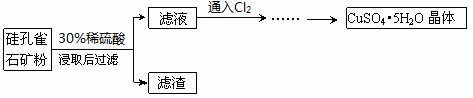
滤渣的主要成分是 ;通入Cl2时被氧化的离子有 。
写出在矿粉中加入30%稀硫酸时CuCO3・Cu(OH)2发生反应的离子方程式: 。
(4)铜可溶解于稀硝酸和稀浓硫酸混合液中,发生反应的离子方程式为:
3Cu+2NO3-+8H+==3Cu2++2NO↑+4H2O
全部溶解后,蒸发结晶,最后得到的晶体是 (填化学式)。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出