题干 |
工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为:N2(g)+2H2(g)=2NH3(g) ΔH=-92.4 kJ・mol-1 ΔS=-200 J・K-1・mol-1。回答下列问题:
(1)合成氨反应在常温下_______(填“能”或“不能”)自发。
(2)_______温(填“高”或“低”,下同)有利于提高反应速率,_______温有利于提高平衡转化率,综合考虑催化剂(铁触媒)活性等因素,工业常采用400~500 ℃。
针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
(3)方案一:双温-双控-双催化剂。使用Fe-TiO2-2xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而TiO2-2xHy的温度为415℃)。

下列说法正确的是_______。
a.氨气在“冷Ti”表面生成,有利于提高氨的平衡产率
b.N≡N在“热Fe”表面断裂,有利于提高合成氨反应速率
c.“热Fe”高于体系温度,有利于提高氨的平衡产率
d.“冷Ti”低于体系温度,有利于提高合成氨反应速率
(4)方案二:M-LiH复合催化剂。
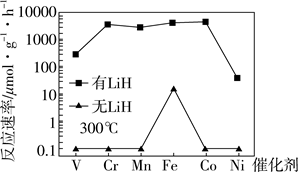 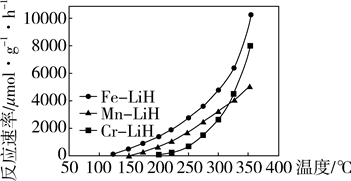
下列说法正确的是_______。
a.300℃时,复合催化剂比单一催化剂效率更高
b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(5)某合成氨速率方程为:v=k・cα(N2)・cβ(H2)・cγ(NH3),根据表中数据,γ=_______;
实验
| c(N2)/mol・L-1
| c(H2)/mol・L-1
| c(NH3)/mol・L-1
| v/mol・L-1・s-1
| 1
| m
| n
| p
| q
| 2
| 2m
| n
| p
| 2q
| 3
| m
| n
| 0.1p
| 10q
| 4
| m
| 2n
| p
| 2.828q
| 在合成氨过程中,需要不断分离出氨的原因为_______。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
(6)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为NH3配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为188g・mol-1,则M元素为_______(填元素符号);在该化合物中,M离子的价电子排布式为_______。
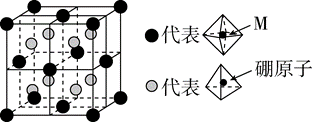
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出