题干 |
资料显示,I2可以将Cu氧化为Cu2+。某小组同学设计实验探究Cu被I2氧化的产物及铜元素的价态。
已知:I2易溶于KI溶液,发生反应I2+I-=I3-(红棕色);I2和I3-氧化性几乎相同。
I.将等体积的KI溶液加入到m mol铜粉和n mol I2(n>m)的固体混合物中,振荡。
实验记录如下:
| | c(KI)
| 实验现象
| 实验Ⅰ
| 0.01mol·L-1
| 极少量I2溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色
| 实验Ⅱ
| 0.1mol·L-1
| 部分I2溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色
| 实验Ⅲ
| 4mol·L-1
| I2完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色
| (1)初始阶段,Cu被氧化的反应速率:实验Ⅰ__________(填“>”“<”或“=”)实验Ⅱ。
(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有[Cu(H2O)4]2+(蓝色)或[CuI2]-(无色),进行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入CCl4,多次萃取、分液。
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
ⅰ.步骤a的目的是_____________________。
ⅱ.查阅资料,2Cu2++4I-=2CuI↑+I2,[Cu(H2O)4]2+(无色)容易被空气氧化。用离子方程式解释步骤b的溶液中发生的变化:______________。
(3)结合实验Ⅲ,推测实验Ⅰ和Ⅱ中的白色沉淀可能是CuI,实验Ⅰ中铜被氧化的化学方程式是____________________。分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入浓KI溶液,__________(填实验现象),观察到少量红色的铜。分析铜未完全反应的原因是____________________。
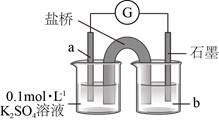
(4)上述实验结果,I2仅将Cu氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了I2能将Cu氧化为Cu2+。装置如图所示,a、b分别是_____________。
(5)运用氧化还原反应规律,分析在上述实验中Cu被I2氧化的产物中价态不同的原因:_________。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出