题干 |
硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根(S2O32-)可看作是SO42-中的一个O原子被S原子取代的产物。
(1)基态S原子价层电子排布式是__________。
(2)比较S原子和O原子的第一电离能大小,从原子结构的角度说明理由:____________________。
(3)S2O32-的空间结构是__________。
(4)同位素示踪实验可证实S2O32-中两个S原子的化学环境不同,实验过程为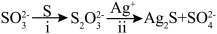 。过程ⅱ中,S2O32-断裂的只有硫硫键,若过程ⅰ所用试剂是Na232SO3和35S,过程ⅱ含硫产物是__________。 。过程ⅱ中,S2O32-断裂的只有硫硫键,若过程ⅰ所用试剂是Na232SO3和35S,过程ⅱ含硫产物是__________。
(5)MgS2O3·6H2O的晶胞形状为长方体,边长分别为a nm、b nm、c nm,结构如图所示。
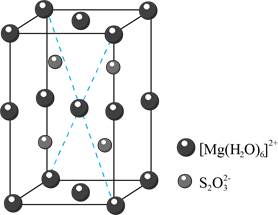
晶胞中的[Mg(H2O)6]2+个数为__________。已知MgS2O3·6H2O的摩尔质量是Mg·mol-1,阿伏加德罗常数为NA,该晶体的密度为__________g·cm-3。(1nm=10-7cm)
(6)浸金时,S2O32-作为配体可提供孤电子对与Au+形成[Au(S2O3)2]3-。分别判断S2O32-中的中心S原子和端基S原子能否做配位原子并说明理由:____________________。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出