题干 |
利用平衡移动原理,分析一定温度下Mg2+在不同pH的Na2CO3体系中的可能产物。
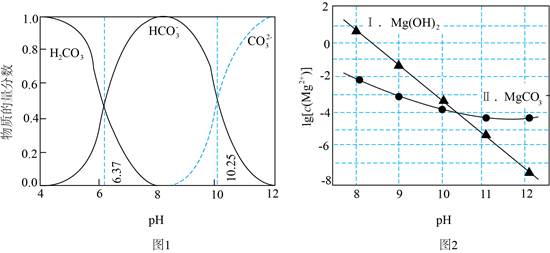
已知:i.图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系。
ii.2中曲线Ⅰ的离子浓度关系符合c(Mg2+)・c2(OH-)=Ksp[Mg(OH)2];曲线Ⅱ的离子浓度关系符合c(Mg2+)・c(CO32-)=Ksp(MgCO3) [注:起始c(Na2CO3)=0.1mol・L-1,不同pH下c(CO32-)由图1得到]。
下列说法不正确的是
A.由图1,pH=10.25,c(HCO3-)=c(CO32-)
B.由图2,初始状态pH=11、lg[c(Mg2+)]=-6,无沉淀生成
C.由图2,初始状态pH=9、lg[c(Mg2+)]=-2,平衡后溶液中存在
c(H2CO3)+c(HCO3-)+c(CO32-)=0.1mol/L
D.由图1和图2,初始状态pH=8、lg[c(Mg2+)]=-1,发生反应:Mg2++2HCO3-=MgCO3↓+CO2↑H2O
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出