题干 |
配合物广泛存在于自然界,且在生产和生活中都发挥着重要作用。
(1)某有机物R能与Fe2+形成橙红色的配离子[FeR3]2+,该配离子可被HNO3氧化成淡蓝色的配离子[FeR3]3+。
①基态Fe2+的3d电子轨道表示式为___________。
②完成反应的离子方程式:NO3-+2[FeR3]2++3H+ +2[FeR3]3++H2O +2[FeR3]3++H2O
(2)某研究小组对(1)中②的反应进行了研究。
用浓度分别为2.0mol・L-1、2.5 mol・L-1、3.0 mol・L-1的HNO3溶液进行了三组实验,得到c([FeR3]2+)随时间t的变化曲线如图。
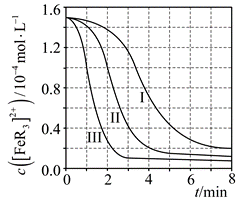
①c(HNO3)=3.0 mol・L-1时,在0~1min内,[FeR3]2+的平均消耗速率=___________。
②下列有关说法中,正确的有___________。
A.平衡后加水稀释,c([FeR3]2+): c([FeR3]3+)增大
B.[FeR3]2-平衡转化率:αⅢ>αII>αI
C.三组实验中,反应速率都随反应进程一直减小
D.体系由橙红色转变为淡蓝色所需时间:tⅢ>tII>tI
(3)R的衍生物L可用于分离稀土。溶液中某稀土离子(用M表示)与L存在平衡:
M+L ML K1 ML K1
ML+L ML2 K2 ML2 K2
研究组配制了L起始浓度c0(L)=0.02mol・L-1、M与L起始浓度比c0(M)/ c0(L)不同的系列溶液,反应平衡后测定其核磁共振氢谱。配体L上的某个特征H在三个物种L、ML、ML2中的化学位移不同,该特征H对应吸收峰的相对峰面积S(体系中所有特征H的总峰面积计为1)如下表。
c0(M)/ c0(L)
| S(L)
| S(ML)
| S(ML2)
| 0
| 1.00
| 0
| 0
| a
| x
| <0.01
| 0.64
| b
| <0.01
| 0.40
| 0.60
| 【注】核磁共振氢谱中相对峰面积S之比等于吸收峰对应H的原子数目之比;“<0.01”表示未检测到。
①c0(M)/ c0(L)=a时,x= ___________。
②c0(M)/ c0(L)=b时,平衡浓度比c平(ML2): c平(ML)=___________。
(4)研究组用吸收光谱法研究了(3)中M与L反应体系。当c0(L)=1.0×10-5mol・L-1时,测得平衡时各物种c平/ c0(L)随c0(M)/ c0(L)的变化曲线如图。c0(M)/ c0(L)=0.51时,计算M的平衡转化率___________(写出计算过程,结果保留两位有效数字)。

|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出