题干 |
科学家研究发现CH3I热裂解时主要发生如下反应:
反应ⅰ:2CH3I(g) 2HI(g) + C2H4(g) ΔH1=+80.2kJ·mol-1 2HI(g) + C2H4(g) ΔH1=+80.2kJ·mol-1
反应ⅱ:2C2H4(g) C4H8(g) ΔH2=-84kJ·mol-1 C4H8(g) ΔH2=-84kJ·mol-1
反应ⅲ:3C2H4(g) 2C3H6(g) ΔH3=-108kJ·mol-1 2C3H6(g) ΔH3=-108kJ·mol-1
反应ⅳ:2HI(g) H2(g) + I2 (g) ΔH4=+11kJ·mol-1 H2(g) + I2 (g) ΔH4=+11kJ·mol-1
回答下列问题:
(1)反应3 CH3I (g) C3H6(g)+3HI(g) ΔH =_________kJ·mol-1 C3H6(g)+3HI(g) ΔH =_________kJ·mol-1
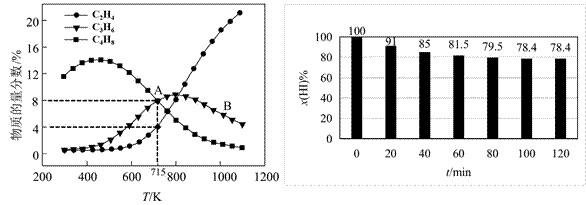
(2)在密闭刚性容器中投料1mol CH3I(g),若只发生反应ⅰ、ⅱ、ⅲ,平衡总压强为p MPa,温度对平衡体系中乙烯、丙烯和丁烯物质的量分数的影响如下图甲所示。
①随温度升高,C3H6物质的量分数先增大后减小的原因是_________。
②CH3I(g)转化率α(A)_________α(B)(填“>” “<”或“=”);
715K时,反应ⅰ平衡常数Kp=_________MPa(列计算式)。
图甲 图乙
(3)反应ⅳ的相关信息如下表:
H-H键能
| I-I键能
| H-I键能
| 正反应活化能Ea
| 436kJ·mol-1
| 151kJ·mol-1
| m kJ·mol-1
| 173.1kJ·mol-1
| ①m=_________,反应ⅳ逆反应的活化能=_________kJ·mol-1。
②研究反应ⅳ发现:v 正=ka·x(H2)·x(I2),v 逆=kb·x2(HI),其中ka、kb为常数。在某温度下,向刚性密闭容器中充入一定量的HI(g),碘化氢的物质的量分数x(HI)与反应时间t的关系如上图乙所示。
0~ 40min,反应的平均速率v(HI)=_________min-1(用单位时间内物质的量分数的变化表示)。该温度下,反应ⅳ的Ka/Kb=________(列计算式)。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出