题干 |
学习小组在实验室中利用如图所示装置制备SO2并进行相关性质的探究。
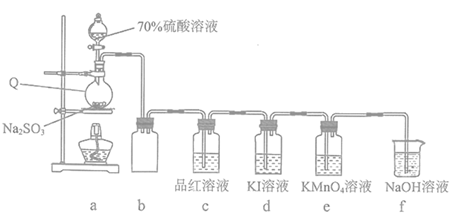
回答下列问题:
(1)仪器Q的名称为__;装置b的作用是__。
(2)装置a中反应的化学方程式为__。
(3)装置e中出现__(填现象)可证明SO2具有还原性。
(4)实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:SO2+4I-+4H+ S↓+2I2+2H2O。 S↓+2I2+2H2O。
探究Ⅰ:探究浓度对上述可逆反应的影响
有同学认为除SO2的浓度外,其他离子的浓度对该可逆反应也有影响。完成实验设计进行验证(SO2体积已折算为标准状况下体积)。
限选试剂:0.1mol•L-1KI溶液、1.0mol•L-1KI溶液、2.0mol•L-1KI溶液、蒸馏水、浓硝酸、浓盐酸
影响因素
| 编号
| 操作
| 现象
| c(I-)
| ⅰ
| 取50mL①__于锥形瓶中,向其中通入20mLSO2
| 溶液变为浅黄色
| ⅱ
| 取50mL1.0mol•L-1溶液于锥形瓶中,向其中通入20mLSO2
| 溶液迅速变黄
| c(H+)
| ⅲ
| 取50mL1.0mol•L-1溶液和5mL②__于锥形瓶中,向其中通入20mLSO2
| 溶液迅速变黄
| ⅳ
| 取50mL1.0mol•L-1溶液和5mL③___于锥形瓶中,向其中通入20mLSO2
| 溶液迅速变黄,且出现乳黄色浑浊
| 探究Ⅱ:探究SO2在KI溶液体系中的反应产物
有同学提出上述可逆反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO42-+2I-+4H+。
为进一步探究体系中的产物,完成下列实验方案。
方案
| 操作
| 预期现象
| 结论
| ⅰ
| 取适量装置d中浊液,向其中滴加几滴④___溶液(填试剂名称),振荡
| 无明显变化
| 浊液中无I2
| ⅱ
| 将装置d中浊液进行分离
| 得淡黄色固体和澄清溶液
| | 取适量分离后的澄清溶液于试管中,⑤___
| ⑥___
| ⑦__
| ⑧综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为__。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出