题干 |
实验小组探究酸对Fe3++3SCN- Fe(SCN)3平衡的影响。将0.005 mol∙L−1FeCl3溶液(接近无色)和0.01 mol∙L−1KSCN溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。 Fe(SCN)3平衡的影响。将0.005 mol∙L−1FeCl3溶液(接近无色)和0.01 mol∙L−1KSCN溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。
(1)FeCl3水解显酸性的原因是___(用方程式表示)。
(2)甲同学认为加入酸后,会使Fe3++3SCN- Fe(SCN)3体系中___浓度改变,导致该平衡正向移动,溶液颜色加深。 Fe(SCN)3体系中___浓度改变,导致该平衡正向移动,溶液颜色加深。
【设计并实施实验】
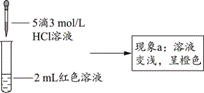 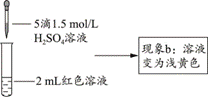
【查阅资料】
Fe3+和Cl-、SO42-均能发生络合反应:
Fe3++4Cl- [FeCl4]-(黄色);Fe3++2SO42- [FeCl4]-(黄色);Fe3++2SO42- [Fe(SO4)2]-(无色)。 [Fe(SO4)2]-(无色)。
实验I.探究现象a中溶液颜色变化的原因
编号
| 操作
| 现象
| ①
| 向2mL红色溶液中滴加5滴水
| 溶液颜色无明显变化
| ②
| 向2mL红色溶液中滴加5滴3 mol∙L−1KCl溶液
| 溶液颜色变浅,呈橙色
| (3)实验①的目的是___。
(4)根据实验①和实验②的结果,从平衡移动角度解释现象a:___。
实验Ⅱ.探究现象b中溶液呈浅黄色的原因
编号
| 操作
| 现象
| ③
| 取1mL0.0025 mol∙L−1Fe2(SO4)3溶液(无色),加入1mL0.01 mol∙L−1KSCN溶液,再加入5滴1.5 mol∙L−1H2SO4溶液
| 溶液先变红,加硫酸后变为浅黄色
| ④
| 取1mL 0.005 mol∙L−1FeCl3溶液,
| | (5)结合实验③可推测现象b中使溶液呈浅黄色的微粒可能有两种,分别是___。
(6)乙同学进一步补充了实验④,确证了现象b中使溶液呈浅黄色的微粒只是(5)中的一种,请将实验④的操作及现象补充完整:___、___。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出