题干 |
羰基硫(COS)是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。以FeOOH作催化剂,分别以CO和CO2为碳源,与H2S反应均能产生COS,反应如下
反应I:CO(g)+H2S(g)⇌COS(g)+H2(g)
反应Ⅱ:CO2(g)+H2S(g)⇌COS(g)+H2O(g)
(1)以CO为碳源制COS反应分两步进行,其反应过程能量变化如图所示。
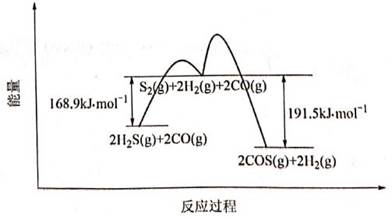
①CO(g)+H2S(g) COS(g)+H2(g) △= 。 COS(g)+H2(g) △= 。
②决定COS生成速率的步骤是 (填“第1步”或“第2步”)
(2)在密闭容器中按下表投料,分别发生反应Ⅰ和反应Ⅱ(N2不参与反应),反应时间和压强相同时,测得COS的物质的量分数随温度变化关系如下图实线所示(虚线表示平衡曲线)。
| | 反应Ⅰ
| 反应Ⅱ
| 起始投料
| CO
| H2S
| N2
| CO2
| H2S
| N2
| 起始物质的量分数/%
| 1
| 1
| 98
| 1
| 1
| 98
| 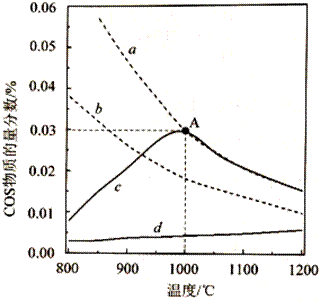
①已知相同条件下,反应Ⅰ速率比反应Ⅱ快。反应Ⅰ的平衡曲线是 (填标号)。800~ 1200℃时,曲线d中COS物质的量分数不断增大,原因是 。
②下列说法正确的是 (填标号)。
A.降低反应温度,CO和CO2的平衡转化率均增大
B.该实验中, 900℃时,反应Ⅰ的COS生成速率大于分解速率
C.恒温恒容下反应Ⅱ达到平衡后,增大N2的体积分数,平衡正向移动
D.选用合适的催化剂均能增大反应Ⅰ和反应Ⅱ的COS的平衡产率
③A点对应的平衡体系中,H2S的转化率为 ,该温度下反应的平衡常数K=
(写计算式)
(3)用COS处理过的粮食食用前需水洗,水洗时COS转化为两种气体,该反应的化学方程式为 。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出