题干 |
能源开发、环境保护、资源利用等是化学应用的重要方向。回答下列问题:
⑴催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g) + O2(g)=2NO(g) △H1=+180.5 kJ · mol-1;
2C(s)+ O2(g)=2CO(g) △H2=-221.0 kJ · mol-1;
C(s)+ O2(g)=CO2(g) △H3=-393.5 kJ · mol-1
则尾气转化反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H =________________。
⑵CO2可通过反应CO2(g)+CH4(g) 2CO(g)+2H2(g)来制取H2。在1.0L密闭容器中充入CO2、CH4各1mol,发生上述反应,测得CH4的平衡转化率与温度压强的关系如图a所示 2CO(g)+2H2(g)来制取H2。在1.0L密闭容器中充入CO2、CH4各1mol,发生上述反应,测得CH4的平衡转化率与温度压强的关系如图a所示
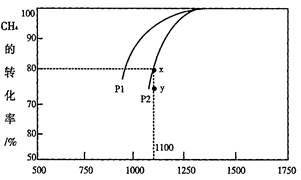
① 由图a可知,压强P1______P2(填“大于”或“小于”),该反应的△H_______0(填“大于”或“小于”)
② 当压强为P2时,y点的υ(正)____ υ(逆) (填“大于”、“小于”或“=”);y点对应温度下,该反应的平衡常数K=___________(保留四位有效数字)。
③ 实验表明,温度高于1250℃时,容器中c(CO2)>c(CH4),请结合两种反应物的性质分析可能的原因:_______________________________________________。
⑶  汽车尾气分析仪对CO的含量分析是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质中自由移动。 汽车尾气分析仪对CO的含量分析是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质中自由移动。
① 请写出负极反应式:_______________________,②该仪器工作时,O2-移向_______极(填写a或b)。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出