题干 |
碱式碳酸镁可用于牙膏、医药和化妆品等工业,化学式为4MgCO3・Mg(OH)2・5H2O,某碱式碳酸镁中含有SiO2杂质,为测定其纯度,某兴趣小组设计了如下几个方案:
方案I 取一定质量的样品,与硫酸充分反应,通过测定生成CO2的质量计算纯度
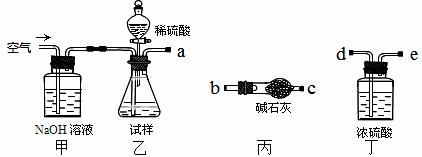
(1)乙中发生反应的方程式为 。
(2)仪器接口的连接顺序为(装置可以重复使用)a ,丁的作用是 。
(3)当样品充分反应完后,缓慢通入空气的目的是: 。
方案Ⅱ ①称取碱式碳酸镁样品mg;②将样品充分高温煅烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g。
(4)下列仪器中,该方案不会用到的是 。
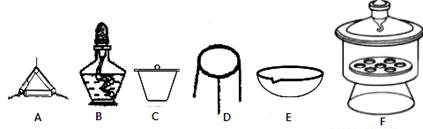
(5)判断样品完全分解的方法是 ;本实验至少需要称量 次。
(6)有同学认为方案Ⅱ高温煅烧的过程中会发生MgCO3 + SiO2 MgSiO3 + CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗? ,(填“正确”或“错误”)请说明自己的理由: 。 MgSiO3 + CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗? ,(填“正确”或“错误”)请说明自己的理由: 。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出