题干 |
“84消毒液”因1984年北京某医院研制使用而得名,在日常生活中使用广泛,其有效成分是NaClO。某小组在实验室制备NaClO溶液,并进行性质探究和成分测定。
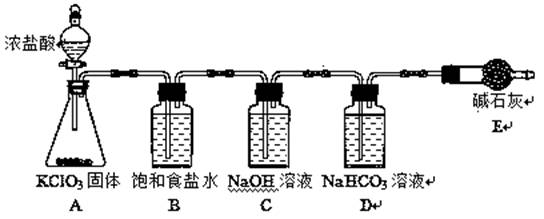
(1)该小组按上图装置进行实验,反应一段时间后,分别取B、C、D瓶的溶液进行实验,实验现象如下表。(已知饱和NaClO溶液pH为11)
实验步骤
| 实验现象
| B瓶
| C瓶
| D瓶
| 实验1:取样,滴加紫色石蕊溶液
| 变红,不褪色
| 变蓝,不褪色
| 立即褪色
| 实验2:取样,测定溶液的pH
| 3
| 12
| 7
| ①装置A中反应的化学方程式为________。
②B瓶溶液中H+的主要来源是________。
③C瓶溶液的溶质是________(填化学式)。
④结合平衡移动原理解释D瓶溶液中石蕊立即褪色的原因________。
(2)测定C瓶溶液中NaClO含量(单位:g・L-1)的实验步骤如下:
Ⅰ.取C瓶溶液20 mL于锥形瓶,加足量盐酸酸化,迅速加入过量KI溶液,盖紧瓶塞并在暗处充分反应。
Ⅱ.用0.1000 mol・L-1Na2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点时共用去20.00 mL Na2S2O3溶液。(I2+2S2O32-==2I-+S4O62-)
①步骤Ⅰ总反应的离子方程式为_______,盖紧瓶塞并在暗处反应的原因是________。
②C瓶溶液中NaClO的含量为________g・L-1。(保留1位小数。NaClO式量为74.5)
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出