题干 |
TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

资料:TiCl4及所含杂质氯化物的性质
化合物
| SiCl4
| TiCl4
| AlCl3
| FeCl3
| MgCl2
| 沸点/℃
| 58
| 136
| 181(升华)
| 316
| 1412
| 熔点/℃
| −69
| −25
| 193
| 304
| 714
| 在TiCl4中的溶解性
| 互溶
| ――
| 微溶
| 难溶
| (1)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ΔH1=+175.4 kJ・mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220.9 kJ・mol-1
①沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:_______________________。
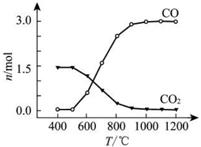
②氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的ΔH_____0(填“>”“<”或“=”),判断依据:_______________。
③氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是__________________________。
④氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤 渣中含有_____________。
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4。示意图如下:
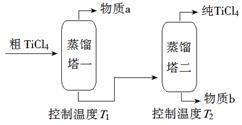
物质a是______________,T2应控制在_________。
|
 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出