 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| �������ۺ� | |
|---|---|
| �����������⣺25 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2003ȫ������ | |||
| ��� | ij��ɫ������������CH4��NH3��H2��CO��CO2��HCl�е�ij����������ɡ��ں��º�ѹ�����£����˻������ͨ��ŨH2SO4ʱ��������������䣻ͨ�������ij���ʯ��ˮ��δ������ǣ������������������С����ʣ�����嵼������O2���ܹ���ȼ��ȼ�ղ��ﲻ��ʹCuSO4��ĩ��ɫ����ԭ�������ijɷ��� ��A�� HCl��CO������ B�� HCl��H2��CO������ C�� CH4��NH3������ D�� HCl��CO��CO2 |
|||
�� |
A | |||
| ��� | 2 |
|
||
���� |
1993ȫ���߿� | |||
| ��� | ��ij��Һ�м�������������ɰ�ɫ����;���˺�����Һ�м�������İ���(ʹ��Һ�ʼ���),���а�ɫ��������;�ٹ��˺�����Һ�м���̼������Һ,�����ɰ�ɫ����.ԭ��Һ�к��е����ӿ����ǡ��� ��A��Ag+��Cu2+��Ba2+����B��Ag+��Ba2+��Al3+��������C��Ag+��Al3+��Ca2+��������D��Al3+��Mg2+��K+ |
|||
�� |
B��C | |||
| ��� | 3 |
|
||
���� |
δ֪ | |||
| ��� | ���и������ʻ�Ϻ��ټ������ɣ�����300��ʱ����������������䣬���յõ��IJ����ǻ������� ��A�����ʵ���Ũ����ͬ��(NH4)2SO4��BaCl2�������� ��B����FeSO4��Һ��ͨ�����Cl2 ��C����FeI2��Һ�м�������H2O2 ��D�������ʵ�����NaHCO3��Na2O2 |
|||
�� |
B��D | |||
| ��� | 4 |
|
||
���� |
2000ȫ������ | |||
| ��� | ���Ȼ������Ȼ�ͭ����������Һ�м������ۣ�����Ӧ��������ʣ��Ĺ����˳����ܱ�������������Ӧ����Һ�д��ڽ϶���������� ��A��Cu2+���������� B��Fe3+�������������� C��Fe 2+�������������� D��H+ |
|||
�� |
C | |||
| ��� | 5 |
|
||
���� |
δ֪ | |||
| ��� | �����и������ʣ���ֻ��һ��ʱ���ȡ����Һ�������м���100mL 0.1mol/LNaOH����Һһ���������ǵ��� ��A��100mL 0.1mol/L BaCl2��Һ��100mL 0.1mol/L NaHCO3��Һ ��B��0.01molAl��100mL 0.1mol/L������Һ ��C��100mL 0.1mol/L A lCl3��100mL 0.3mol/L NH3��H2O ��D��100mL0.1mol/L NH4Cl��100mL0.1mol/L AlCl3��Һ |
|||
�� |
B | |||
| ��� | 6 |
|
||
���� |
2003�㶫�߿� | |||
| ��� | ��ij������Һ�����ܺ���Br����SO42����H2SO3��NH4�����ֱ��������ʵ�飺 ���ټ���ʱ�ų����������ʹƷ����Һ��ɫ ���ڼӼ�������Ժ���ʱ�ų����������ʹ��ʪ�ĺ�ɫʯ����ֽ������ ���ۼ�����ˮʱ����Һ���Ի�ɫ���ټ���BaCl2��Һʱ�������İ�ɫ����������ϡ���� �����������ʲ���ȷ��������Һ���Ƿ���ڵ��� ��A�� Br�������� B�� SO42�������� C�� H2SO3������ D�� NH4�� |
|||
�� |
B | |||
| ��� | 7 |
|
||
���� |
2005Ȫ��ģ�� | |||
| ��� | Ϊ�ⶨij���ε���ɣ�ȡһ�����ĸ�����Ʒ���Ƴ�ˮ��Һ�� ��  ������ ��ش��������⣺ ��1��д������C�Ͱ�ɫ����F�Ļ�ѧʽ��C�������������������������������� ��F���������������������������������� �� ��2����Ӧ�ٵ����ӷ���ʽ�ǣ��������������������������������������������������������������������� �� ��3���ø��εĻ�ѧʽ�ǣ����������������������������������������� �� ��4�������¸ø�����Һ��pH�������������������� 7����д����������������=������ |
|||
�� |
��1��NH3��BaSO4 ��2��2Fe2++Cl2��Fe3++2Cl�� ��3��(NH4)2Fe(SO4)2 ��д��Fe (NH4)2 (SO4)2Ҳ���֣� ��4���� |
|||
| ��� | 8 |
|
||
���� |
2009Ȫ���ʼ� | |||
| ��� | ̼���һ�ֽϳ�ʹ�õĻ��ʣ����ڳ������ֽ⡣ij��ѧ��ȤС���̼淋ijɷִ������ʣ�����������̽���� ������ʵ�顿������Һ�е����������ӡ� ȡ������������Թ��У��������ᣬ�����ɵ�����ͨ�����ʯ��ˮ�У��а�ɫ�������ɡ�����ȡ����̼立����Թ��У�����ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ�������ɵ����壬ʯ����ֽ����ɫ�� ����1������ʵ�������Ʋ�̼��������������ӿ����������������������� ����2������ʵ������̼���NaOH��Һ��Ӧ�����ӷ���ʽ���������������������������������������� ������ʵ�顿�ⶨ̼���CԪ�غ�NԪ�������ȡ� ����ȤС��ȷ��ȡag̼泥�����ʹ֮�ֽ⣬���Ѳ���ͨ���ʯ���У�����ͼ��ʾ��  �� �� ��1��̼粒���Ӧ���������������н��м��ȡ� ������A���Թܡ�����B����������C����ƿ��������D������ ��2���Ӱ�ȫ�ĽǶȿ��ǣ�β��������װ�ÿ���ѡ��������������  ��������������A������������������ B������������������������ C�� ������������������ D ��3�������պ�û�й�����࣬����U�ι���ʵ��ǰ���������Ϊbg���ɴ˲��NԪ�ص���������������g�� ��4��Ϊ�˲ⶨ̼���̼Ԫ�ص�������������Ƶ�ʵ�鷽���ǽ�ag̼���ȫ�ܽ���ˮ���������BaCl2��Ȼ��ⶨ���ɳ����������������۸÷����Ƿ��������������������������������������������������������������������������������������������������� ���������������� |
|||
�� |
������ʵ�顿 ��1��HCO3����CO32�� ��2��NH4����OH����NH3����H2O��HCO3����OH����CO32����H2O ����NH4����HCO3����2OH����NH3��CO32����2H2O������������������ ������ʵ�顿 ��1��A ��2��A ��3��  ��4����С�����ڿ��������⣬�������ش𡰺���������������������������Ӧ���ͣ���������֡����磺�����ش� �ٲ���������Ϊ̼��п��ܺ���HCO3����������BaCl2���������������̼Ԫ������������ȷ����3�� �ں�������Ϊ̼���ֻ����CO32��������BaCl2����ȫ���ɳ�������ȷ���̼Ԫ�ص�����������3�� �۲���������õĽ����ȷ����2�� |
|||
| ��� | 9 |
|
||
���� |
2009ȫ���߿� | |||
| ��� | ��֪�����������ȵ�����ͭ��Ӧ�õ������ͽ���ͭ����ʾ��ͼ�е�װ�ÿ���ʵ�ָ÷�Ӧ�� �ش��������⣺ ��1��A�м����������_______________________________________. ������Ӧ�Ļ�ѧ����ʽ��___________________________________; ��2��B�м����������__________����������____________________: ��3��ʵ��ʱ��C�й۲쵽��������________________________�� ������Ӧ�Ļ�ѧ����ʽ��________________________________; (4)ʵ��ʱ��D�й۲쵽��������____________________________�� D���ռ�����������___________,��������ʵķ�����������_______________. |
|||
�� |
��1������NH4Cl Ca(OH)2
2NH4Cl+Ca(OH)2 CaCl2NH3��+2H2O CaCl2NH3��+2H2O �������𰸺���Ҳ���֣� ��2����ʯ�ң���CaO�� ��ȥNH3�����е�ˮ�� ��3����ɫ��ĩ������Ϊ��ɫ��2NH3+3CuO  N2+3H2O+3Cu N2+3H2O+3Cu��4��������ɫҺ�� ��ˮ �ú�ɫʯ����ֽ���顢��ֽ���� ����ˮ����ͭ���顢��ˮ����ͭ���� |
|||
| ��� | 10 |
|
||||
���� |
2008Ȫ��ģ�� | |||||
| ��� | A��B��C��D�������ʾ�Ϊ����������ɵĿ����Ի����������������ʵ����ӣ����Ӳ����ظ���ϣ��У�
��B��Һ�ֱ���C��D��ϣ����а�ɫ�������� �ڽ�A��Һ��ε���C��Һ�У��г������ɣ������μ�A��Һʱ����������ֱ����ȫ��ʧ ��A��D���ֹ��������������ɣ���������ʹʪ��ĺ�ɫʯ����Һ���� ����ʯī�缫���B��Һ���������ϲ���һ���д̼�����ζ������ �ش��������� ��1��A�����������ӵĵ���ʽ���������������������� B���������������������������� ��2��C�Ļ�ѧʽ���������������������� D�Ļ�ѧʽ���������������������� ��3����PtΪ�缫���1L0.1mol/LB��ˮ��Һ������·��ͨ��0.1mol����ʱ����Һ��pHΪ���������������� �����������Һ������䣩�������ĵ缫��ӦʽΪ �������������������������������������������������������������� ��4��д�����г����ܽ�����ӷ���ʽ �������������������������������������������������������������������������� |
|||||
�� |
��1��[:O:H:]����Ba2+ ��2��Al2(SO4)3��(NH4)2CO3 ��3��13��2Cl����2e����Cl2�� ��4��Al(OH)3+OH����AlO2��+H2O |
|||||
| ��� | 11 |
|
||
���� |
2008ȫ����� | |||
| ��� | ij������Һ���ܺ���������NO3����CO32����SO32����SO42����Cl����Br3����I����Ϊ������Щ����-���ֱ�ȡ������Һ��������ʵ�飺 �ٲ�û��Һ�ʼ��ԣ� �ڼ�HCl��������ɫ��ζ���塣��������ʹ����ʯ��ˮ��Һ����ǣ� �ۼ�CCl4���μ�������ˮ����CCl4��δ��ɫ�� �ܼ�BaBl2��Һ������ɫ���������룬�ڳ����м����������ᣬ����������ȫ�ܽ⣻ �ݼ�HN03�ữ���ټӹ���AgNO3����Һ��������ɫ������ ��1����������5��ʵ�飬д��ÿһʵ��������ӵĽ��������ɡ� ʵ���______________________________________________________________�� ʵ���______________________________________________________________�� ʵ���______________________________________________________________�� ʵ���______________________________________________________________�� ʵ���______________________________________________________________�� ��2������5��ʵ�鲻��ȷ���Ƿ���ڵ�����___________________________________�� |
|||
�� |
��1����CO32����SO32�����ܴ��ڣ�������ˮ��ʼ��� ��CO32���϶����ڣ������������CO2����SO32�����ڣ���Ϊû�д̼�����ζ��������� ��Br����I�������ڣ���û����͵����ɫ���� ��SO42�����ڣ���BaSO4���������� ��Cl�����ڣ�����Ag+�γɰ�ɫ���� ��2��NO3�� |
|||
| ��� | 12 |
|
||
���� |
2010Ȫ���ʼ� | |||
| ��� | �����������Ի������Һ�о�����NO3������������ԭ��Ӧ��ת����ϵ����ͼ��ʾ�� �� �����У�����D��F��Ӧ�������Σ�����D��A��Һ��Ӧ���ɰ�ɫ������ ��ش��������⣺�� ��1��д��Al3+�Ľṹʾ��ͼ�������������������� ��2�����������ӷ���ʽ�ĺ�������д����Ļ�ѧʽ������Ҫ��ƽ�� ������Al+NO3��+OH��+H2O��������������+���������� ��3����Aת��ΪB���ɼ�����Լ������������������� ��4��д��D����C��Ӧ�Ļ�ѧ����ʽ�� ��5��C��E��������л���ɴ�����Ⱦ���ڴ��������£�D���Խ�C��Eת��Ϊ������̬���ʣ��õ������������������� ��6��д������D��һ����;������������������������������ ������������������������������������������������ ��7��Al��NO3�������������·�Ӧ��Al�뱻��ԭ��NO3�������ʵ���֮���������������� |
|||
�� |
��1�� ��2��AlO2�� NH3 ��3��NaOH��Һ ��4��4NH3+5O2= 4NO+6H2O ��5��N2 ��6����������ƻ��ʵ� ��7��1�U1 |
|||
| ��� | 13 |
|
|||||||||||
���� |
2009Ȫ���ʼ� | ||||||||||||
| ��� | ij��ѧ̽��С������ͭƬ��ȡCu(NO3)2����̽���仯ѧ���ʡ� ��һ�������Ȱ�ͭ�۷��ڿ��������գ�����ϡHNO3��Ӧ��ȡ����ͭ�� ��1�����ֱ����ͭм��HNO3��Ӧ����ȡ����ͭ�����ܵ��µ��������������������������������������������������������������� ������������ ���������������������������������������������������������������������� �� ��2��ʵ����ͭӦ�÷������������������������� �����������ƣ������ա����ӷ�Ӧ�����Һ�еõ�����ͭ���壬ʵ��������谴˳��ֱ��� �������������������������������������������������� �����ˡ��� ������Ϊ��̽��Cu(NO3)2���ȶ��ԣ�̽��С������ͼ�е�װ�ý���ʵ�顣��ͼ������̨�����кͼ����豸����ȥ��
�����Թ��з�����ϸ����ˮCu(NO3)2���岢���ȣ��۲쵽���Թ����к���ɫ�������ɣ����ղ�����ɫ��ĩ����U�ܳ�ȥ����ɫ���壬�����Թ����ռ�����ɫ���塣 ����1������ɫ������ ���������������������������������� ����2�������ܿڲ���������ð��ʱ��ֹͣ��Ӧ����ʱ�ڲ�����Ӧע������������������������������������������ �������������������������� ��3�����������˺���ɫ���壬̽��С���ж�Cu(NO3)2�ķֽ�����������ԭ��Ӧ����һ���������ƶϣ����Թ����ռ���������һ�������������������������� �� ������Ϊ��̽��Cu(NO3)2�����������¸������ʵķ�Ӧ������ȡһ֧�Թܣ�����Cu(NO3)2��Һ����������ϡ�����ữ���ټ���һ�������ۣ�ʵ���û�й���������ʴ��ڡ� ��1����Ӧ�п������������õ������������������������������� ���� ��2����̽��С��Է�Ӧ����Һ����Ԫ�صļ�̬����̽�������������ʵ�鷽����������ʵ�顣���ڴ���ϰ��±���ʽ����д��ʵ��������衢Ԥ����������ۡ�
|
||||||||||||
�� |
��һ�� ��1�����ɵ����ʵ���������ͭ����������ԭ�϶࣬�Ҳ�����Ⱦ�ﵪ����� ��2������������Ũ������ȴ�ᾧ ������ ��1��NO2 ��2���Ȱѵ������Ƴ�ˮ�棬Ȼ��Ϩ����� ��3��O2 ������ ��1��HNO3��Cu2+ ��2�����ܣ� ��KMnO4��Һ���Ϻ�ɫ��ȥΪ��ɫ��Һ����˵����������Ԫ�صļ�̬��+2�ۣ�������ɫ����˵����������Ԫ�صļ�̬����+2�ۡ� ��ȡ������Һ���μ�KSCN��Һ�� |
||||||||||||
| ��� | 14 |
|
||
���� |
2007Ȫ���ʼ� | |||
| ��� | ij�о�ѧϰС����ĵ��������ϣ��������ͼ��ʾ��װ����̽��NH3�Ļ�ԭ�ԡ� ����һ��NH3��ǿ��ԭ�����ܽ�ijЩ���������ﻹԭΪ�������ʻ�ͼ�̬��������磺 �������������� 2NH3+3CuO  3Cu+N2+3H2O 3Cu+N2+3H2O���϶���Cu+��������Һ�в��ȶ�,�ɷ�������������ԭ��Ӧ����Cu2+��Cu�� ��������Cu2O��2H+��Cu2+��Cu��H2O  ��ش��������⣺ ��1����ʵ�������ѧϰС�����������ȡ�������ﰱ���ķ��������ס����е���ѷ����������������� A�������Ȼ�粒��壬��ͨ����ʯ�� B����N2��H2�Ļ�������������ú����������500�棬��ͨ����ʯ�� C������Ũ��ˮ����ͨ����ʯ�� D������ʯ���м���Ũ��ˮ����ͨ��Ũ���� ��2��Ϊ֤��NH3��ԭCuO�ķ�Ӧ����H2O���ɣ�B��Ӧ������Լ������������� ������ ��3�����۲쵽��������������������������������������������A�еķ�Ӧ�Ѿ���ɡ� ��4����С�����������Ϊ1:4��ϡ�������Լ������鷴Ӧ�Ƿ���Cu2O�������ɡ�����98%Ũ��������1:4��ϡ���ᣬ����IJ����������˽�ͷ�ι���������������������������� ��������֤����ԭ�����к���Cu2O������������������������������������������������������ ��5����д��A������Cu2O�Ļ�ѧ����ʽ�������������������������������������������� �� ��6�����������ķ����ⶨ�÷�Ӧ�Ƿ�����Cu2O��������ȷ�ķ��������������������������������� �� |
|||
�� |
��1��C ��2����ˮ����ͭ ��3��A�й����ɺ�ɫ��ȫ��Ϊ��ɫ����C�е��ܿ����������ݳ�����C���Թܵ�Һ�治���½� ���������һ�����ɣ� ��4���ձ�����Ͳ����������д��һ����1�֣���д��1�֣� �����������Һ����ɫ ��5��2NH3+6CuO  3Cu2O+N2+3H2O 3Cu2O+N2+3H2O��6��������Ӧǰ��װ��A�й�������� |
|||
| ��� | 15 |
|
||
���� |
1992ȫ���߿� | |||
| ��� | ij����Һ�п��ܺ���Fe2+��Fe3+��Ag+��Al3+��Ba2+��Ca2+��NH4+�����ӣ���������ʵ�飨�����ᡢ���ˮ����ˮ���ǹ����ģ���  ����ʵ����: (1)�ж�����Һ������Ba2+��Ca2+����,��д������.��:������������������ . (2)д������D�ķ���ʽ:���������������������� .�� (3)д������ҺD���ɳ���E�ķ�Ӧ�����ӷ���ʽ:���������������������� . |
|||
�� |
(1)����Ba2+��Ca2+�����е�һ�ֻ�����,��ΪBaSO4������ˮ,CaSO4����ˮ (2)Fe(OH)3 2AlO2����CO2��3H2O��2Al(OH)3��CO32�� ����AlO2����CO2��H2O��Al(OH)3��HCO3���� |
|||
| ��� | 16 |
|
||
���� |
1996ȫ���߿� | |||
| ��� | ij��Һ����NH4+��Mg2+��Fe2+��Al3+��������,�������м������������������Һ,�Ȳ�����,�ټ����������,��Һ�д������ٵ��������� ��A��NH4+�� ������ B��Mg2+�� ���� C��Fe2+ ������ ��������D��Al3+ |
|||
�� |
A��C | |||
| ��� | 17 |
|
||
���� |
2001�㶫�߿� | |||
| ��� | �����£�����A��B��C�ֱ�Ϊ���塢����ɫ���塢��ɫ���壬�ں��ʷ�Ӧ�����£����ǿ���ͼ2���з�Ӧ����֪E��Һ����ɫ�ģ���ش� ͼ2 ����Ӧ���� ��1��A���������� ��B�������� �ǡ�C�� �����������������ѧʽ���� ��2����Ӧ�ٵĻ�ѧ����ʽΪ������������������������������������ �������������������������������������� ��3����Ӧ�۵Ļ�ѧ����ʽΪ���������������������������������������������������������������������� ���� ��4����Ӧ�ܵĻ�ѧ����ʽΪ���������������������������������������������������������������������� ���� ���� |
|||
�� |
��1��Fe Cl2 H2 ��2��2Fe��3Cl2  2FeCl3 2FeCl3��3��2HCl��Fe��FeCl2��H2�� ��4��2FeCl2��Cl2��2FeCl3 |
|||
| ��� | 18 |
|
||
���� |
2005Ȫ��ģ�� | |||
| ��� | ��֪A��B��C��D��L���ǵ��ʣ�����B��LΪ���壬E��F����Ư�����á�����֮���ת����ϵ����ͼ��ʾ�� ��ش��������⣺  ��1��E�к��У����������������� Ԫ�أ�G�Ļ�ѧʽ�ǣ����������������������� ��2��д��D��I��Һ��Ӧ�Ļ�ѧ����ʽ�������������������������������������������������������������������� ��3��д��F�ĵ���ʽ���������������������� ����1 mol F������ˮ��Ӧ��ת�Ƶĵ���Ϊ���������� mol ��4��д��Kת��ΪJ�����ӷ���ʽ:���������������������������������������������������������������������������������� |
|||
�� |
��1��S��O��SO3 ��2��2Al + 2NaOH + 2H2O �� 2NaAlO2 + 3H2�� ��3��  ��1 ��1��4��AlO2�� + 4H+ �� Al3+ + 2H2O |
|||
| ��� | 19 |
|
||
���� |
2007Ȫ��ģ�� | |||
| ��� | ��ѧ��ѧ�м��ֳ������ʵ�ת����ϵ����ͼ���в��ֲ���δ��������A��һ�ֽ������ʣ�D��һ�ַǽ������嵥�ʡ� �ش��������⣺ ��1��A��������������������G������������������ ��2����д������B�������ӵ�ʵ�鷽�������� ��3�������������£��پٳ���ʹBת��ΪC�Ķ����Լ��������������������������������������� ��4��д����ӦC��A����B�����ӷ���ʽ�� ��5��д����ӦE��H2O2����F�Ļ�ѧ����ʽ�� |
|||
�� |
��1��Fe��FeS ��2��ȡ����B��Һ���μ�KSCN��Һ����죬�ٵμ���ˮ����Һ���ɫ�� ��3��KMnO4��Cl2�ȣ�ֻҪ�����͵÷� ��4��2Fe3+��Fe��3Fe2+ ��5��SO2��H2O2��H2SO4 |
|||
| ��� | 20 |
|
||
���� |
2006Ȫ�ݸ��� | |||
| ��� | ij��ѧ̽��ѧϰС���������ͼװ�ý��а����Ĵ�����ʵ�飬���������ɵ�NO����ͼ�еļгֺͼ�������������ȥ��  �� �� ��С�齫�ȼ���A����װ���еĿ������ϸɾ����ٽ���E���м�������ʵ�顣��ش��������⣺ ��1����С������NH4HCO3��ȡNH3���壬����ͬʱ�����������������ʶ���������ʵ�����Ʊ�NH3���塣���и�������ʵ�����Ʊ�NH3����������������������� ���ٹ�̬�Ȼ������ʯ�һ�ϼ��ȡ��ڹ�̬�Ȼ�識��ȷֽ� ����ʯ�ҵμ�Ũ��ˮ���������������Ȼ��������������Һ���� ��2��Bװ����ʢ�ŵ��������������������������������������������������������������������� ��3��װ��C�з�����Ӧ�Ļ�ѧ����ʽ������������������������������������������������������������������������ �� ��4��װ��D��Ũ��������������������������������������������������������������������������������������� ���û�ѧ����ʽ��ʾ���� ��5����֤�����Ĵ���������NO�������� �������������������������������� ��6��Dװ�ò�����������ɵĺ���� ���������������������������� |
|||
�� |
��1�� �٢� ��2�� ��ʯ�� ��3��4NH3+5O2  4NO+6H2O 4NO+6H2O ��4��NH3+H2SO4===(NH4)2SO4 ��5���Թ�E�к���ɫ�������� ��6��Ũ���ᵹ������C�ܡ� |
|||
| ��� | 21 |
|
||
���� |
2005������� | |||
| ��� | A��B��Ϊ���ε�ˮ��Һ��A�����ԣ�B�ʼ��Բ����������ԡ�����Ϊ���ʵ�鲽���ʵ������  ��ش� ����1��д��A��B��C�Ļ�ѧʽ��A���������������������� ��B������������������ ��C�������������������� �� ����2������д��A��D��D��E��E�к���ij��5��Ԫ�صĺ���������ӣ������ӷ���ʽ�� ���������������������������������������������������������� ���������������������������������������������������������������������� �� ����3��д����SO2����ͨ��K��Һ�з�����Ӧ�����ӷ���ʽ�������������������������������������������� ����4��д����F��H�Ļ�ѧ����ʽ���������������������������������������������������������������������������������������� �� |
|||
�� |
��1��NaI
NaClO AgI ��2��2I����ClO����H2O��I2��Cl����OH�� I2��5ClO����2OH����2IO3����5Cl����H2O ��3��Fe3����SO32����2H2O��Fe2����SO42����4H�� ��4��Cl2��2NaOH��NaClO��NaCl��H2O |
|||
| ��� | 22 |
|
||||||
���� |
2009�㶫�߿� | |||||||
| ��� | ijʵ��С����������װ�ã����̶ֹ�װ���ԣ��Ʊ������ƣ�Ca3N2������̽����ʵ��ʽ��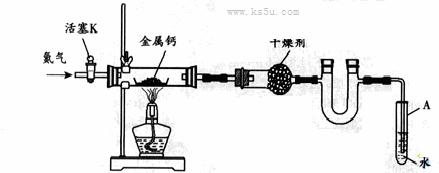 ��1����ͼ���Ӻ�ʵ��װ�á����װ�õ������ԣ����������������������������� �� ��2����Ӧ������ĩ�˵��ܱ�������Թ�A��ˮ�У�Ŀ���� �������������������� ��3���Ʊ������ƵIJ��������ǣ��ٴ���K��ͨ��N2���ڵ�ȼ�ƾ��ƣ����з�Ӧ���۷�Ӧ���������������� ���������ܲ��װ�ã�ȡ����� ��4�����ݼ�¼���£�
����ͨ���N2�л�������O2����Ƚ�x��3�Ĵ�С���������ж����ݣ��������������������� �� |
|||||||
�� |
(1)�رջ���K����Ӳ�ʲ����ܣ���A���������ݳ�������ȴ��A�е����γ�ˮ����˵�����������á� ��2����ֹ��������Ӳ�ʲ���������Ca��Ӧ�� ��3������ͨ��N2������ȴ�����¡� ��4����2.8 ��x<3��O2��Ca��Ӧ����CaO��Ca������������Ca3N2��С��ʹ������ƫС�� |
|||||||
| ��� | 23 |
|
||
���� |
2005���ݲ��� | |||
| ��� | ��.�ϳɰ���ҵ�Ի�ѧ������ҵ������Ҫ�����塣д������������Ҫ��; ���������������� ���������������������������������������������������������� ��.ʵ�����Ʊ����������з���������ѡ�õ��� �����������������������������������������ţ� �� �����Ȼ�識��ȷֽ� �� �������������еμ�Ũ��ˮ �� �Ȼ����Һ������������Һ���� �� ��̬�Ȼ�����������ƻ�ϼ��� ��.Ϊ����ʵ�������ù�ҵԭ���Ʊ������������������������װ�ã�ͼ�мг�װ�þ�����ȥ��  ʵ������� ʵ��������� ���ʵ��װ�õ������Ժرյ��ɼ�a��b��c��d��e����A�м���п������©��ע��һ����ϡ���ᡣ���ɼ�c��d��e����A����������������F���ڴ��ռ������������䴿�ȡ� �� �رյ��ɼ�c��ȡ�½�ȥ�ײ���ϸ��ƿC�����ɼ�a��������������B�鴿���ȼ��Ȼ������������ϸ��ƿC��������������ͼ��ʾ������������ƿ��ȼ�գ������Ӻ����Ϩ�� �� �þƾ��Ƽ��ȷ�Ӧ��E������ͨ����������ϸ��ƿC��ˮλ�½���Һ�汣�ֲ���ʱ�����ɼ�b����ϸ��ƿC�����徭D���뷴Ӧ��E��Ƭ�̺�F�е���Һ��졣 ��ش��������⣺ ��1�������������ȵ�Ŀ���� ���������������������������������������������������������������������������������������� ��2��Cƿ��ˮλ�½���Һ�汣�ֲ���ʱ��Aװ���ڷ����������������������������������������� ������ֹ��ʵ��װ����ѹǿ����ʱ�ٴ��ɼ�b��ԭ���������������������������������������������������� ����Cƿ������ijɷ��� �������������������������������������� ��3���ڲ�����У��ȼ�������ý��ԭ�������������������������������������� ���������������������� ��Ӧ��E�з�����Ӧ�Ļ�ѧ����ʽ�� �������������������������������������������������������������� |
|||
�� |
��.�ƻ��ʡ������� ��. �ڢ� ��.��1���ų���������֤��ȫ ��2��п���������� ��������������Ũ������ߵ�����ת���ʣ� N2��H2 ��3������ý�ڽϸ��¶�ʱ�������ӿ찱�ϳɵķ�Ӧ���� N2 + 3H2  2NH3 2NH3 |
|||
| ��� | 24 |
|
||
���� |
2010�����߿� | |||
| ��� | ��ҵ�ϳ�����������ʢװ��Ũ�ᡣΪ�о����ʲ�������Ũ����ķ�Ӧ��ijѧϰС�����������̽����� [̽��һ] ��1������ȥ�������������������̼�ظ֣�������Ũ�����У�10���Ӻ���������ͭ��Һ�У�Ƭ�̺�ȡ���۲죬�������������Ա仯����ԭ�������������������� �� ��2������ȡ����6.0g����15.0ml.Ũ�����У����ȣ����Ӧ��õ���ҺX���ռ�������Y�� �ټ�ͬѧ��ΪX�г�Fe3+����ܺ���Fe2+����Ҫȷ�����е�Fe2+��Ӧ���������������������� ѡ����ţ��� a��KSCN��Һ����ˮ������ b�����ۺ�KSCN��Һ�������� c.��Ũ��ˮ������ d������KMnO4��Һ ����ͬѧȡ336ml����״��������Yͨ��������ˮ�У�������Ӧ�� SO2+Br2+2H2O��2HBr+H2SO4 Ȼ���������BaCl2��Һ�����ʵ�������ø������2.33g�����ڴ���֪����Y��SO2���������Ϊ������������������������ �� [̽����] ��������ʵ����SO2��������Ľ������ͬѧ��Ϊ����Y�л����ܺ�����H2��Q���塣Ϊ�����������̽��ʵ��״�ã�ͼ�мг�����ʡ�ԣ���  ��3��װ��B���Լ������������������������������� �� ��4����Ϊ����Y�л�����Q������������������������������ ���û�ѧ����ʽ��ʾ���� ��5��Ϊȷ��Q�Ĵ��ڣ�����װ��������M�������������������������� ��ѡ����ţ��� �� a. A֮ǰ���������� b.A��B�䡡���������� c.B��C�䡡���������� d.C��D�� ��6���������Y�к���H2��Ԥ��ʵ������Ӧ������������������������ �� ��7����Ҫ�ⶨ���������Y��H2�ĺ�������״����Լ��28ml H2���������ò���H2����ķ����⣬�ɷ�ѡ�����������ķ����������жϲ�˵�������������������������������� �� |
|||
�� |
��1���������汻�ۻ��������������𰸣� ��2����d ��66.7%�������������𰸣� ��3������SO2�Ƿ���� ��4��C��H2SO4(Ũ)  CO2����SO2����2H2O CO2����SO2����2H2O��5��c ��6��D�й����ɺڱ���E�й����ɰױ��� ��7������������ƽ������D��E�IJ��������÷�����ƽ����D��E�IJ��� |
|||
| ��� | 25 |
|
||
���� |
1997�Ϻ��߿� | |||
| ��� | Ϊ�ⶨһ�ָ��������↑֧�Ĵ��Է�ĩ���ϵ���ɣ���ȡ12.52����Ʒ������ȫ�����ڹ���ϡ��������100������Һ��ȡ��һ�룬�������K2SO4��Һ�����ɰ�ɫ�����������ˡ�ϴ�ӡ���ɺ��4.66�˹��塣�����µ�50������Һ�м�������KSCN��Һ���Ժ�ɫ������������NaOH��Һ�������ɺ��ɫ���������������ˡ�ϴ�ӡ����պ��3.20�˹��塣��1��������Է�ĩ��������Ԫ�ص������ٷֺ�������2��ȷ���ò��ϵĻ�ѧʽ |
|||
�� |
��1����������Ϊ5.48�ˣ���4.48�ˣ���Ϊ20.45% ��2��ԭ�Ӹ�����ΪBa��Fe��O=1��2��4����ѧʽΪBaFe2O4����BaO��Fe2O3�� |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |