 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| ��� | |
|---|---|
| �����������⣺45 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2009�����ʼ� | |||
| ��� | ���������缫����KOH��Һ�У��������ֱ�ͨ��CH4��O2�����ɼ���ȼ�ϵ�ء���֪��ͨ��CH4��һ������缫��Ӧʽ�ǣ�CH4 + 10OH-�� - 8e-��CO32-+7 H2O��ͨ���2����һ������缫��Ӧʽ�ǣ�2O2 + 4H2O + 8e- = 8OH-��������������ȷ���� ��A��ͨ��CH4�ĵ缫Ϊ���� ��B����������������Ӧ ��C��ȼ�ϵ�ع���ʱ����Һ�е�OH-���ƶ� ��D���õ��ʹ��һ��ʱ���Ӧ����KOH |
|||
�� |
B | |||
| ��� | 2 |
|
||
���� |
2009����߿� | |||
| ��� | ������A�����ڲ�ͬ�Ķ�����Ԫ��X��Y��ɣ������õ����ȳ�����ϡ� ��1��X�ĵ��ʼȿ������ᷴӦ���ֿ���NaOH��Һ��Ӧ��X��ԭ�ӽṹʾ��ͼΪ������������������������ ��2��X����������Һ�����NaOH��Һ��Ӧ�����ӷ���ʽΪ������������������������������������ ��3��һ�������£�A��ˮ�����������ɺ�Y�Ļ�����Z��Z���Ӻ���10�����ӡ� ��Z��H2O2��Ӧ�������֮һ��Y�ĵ��ʣ�Y�ĵ��ʵص���ʽΪ�������������������������� ��Z���ӵĽṹ�������������������������� ��A�Ļ�ѧʽ���������������������������� ��4��X�ĵ��ʡ�ʯī�Ͷ�������(TiO2)��������ϣ������·�Ӧ�õ��Ļ������������Ԫ����ɣ��Ҷ��������մɲ��ϣ��ڻ���ӵ���������ҪӦ�ã����䷴Ӧ�Ļ�ѧ����ʽ������������������������������������������ |
|||
�� |
��1�� ��2��Al3++4OH��=AlO2��+2H2O ��3����  �������� ����������AlN ��4Al+3tiO2+ 3C  Al2O3+3TiC Al2O3+3TiC |
|||
| ��� | 3 |
|
||
���� |
2009ȫ������ | |||
| ��� | ��֪���·�У�������ͭ����a�����й���ͼ��ʾ��װ�÷���������һ���� �� ����A����װ����Cu��Ϊ���� ��B����ͭ���������仯Ϊ12 .8gʱ��a�������ĵ�O2�ڱ�״���µ����Ϊ2.24L ��C��b����Ӧ�ĵ缫��ӦʽΪ��H2��2e��=2H+ ��D��һ��ʱ���пƬ�������� |
|||
�� |
B���·�е�����ͭ����a����˵��CuΪ����ZnΪ������aΪ������bΪ����;b_����Ӧ�ĵ缫��ӦʽΪ��2H2һ4eһʮ4OH��=4H2O��пƬ���������䡣 |
|||
| ��� | 4 |
|
||
���� |
2009����ͳ�� | |||
| ��� | �۲����м���װ��ʾ��ͼ���й�������ȷ���� ��A��װ�â���������������ɫ���� ��B��װ�âڵĴ�������ƷӦ���Դ�������� ��C��װ�â��бպϵ�������·������a������b�� ��D��װ�âܵ����ӽ���Ĥ���������ӡ������ӡ�ˮ��������ͨ�� 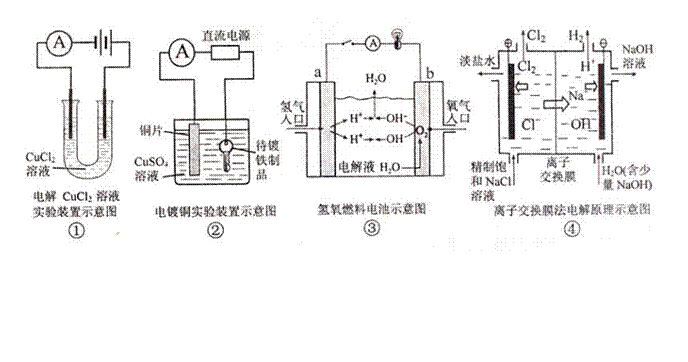 |
|||
�� |
C | |||
| ��� | 5 |
|
||
���� |
2009ɽ����� | |||
| ��� | ����������ȼ�ϵ�ص���±ˮ����C1����Br����Na+��Mg2+����װ������ͼ��ʾ��a��bΪʯī�缫���� ����˵���У���ȷ���� ��A����ع���ʱ��������ӦʽΪ��O2+2H2O+4e��=4OH�� ��B�����ʱ��a�缫��Χ���ȷŵ����Brһ������C1��˵��������������ͬʱǰ�ߵĻ�ԭ��ǿ�ں��ߡ� ��C�����ʱ������������·���ǣ����������·����������Һ������������ ��D������������ģ������������ 0.02gH2ʱ��a����Χ�����0.71gCl2 |
|||
�� |
B | |||
| ��� | 6 |
|
||
���� |
2009Ϋ��ģ�� | |||
| ��� | ����˵����ȷ���� ��A������������Ʒ�ĶƲ�����ʱ���Ʋ����ܶ�����Ʒ��ͬ���ı������� ��B����⾫��ͭʱ����ͬʱ������������ͭ�������������ܽ�ͭ�������� ��C��ϡ���ᡢŨ������ܽ�ľ̿�����ɶ�����̼�� �� D����ҵ�ϣ��뵼����Ϲ��Ӧ�÷dz��㷺�����Ʊ����̲��漰������ԭ��Ӧ |
|||
�� |
B | |||
| ��� | 7 |
|
||
���� |
2006�������� | |||
| ��� | �����������ض�����Ҫ�Ĺ�ҵ��Ʒ����ش� ��1����ҵұ�����Ļ�ѧ����ʽ���������������������������������������������� �� ��2����������������Һ��Ӧ�����ӷ���ʽ�������������������������������������������� �� ��3����ҵƷ�������ص���Һ�к���ijЩ����������ʣ��������ӽ���Ĥ������ᴿ�� ������װ�������ӽ���Ĥ��ֻ����������ͨ�������乤��ԭ����ͼ��ʾ��  �ٸõ��۵�������Ӧʽ�������������� ���������������� ��ͨ�翪ʼ������������ҺpH�����������ԭ������������������������������ ���������������������������������������� �۳�ȥ���ʺ������������Һ��Һ�����_______����д��A����B���������� |
|||
�� |
��1��2Al2O3  4Al��3O2�� 4Al��3O2����2��2Al��2OH����2H2O��2AlO2����3H2�� ��3����4OH����4e����2H2O��O2�� ��H���ŵ磬�ٽ�ˮ�ĵ��룬OH��Ũ������ ��B |
|||
| ��� | 8 |
|
||
���� |
2008���dz��� | |||
| ��� | ��ͼΪ�����ӽ���Ĥ����ⱥ��ʳ��ˮԭ��ʾ��ͼ�� ����˵������ȷ���� ��A����E���ݳ���������H2�� ��B����B�ڼ��뺬����NaOH��ˮ��Һ����ǿ������ ��C����״����ÿ����22.4 LCl2�������2 mol NaOH ��D������ˮ�к�Ca2+��Mg2+��Fe3+��SO42�������ӣ�����ʱ�ȼ�Na2CO3��Һ |
|||
�� |
D | |||
| ��� | 9 |
|
||
���� |
2008ȫ��I�� | |||
| ��� | ���100mL��c��H+����0.30mol/L��������Һ������·��ͨ��0.04mol����ʱ�������������������������� ��A��0.10mol/LAg+�������������������������������������������������������������� B��0.02mol/L Zn2+ ��C��0.20mol/L Cu2+������������������������������������������������������������ D��0.20mol/L Pb2+ |
|||
�� |
C | |||
| ��� | 10 |
|
||
���� |
2009��ƽ�ʼ� | |||
| ��� | ��ͼ�У����缫�Ϸ����ĵ缫��ӦΪ��a����Cu2++2e��=Cu���� b����Fe��2eһ=Fe2+������˵��������ȷ���� ��A����װ�ÿ����ǵ��ء� ��B��a���Ϸ������ǻ�ԭ��Ӧ ��C��a��b������ͬ�ֵ缫���� ��D����װ���ڹ���ʱ����Һ�е������ӿ�����b���ƶ�  |
|||
�� |
D | |||
| ��� | 11 |
|
||
���� |
2008Ȫ��ģ�� | |||
| ��� | ��ͼa��װ�ý���ʵ�飬��ͼb��X���ʾ����缫�ĵ��ӵ�������Y����ܱ�ʾ������� �� A��c(Ag+)�������������� B��c(NO3��)������ �� C����Һ��pH������D����������  |
|||
�� |
D | |||
| ��� | 12 |
|
||
���� |
2009ɽ���߿� | |||
| ��� | Zn-MnO2�ɵ��Ӧ�ù㷺����������Һ��ZnCl2-NH4Cl�����Һ�� ��1���õ�صĸ���������������������ع���ʱ������������������������������������� ��2����ZnCl2��NH4Cl�����Һ�к�������Cu2+�������ij�缫�ĸ�ʴ.����Ҫԭ������������������ȥCu2+,���ѡ�������Լ��е���������������ţ��� a.NaOH���� b.Zn��������c.Fe������ ������d.NH3��H2O ��3��MnO2����������֮һ����ʯīΪ�缫������ữ��MnSO4��Һ�������ĵ缫��Ӧʽ������������������·��ͨ��2mol���ӣ�MnO2�����۲���Ϊ���������� |
|||
�� |
��1��Zn����п�� ���� ��2��п�뻹ԭ����ͭ����ͭпԭ��ض��ӿ�п�ĸ�ʴ b ��3��2H++2e-==H2�� 87 |
|||
| ��� | 13 |
|
||
���� |
2009����һ�� | |||
| ��� | ��ͼ, X��Y��Ϊ�缫ʯī�� ��I�������ҺΪ���з�̪�ı���ʳ��ˮ����ⷴӦ�����ӷ���ʽΪ�������� ����������������������������������ֺ�ɫ�� ��II�������ҺΪ500mL��A���ʵ�ij��ɫ��Һ�����һ��ʱ�䣬�۲쵽X�缫�����к�ɫ�Ĺ�̬�������ɣ�Y�缫����ɫ�������ɣ���Һ��ԭ��������ȫ����ֹͣ��⣬ȡ��X�缫��ϴ�ӡ�����������缫����1.6g�� ��1��������Һ��pHΪ��������Ҫʹ������Һ�ָ������ǰ��״̬�������һ�������������������� ����������ʵĻ�ѧʽ������������ǰ����Һ��������䣩 ��2�������Ʋ�ԭ��Һ��������������ӿ��������������� �������ʵ����֤����Ʋ⣬д��ʵ��IJ������衢����ͽ��ۣ����������������� |
|||
�� |
��I��2Cl��+ 2H2O == 2OH��+Cl2��+H2���������� ��II����1��1�� CuO��CuCO3 (����1�ּ���) ��2����������ӣ�ȡ��������Һ���Թ��У��μ����������������������Ȼ�����Һ���а�ɫ������������֤����������ӡ� [����������ӣ�ȡ��������Һ���Թ��У�����Ũ����μ�Ũ�����ͭ�����к���ɫ�����������֤�����������] |
|||
| ��� | 14 |
|
||
���� |
2009���ݵ��� | |||
| ��� | ��Ƶȹ�ҵ��ˮ�г����о綾���°���Cr2O72�����÷�ˮ������һ�ַ����ǣ����û�ԭ����Cr2O72����ԭ�ɶ��Խϵ͵�Cr3+���ټӼ����ɳ�������һ�ַ����ǣ����ˮ�м����ʵ���NaCl����Fe���缫���е�⡣����˵���������ǣ� ��A�����ʱ��������ӦΪ��Fe��2e����Fe2�������� ��B���������������ܲ������� ��C����ⷨ�У�ת��Cr2O72�������ӷ���ʽΪ��Cr2O72����6Fe2����14H����2Cr3����6Fe3����7H2O ��D���������У�������������Fe(OH)3��Cr(OH)3���� |
|||
�� |
D | |||
| ��� | 15 |
|
||
���� |
2009���ո߿� | |||
| ��� | Cu2O��һ�ְ뵼����ϣ�������ɫ��ѧ������Ƶ���ȡ.Cu2O�ĵ���ʾ��ͼ���£�����ܷ�Ӧ��2Cu+H2O==Cu2O+H2��������˵����ȷ���� ��A��ʯī�缫�ϲ������� ��B��ͭ�缫������ԭ��Ӧ ��C��ͭ�缫��ֱ����Դ�ĸ��� ��D������0.1mol����ת��ʱ����0.1molCu2O���ɡ�  |
|||
�� |
A | |||
| ��� | 16 |
|
||
���� |
2009�㶫�ῼ | |||
| ��� | �õ�Ʒ������Ƽ��������һ��ͭ������������ȷ���� ��A.�����Ƽ������������� ������������B�������Ƽ������� ��C����Na2S04��Һ�����Һ���� ����D����K2S04��Һ�����Һ |
|||
�� |
B | |||
| ��� | 17 |
|
||
���� |
2007����һ�� | |||
| ��� | һ�����͵�ȼ�ϵ�أ����Զ������Ϊ�缫����KOH��Һ�У�Ȼ��ֱ�������ͨ��������������йش˵�ص��ƶ���ȷ���� ��A.������ӦΪ14H2O��7O2��28e����28OH�� ��B.�ŵ�һ��ʱ�������Χ��pH���� ��C.ÿ����1mol C2H6�����·��ת�Ƶĵ���Ϊ14mol ��D.�ŵ������KOH�����ʵ���Ũ�Ȳ��� |
|||
�� |
C | |||
| ��� | 18 |
|
||
���� |
2008���ĸ߿� | |||
| ��� | һ��ȼ�ϵ���з����Ļ�ѧ��ӦΪ����������Һ�м״�������������ˮ�Ͷ�����̼�� ���õ�ظ��������ķ�Ӧ�� ��A.CH3OH(g)+O2(g)=H2O(1)+CO2(g)+2H��(aq)+2e�� ��B.O2(g)+4H+(aq)+4e_=2H2O(1) ��C.CH3OH(g)+H2O(1)=CO2(g)+6H��(aq)+6e�� ��D.O2(g)+2H2O(1)+4e��=4OH�� |
|||
�� |
C | |||
| ��� | 19 |
|
||
���� |
2007�������һ | |||
| ��� | �ö��Ե缫���һ��Ũ�ȵ�����ͭ��Һ����ʱ��ͨ�����������Һ�м���0.2mol Cu(OH)2��ǡ�ûָ������ǰ��Ũ�Ⱥ�pH�����������ת�Ƶ��ӵ������ʵ���Ϊ ��A��0.2mol������������������������������ B��0.4mol������������������������������ C��0.6mol������������������������������ D��0.8mol |
|||
�� |
D | |||
| ��� | 20 |
|
||
���� |
2009������ĩ | |||
| ��� | ij�¶�ʱ���ö��Ե缫��������ƵIJ�������Һ�����������ռ������������Ϊ22.4aLʱ��ʣ����Һ�ָ���ԭ�¶ȣ���������mg���������ռ������������Ϊ33.6aLʱ��ʣ����Һ�ָ���ԭ�¶ȣ���������ng�����������ڸ��¶�ʱ���ܽ���ǣ�������������ۺ�Ϊ��״���µ������ ��A��  ������������ B�� ������������ B�� ��C��  ������������ D�� ������������ D�� |
|||
�� |
C | |||
| ��� | 21 |
|
||
���� |
2008�ɶ����� | |||
| ��� | ������A��B��C��D��E�ֱ���H+��Na+��Al3+��Cu2+���������Ӻ�CO32����Br����SiO32����SO42����������������ɡ�����֪����A��B��C������ҺpH<7��D��E��ҺpH>7�� ��A��C����������ͬ��D��E����������ͬ�� ����ʯī�缫���A����Һ����������ɫ��������������к�ɫ�������ɡ� ��C��Һ��D��Һ��Ӧ������һ�ְ�ɫ������һ�����壬�Ҵ˳���������B����Һ��������ͨ��E����Һ�пɲ�����һ�ְ�ɫ������ �����������ʵ��գ� ������1��д��B��C��E�Ļ�ѧʽ��B___________��C___________��E____________�� ������2��D��Һ��pH>7��ԭ���ǣ�_________________________________________�� ������3��д��C��Һ��D��Һ������Ӧ�����ӷ���ʽ��_______________________�� ������4������ʯī�缫���400mL��1.0 mo1��L��1A����Һ����������2.24 L���壨��״��������ʱ����Һ��pH��_______________������Һ��������䣩�� |
|||
�� |
��1��HBr Al2(SO4)3Na2SiO3 ��2����ΪCO32������ˮ�������H+�������HCO3�����ٽ���ˮ�ĵ��룬ʹ��Һ�е�c��OH��������������ҺpH>7 ��3��2Al3++CO32��+3H2O=2Al(OH)3��+3H2O�� ��4��0 |
|||
| ��� | 22 |
|
||
���� |
2008�Ϻ��߿� | |||
| ��� | ȡһ���ñ���NaCl��Һ��ʪ��pH��ֽ������Ǧ��о���缫����ֱͨ����Դ��һ��ʱ�����a�缫����ֽ�Ӵ�������һ��˫ɫͬ��Բ����ԲΪ��ɫ����Բ��dz��ɫ��������˵��������� ��A��b�缫������ ��B��a�缫���Դ������������ ��C���������У�ˮ�������� ��D��b�缫������Һ��pH��С  |
|||
�� |
D | |||
| ��� | 23 |
|
||
���� |
2007����һ�� | |||
| ��� | ������ͼ��ʾװ�õ���������ȷ����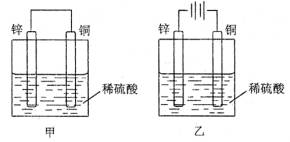 ��A������װ����пƬ�������� ��B������װ���У���Һ�ڵ���������ͭƬ���汻��ԭ ��C������װ���У�пƬ�Ϸ����ķ�Ӧ���ǻ�ԭ��Ӧ ��D����װ���У�ͭ�������������ɣ���װ����ͭƬ�������� |
|||
�� |
D | |||
| ��� | 24 |
|
||
���� |
2004ȫ����� | |||
| ��� |  �ڲ���ԲͲ��ʢ��������ɫ�Ļ������ܵ�����Һ�塣�ϲ�Һ���в�������ʯī�缫��ԲͲ�ڻ�����һ���¶���ɻ�״�IJ����������������½���Һ�壬װ������ͼ����ͨ��Դ��������Χ��Һ�������ɫ������ɫ��dz������������������ɡ�ֹͣͨ�磬ȡ���缫���ý������¾��ҽ��������ú�Һ���ֳַ����㣬�²�Һ����Ϻ�ɫ���ϲ�Һ�弸����ɫ����������ʵ��ش� ��1�������ϵĵ缫��ӦʽΪ_____________________�� ��2�������ϵĵ缫��ӦʽΪ_____________________�� ��3��ԭ�ϲ�Һ����_____________________________�� ��4��ԭ�²�Һ����______________________________�� ��5�����������Һ����ɫ�����仯��ԭ����________ �������� �������������������������������������������������������������������������������������������������������������������������������������� ��6��Ҫ�����ϲ�Һ���к��еĽ������ӣ��䷽����_____________________________�� ��������������_____________________________________________________________���� _____________________________________________________________________�� |
|||
�� |
��1��2I����2e����I2
��2��2H����2e����H2�� ��3��KI����NaI�ȣ�ˮ��Һ ��4��CCl4����CHCl3�ȣ� ��5��I2��CCl4�е��ܽ�ȴ�����ˮ���ܽ�ȣ����Ծ���I2��ת�Ƶ�CCl4�� ��6����ɫ��Ӧ ����ɫ�ܲ����۲�������ɫ������������ͬ�����֡����磬�����д�NaIˮ��Һ����������ʻ�ɫ���� |
|||
| ��� | 25 |
|
||
���� |
2005Ȫ��ģ�� | |||
| ��� | ijѧ����X��Y��װ�ã�����ͼ������ͭ�ĵ�⾫��ʵ�飨��ͭ����п���������������ʣ�������˵����ȷ���ǡ��� ��A��aӦ��c�����ӣ�bӦ��d������ ��B�����һ��ʱ�䣬b��d�����������ʵ����ʵ������ ��C�����һ��ʱ�䣬b��������Һ��pH���� ��D���������У�Yװ����Cu2+��Ũ��ʼ�ղ���  |
|||
�� |
B | |||
| ��� | 26 |
|
||
���� |
2005����Ѻ�� | |||
| ��� | ��ͼ��ʾ������ʵ��װ���У���Һ�������Ϊ200mL����ʼʱ�������Һ��Ũ�Ⱦ�Ϊ0.1mol/L������һ��ʱ���õ����о�ͨ��0.01mol���ӣ����������ε�ˮ�����Һ����ı仯����������������ȷ���� ��A.�ұߵ缫���������ʵ��������٣��� ��B.�����ϲ��������������٣��� ��C.��Һ��pH�仯�������ڼ�С ��D.�缫��Ӧʽ����������4OH-��-4e-��2H2O��O2�����и�����2H����2e-��H2�� |
|||
�� |
B | |||
| ��� | 27 |
|
||
���� |
δ֪ | |||
| ��� | ���й���ʵ���������������ȷ���ǡ� ��A����ͭƬ����Ƭ������һ�����ϡ�����У�ͭƬ����������� ��B����пƬ����������Ƭ��������������Ȼ�п��Һ����Ƭ�������һ��п ��C����ͭƬ�������Ȼ�����Һ�У���ͭƬ�������һ���� ��D����п������ʢ��������Թ��У����뼸���Ȼ�ͭ��Һ�����ݷų����ʼӿ� |
|||
�� |
C | |||
| ��� | 28 |
|
||
���� |
δ֪ | |||
| ��� | ��пƬ����Ƭ����ʢ��ϡʳ��ˮ�ͷ�̪��Һ�����Һ�IJ������У���ͼ��ʾƽ��ͼ��������һ��ʱ������ȹ۲쵽��Һ���������� A����͢������������� B����͢����������� C����͢����������� D����͢�����  |
|||
�� |
B | |||
| ��� | 29 |
|
||
���� |
δ֪ | |||
| ��� | �мס��ҡ����������ֽ��������ס����õ�����������ϡ�����п��Կ����������ܽ⣬���ı����������ݳ����Ѷ��ŵ��ҵ���������Һ�к����渲��һ���ҵĵ��ʣ���ʯī�缫��⺬����ͬ���ʵ���Ũ�ȵļͱ����ֽ���������Һ�����ĵ�����������������ϡ��������H2��������֪���ֽ�������һ����ͭ����������ʵ���жϣ�ͭ�� ��A���ס��� B���ҡ��� C�������� D���� |
|||
�� |
C | |||
| ��� | 30 |
|
||
���� |
2005������У | |||
| ��� | ͼ����װ���У���Һ�����Ϊ200ml����ʼʱ���������Һ��Ũ�Ⱦ�Ϊ0.1mol��L-1������һ��ʱ���õ����϶�ͨ����0.02mole��������������Һ����ı仯��������������ȷ����  ��A����������������٣��� ��B���缫�����������������٣��� ��C���缫��Ӧʽ������������4OH�D�D4e����2H2O��O2�������и�����2H����2e����2H2�� ��D����Һ��pH�仯���ټ�С�������� |
|||
�� |
D | |||
| ��� | 31 |
|
||
���� |
2006����һ�� | |||
| ��� | ����ͼװ���У�b�缫�ý�����M�Ƴɣ�a��c��dΪʯī�缫����ͨ��Դ������M������b����ͬʱa��d�缫�ϲ������ݡ��Իش� ������ ������ (1)aΪ���������������������� ����c���ĵ缫��ӦʽΪ�������������������������������������������������������� �� (2)��ʼʱ����B�ձ������룬�μ��ε�����Һ�����ܹ۲쵽�������ǣ��������������������� ��������һ��ʱ�������c���ϵ��Թ���Ҳ�ռ��������壬��ʱc���ϵĵ缫��ӦΪ�������������������� (3)��d�����ռ���44.8mL���壨��״����ʱֹͣ��⣬a���Ϸų������������������� ����moL���壬��b�缫�ϳ�������M������Ϊ0��432g������˽�����Ħ������Ϊ������������������ �������� (4)���ֹͣ�������ˮʹA�ձ��е���Һ�����Ϊ200mL��ȡ������Һ���뵽�� 25��0mL0��100mol��L��1HCI��Һ�У�������31��25mL��Һʱ�պó�����ȫ���Լ��㣺���ǰA�ձ���MNO3��Һ�����ʵ���Ũ�ȡ��� |
|||
�� |
(1)����2I��һ2e����I2 (2)c����������Һ���ȱ�Ϊ��ɫ 40H����4e����2H2O+O2�� (3)0��001��108g��mol (4)0.1mol��L��1 |
|||
| ��� | 32 |
|
||
���� |
2009Ȫ���ʼ� | |||
| ��� | �Զ��Ե缫���NaCl��Һ��CuSO4��Һ���õ����ֲ���A��B��C��������֮���ת����ϵ����ͼ��ʾ��ͼ�в��뷴Ӧ�����ɵ�ˮ������ȥ������֪���Ƕ�����Ԫ�صĵ��ʣ������ճ������г��õİ�װ���ϡ� �ش��������⣺ ��1������Ԫ�����ڱ���λ�������������������������� ������ ��2����������NaCl��Һ�� ��A��B��Ӧ�����ӷ���ʽ������������������������������������������������ �� �������100mL0.1mol•L��1NaCl��Һ������������������112mL���壨��״��������������Һ��pHΪ���������������������Է�Ӧǰ����Һ������仯�� ��3����������CuSO4��Һ�� ��E�Ļ�ѧʽ�������������������� �����ʱ�����ĵ缫��Ӧʽ������������������������������������ �������� �ڼ���ʱ��A��Ũ��Һ����B������Ӧ��A��Ũ����ʱ��仯��ͼ����ȷ�������� ��  ������������A������������������������������������������������ B������������������������������������ C �������÷�ӦA��B��C����CuSO4+H2O���ѻ�ѧ��ת��Ϊ���ܣ�����Ƶ�صĸ����������������������� ����������Ԫ�ط��ţ��� |
|||
�� |
��1����3���ڵڢ�A�� ��2����Cl2��2OH��= Cl��+ClO��+H2O����13 ��3����SO2��4OH����4e����O2����H2O���� ��A��������Cu |
|||
| ��� | 33 |
|
||
���� |
2007����һ�� | |||
| ��� | ����ͼ��ʾװ�ã�����������ʢ�����з�̪��Һ��NaCl������Һ��C����C����Ϊ���ʯī�缫����ͨS1��C��������Һ��죬�������������������ɡ�һ��ʱ�������������Һ��δ����缫�����Ͽ�S1����ͨS2����������ָ�뷢��ƫת,˵����ʱ��װ���γ���ԭ��أ����ڸ�ԭ��ص�������ȷ���� ��A. C��I���ĵ缫���������� ��B��C��II���ĵ缫�����Ǹ��� ��C��C��I���ĵ缫��Ӧʽ��2H++2e��=H2�� ��D��C��II���ĵ缫��Ӧʽ��Cl2��2e����2Cl��  |
|||
�� |
D | |||
| ��� | 34 |
|
||
���� |
2002�㶫�߿� | |||
| ��� | ��ԭ��غ͵��صĵ缫���������ķ�Ӧ��ͬ��������Ӧ��ͬ����ԭ��Ӧ���� ��A��ԭ��ص������͵��ص������������ķ�Ӧ ��B��ԭ��ص������͵��ص������������ķ�Ӧ ��C��ԭ��صĸ����͵��ص������������ķ�Ӧ ��D��ԭ��صĸ����͵��ص������������ķ�Ӧ |
|||
�� |
BC | |||
| ��� | 35 |
|
||
���� |
2007�ɶ�һ�� | |||
| ��� | ����ͼ��ʾ��a��b�Ƕ��ʯī�缫��ijͬѧ��ͼװ�ý�������ʵ�飺�Ͽ�K2���պ�K1һ��ʱ�䣬�۲쵽��ֻ�������ڶ������ݽ��缫��Χ����ʱ�Ͽ�K1���պ�K2���۲쵽������A��ָ����ƫת������˵������ȷ���� ��A���Ͽ�K2���պ�K1ʱ��a���ϵĵ缫��ӦʽΪ��4OH��һ4e�� === O2��ʮ+2H2O ��B���Ͽ�K2���պ�K1һ��ʱ�䣬��Һ��pHҪ��� ��C���Ͽ�K1���պ�K2ʱ��b���ϵĵ缫��ӦʽΪ��2H++2e��=== H2�� ��D���Ͽ�K1���պ�K2ʱ��OH����b���ƶ�  |
|||
�� |
C | |||
| ��� | 36 |
|
||
���� |
2008Ȫ���ʼ� | |||
| ��� | ��ͼ�У����缫�Ϸ����ĵ缫��ӦΪ�� a����Cu2����2e����Cu�������������������� b����Fe��2e����Fe2�� ����˵������ȷ���� A��װ���е������Һһ������Cu2�� B����װ��һ���ǻ�ѧ��ת��Ϊ���� C��a��b������ͬ�ֵ缫���� D��a����һ��������ԭ��Ӧ  |
|||
�� |
B | |||
| ��� | 37 |
|
||
���� |
2009�����ʼ� | |||
| ��� | ������Ԫ��A��B��C��D��AԪ�ص�ԭ���������������ڲ��������������BΪ�ؿ��к�������Ԫ�أ�C��ԭ�Ӱ뾶���Ķ���������Ԫ�أ�C��D�γɵ����ӻ�����CD�dz��õĵ�ζƷ����д���пհף� ��1��A������B���ʷ�����Ӧ�IJ��������������������������������������������� �����ѧʽ�� ��2��B��C��ɵ�һ�ֻ�������ˮ�������Ϸ�Ӧ�Ļ�ѧ����ʽΪ�� ��3������ͼ��ʾ��ȡһ����CD��Һ��ʪ��pH��ֽƽ���ڲ���Ƭ�ϣ�ȡ����ʯī�����缫����ֱͨ����Դ��һ��ʱ���b�缫����pH��ֽ�Ͽɹ۲쵽���������������������������������������������������� , a�缫�ĵ缫��ӦʽΪ���������������� ����������������������������������������������������������������������������  ��4�������£���ͬ�����0.2mol��L��1CD��Һ��0.1mol��L��1 C2AB3��Һ�У���������Ŀ�϶���������������������� ��Һ�����ѧʽ�� |
|||
�� |
��1��CO��CO2 ��2��Na2O + H2O ==2NaOH ��3����ֽ�ȱ�죬����ɫ��������Ư����ɫ��2H+ +2e�� =H2����2H2O + 2e�� =H2��+ 2OH�� ��4��NaCl |
|||
| ��� | 38 |
|
||
���� |
2009���� | |||
| ��� | ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⡣ ��1������ʼʱ����K��a���ӣ���B���ĵ缫��ӦʽΪ���������������������������� ���������������������������� ��2������ʼʱ����K��b���ӣ���B���ĵ缫��ӦʽΪ���������������������������������������������������� ���ܷ�Ӧ�����ӷ���ʽΪ������������������������������������������������ �������й�����ʵ�飬����˵����ȷ���ǣ�����ţ����������������������� �� �� ����Һ��Na+��A���ƶ� �� �ڴ�A�����ݳ���������ʹʪ��KI������ֽ���� �� �۷�Ӧһ��ʱ������������ɻָ������ǰ����ʵ�Ũ�� �� ������״����B������2.24L���壬����Һ��ת��0.2 mol���� ��3����С��ͬѧģ�ҵ�������ӽ���Ĥ�����ռ�ķ�������ô������������ͼ9װ�õ���������Һ����ȡ������������������������ء�  �ٸõ��۵�������ӦʽΪ�������������������������������������������������������� ����ʱͨ�������ӽ���Ĥ������������������ ������ڡ���С�ڡ����ڡ���һͨ�������ӽ���Ĥ���������� ���Ƶõ�����������Һ�ӳ��ڣ���д��A������B������C������D������������������ ������ ��ͨ�翪ʼ������������ҺpH�����������ԭ���������������������������� ���������������������� �������Ƶõ�����������������������Һ���Ϊ����ȼ�ϵ�أ����������ĵ缫��ӦʽΪ�������������������������������������������� �� |
|||
�� |
��1��Fe��2e = Fe2+ ��2��2H+ + 2e- = H2�� 2Cl- + 2H2O ��� 2OH- + H2�� + Cl2�������� �� ��3���� 4OH- - 4e- = 2H2O + O2���� �� �� D �� H+�ŵ磬�ٽ�ˮ�ĵ��룬OH-Ũ������ �� O2 + 2H2O + 4e- = 4OH- |
|||
| ��� | 39 |
|
||
���� |
2009�������� | |||
| ��� | ij����С����е�ⱥ��ʳ��ˮ��ʵ�飨��ͼ����  ��ش��������⣺ ��1��ͨ��һ��ʱ��ɹ۲쵽�����缫�������������������������Һ��ɫ�ȱ�죬�õ缫�ϵĵ缫��ӦʽΪ������ ��2������Һ��ⷴӦ�Ļ�ѧ����ʽΪ�������������� �� ��3������ʼʱ���������������������ĵ缫��ӦʽΪ�������������� �� ��4������H2��O2Ϊ��Ӧ���KOHΪ�������Һ�� �ɹ�������ȼ�ϵ�أ���ͼ���������缫���ɶ����̿�Ƴɣ�ͨ�������ɿ�϶���ݳ������ڵ缫����ŵ硣����a�����������������������B���ĵ缫��ӦʽΪ������������ ������������������ ��  |
|||
�� |
��1������ 2H++2e-=H2��
��2��2NaC1+2H2O  C12��+H2��+2N aOH��2�֣� C12��+H2��+2N aOH��2�֣���3��Fe��2e-Fe2+ ��4���� O2+2H2O+4e-=4OH- |
|||
| ��� | 40 |
|
||
���� |
2008�ɶ����� | |||
| ��� | ��ͼ�У����缫�Ϸ����ĵ缫��Ӧ���£�a����2H++2e��=H2����b����Zn��2e=Zn2+��������˵������ȷ���� ��A����װ�ÿ����ǵ��� ��B����װ���е������ҺpH���ܵ���7 ��C��a��b������ͬ�ֵ缫���� ��D���ù�����������ת��һ���ǻ�ѧ��ת��Ϊ����  |
|||
�� |
D | |||
| ��� | 41 |
|
||
���� |
2009Ϋ��һģ | |||
| ��� | ����˵����ȷ���� ��A����ԭ��ع���ʱ����Һ�е����������ƶ� ��B���ö��Ե缫���ij��Һ���������ֱ�ֻ��H2��O2���ɵ��һ��ʱ�����Һ��Ũ�ȿ��ܼ�С ��C��Ҫʹ�����CuSO4��Һ��ԭ���������м���Cu(OH)2���� ��D�������������ֱ����Դ�ĸ������������������ӵ������ϣ����Է�ֹ��������ʴ |
|||
�� |
D | |||
| ��� | 42 |
|
||
���� |
2009�����߿� | |||
| ��� | �����ʺϵ�����������Ӧ2Fe3++2I��  2Fe2++I2��Ƴ�����ͼ��ʾ��ԭ��ء������ж�����ȷ���� 2Fe2++I2��Ƴ�����ͼ��ʾ��ԭ��ء������ж�����ȷ������A.��Ӧ��ʼʱ������ʯī�缫�Ϸ���������Ӧ ��B.��Ӧ��ʼʱ������ʯī�缫��Fe3+����ԭ ��C.�����ƶ���Ϊ��ʱ����Ӧ�ﵽ��ѧƽ��״̬ ��D.�����ƶ���Ϊ����ڼ�������FeCl2�̶�������ʯī�缫Ϊ����  |
|||
�� |
D | |||
| ��� | 43 |
|
||
���� |
2007�ɶ����� | |||
| ��� | ������ͼ���ṩ����Ϣ���ڷ�Ӧһ��ʱ��� ��1���׳��е�����Ϊ������������������������������������������������������ ��2���׳����ܷ�Ӧ�����ӷ���ʽΪ�������������������������������������������� �� ��3���ҳ����ܷ�Ӧ�����ӷ���ʽΪ������������������������������������ �� ��4����ʪ��ĵ���KI��ֽ�����ҳ�̼��������������ֽ��������ԭ���ǣ������ӷ���ʽ��ʾ���������������������������������������� ������������һ��ʱ����ַ�����ɫ��ȥ��������Ϊ������Cl2�����ɵ�I2������������Ӧ��Cl2��I2���ʵ���֮��Ϊ5��1�������������ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ������������������������������������ �� ��5�����ҳصĵ�Դ���ӷ���ʼʱ����������ͼʾ�෴����Ӧһ��ʱ�������Һ�п��ܳ��ֵ����������������������������������������������������������� ��  |
|||
�� |
��1���������ܽ⣬̼�����к�ɫ������������ɫ��Һ��dz ��2��Fe��Cu2��====Fe2����Cu ��3��2Cl����2H2O  Cl2����H2����2OH�� Cl2����H2����2OH����4��Cl2��2I��====I2��2Cl�� 5Cl2��I2��6H2O====2HIO3 ��10HCl ��5��������ɫ��״���� |
|||
| ��� | 44 |
|
||
���� |
δ֪ | |||
| ��� | �û���Ӧ��ͨʽ�ɱ�ʾΪ�� ��ش��������⣺ ��1������Ϊ����ɫ���壬��������ʹ������Һ����ɫ����÷�Ӧ�����ӷ���ʽΪ �������������������������������������������������������������������������� ��2���������ĵ��ʼ��뻯����A������Ӧ�Ļ�ѧ����ʽΪ����2Al+Fe2O3  Al2O3+2Fe�� Al2O3+2Fe������ȥ��Ӧ��������ʣ������������ɵ�Al2O3���õ��Լ����������������������� ��3����ҵ�������û���Ӧԭ���Ʊ�һ�ְ뵼����ϣ�д���÷�Ӧ�Ļ�ѧ����ʽ �������������������������������������������������������������������������� ��4�����������Ǻ�ɫ�ǽ������嵥�ʣ�������B�����ʵ����²��ϣ���÷�Ӧ�Ļ�ѧ����ʽΪ���������������������������������������������������������������������������� �� |
|||
�� |
��1��2I- + Cl2 = I2 + 2Cl- ��2��NaOH��Һ ��3��SiO2 + 2C  Si + 2CO�� Si + 2CO����4��2Mg+CO2  2MgO+C 2MgO+C |
|||
| ��� | 45 |
|
||
���� |
2009���ĸ߿� | |||
| ��� | ��ͼ��ʾ�й����ʣ����ɶ�����Ԫ���γɣ�֮���ת����ϵ������AΪ�����Ľ������ʣ�BΪ�ǽ������ʣ�һ���Ǻ�ɫ��ĩ����C�dz�������ɫ��ζҺ�壬D�ǵ���ɫ�Ĺ��廯�������Ӧ����ͼ����ʡ�ԡ��� ��1��A��B��C��D���������ʷֱ�Ϊ�ߣߣߡ��ߣߣߡ��ߣߣߡ��ߣߣߣ��ѧʽ���� ��2����Ӧ���е�C��D���������÷�Ӧ�Ļ�ѧ����ʽ�ǣߣߣߣߣߣߣߣߣߣߣߣߣ� ��3����Ӧ���У���B��F���ʵ���֮��Ϊ4��3��G��H�ֱ��ǣߣߡ��ߣߣ��ѧʽ���� ��4����Ӧ�۲�����K�Ļ�ѧʽΪ�ߣߣߣߣߣߣߣߣߣߣߣߣߣ� ��5����Ӧ�ܵ����ӷ���ʽΪ�ߣߣߣߣߣߣߣߣߣߣߣߣߡ� |
|||
�� |
��1��Al�� C����H2O��Na2O2 ��2��2Na2O2+2H2O=4NaOH+O2�� ������2Al+2NaOH+2H2O=2NaAlO2+3H2�� ��3��CO2������CO ��4��Na2CO3 ��5��CO2+AlO2��+OH��+H2O=CO32��+Al��OH��3�� |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |