 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| �߶���ѧ������ƽ�ⵥԪ��⡷��2�� | |
|---|---|
| �����������⣺26 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
δ֪ | |||
| ��� | �����£���0.1 mol��L��1 CH3COOH��Һ�У�ˮ�����ӻ��� ��A��1��10��14���������������� B��1��10��13.�������������������������� C��1.32��10��14�������� D��1.32��10��15. |
|||
�� |
A | |||
| ��� | 2 |
|
||
���� |
δ֪ | |||
| ��� | 90��ʱˮ�����ӻ�KW��3.8��10��13�����¶�ʱ��ˮ��pH�� ��A������7�������������������� B������6��7֮��.���� C������7���������������� D����ȷ�� |
|||
�� |
B | |||
| ��� | 3 |
|
||
���� |
δ֪ | |||
| ��� | ��Ӱ��ˮ�ĵ���ƽ�⣬��ʹ��Һ�е�c(H��)��c(OH��)�IJ����� ��A����ˮ��Ͷ��һС������� .������������������������������ B����ˮ�������. ��C����ˮ��ͨ�������̼����. ������������������������������ D����ˮ�м�ʳ�ξ��� |
|||
�� |
C | |||
| ��� | 4 |
|
||
���� |
δ֪ | |||
| ��� | ��������Һ��pH��ͬʱ�������ʵ���Ũ����С���ǡ� ��A��H2SO3�������������������������� B��H2SO4.�������������������� C��CH3COOH������������ D��HNO3. |
|||
�� |
B | |||
| ��� | 5 |
|
||
���� |
δ֪ | |||
| ��� | ������c(OH��)��С���� ��A��pH=0����Һ.������������������������������������������������������ B��0.05 mol��L��1 H2SO4. ��C��0.5 mol��L��1 HCl.������������������������������������������ D��0.05 mol��L��1��Ba(OH)2 |
|||
�� |
B | |||
| ��� | 6 |
|
||
���� |
δ֪ | |||
| ��� | ������ˮϡ��1 mol��L��1����ʱ��ʼ�ձ����������Ƶ��� ��A����Һ�е�c(CH3COO��) ������B����Һ�е�c(H��)������ C����Һ�е�c(CH3COOH) ��������D����Һ�е�c(OH��) |
|||
�� |
D | |||
| ��� | 7 |
|
||
���� |
δ֪ | |||
| ��� | 25��ʱ��pH=2��HCl��Һ�У���ˮ�������H��Ũ���� ��A��1��10��7mol��L��1���������������������� B��1��10��12mol��L��1. ��C��1��10��2mol��L��1�������������������� D��1��10��14mol��L��1. |
|||
�� |
B | |||
| ��� | 8 |
|
||
���� |
δ֪ | |||
| ��� | pH���������ͬ�Ĵ�������ᣬ�ֱ���������Na2CO3��Һ��Ӧ������ͬ�����·ų�������̼���������� ��A��һ���ࡡ���������� B������������.���� ��C������ȴ���ࡡ���������� D�����Ƚ� |
|||
�� |
B | |||
| ��� | 9 |
|
||
���� |
δ֪ | |||
| ��� | 95��ʱ��ˮ�е�H+�����ʵ���Ũ��Ϊ10��6 mol��L��1������0.01 mol��NaOH�����ܽ���95��ˮ�����1 L��Һ������Һ��pHΪ�� ��A��4���������������������������������� B��10���������������������������������� C��2�������������������������� D��12 |
|||
�� |
B | |||
| ��� | 10 |
|
||
���� |
δ֪ | |||
| ��� | ��pH��6��CH3COOH��Һ��ˮϡ��1000������Һ�е� ��A��pH��9�������������� B��c(OH��)��10��5mol��L��1������ ��C��pH��7�������������� D��c(OH��)��10��7 mol��L��1. |
|||
�� |
CD | |||
| ��� | 11 |
|
||
���� |
δ֪ | |||
| ��� | �����ͬ��pHҲ��ͬ��HCl��HNO3��CH3COOH�ֱ���������NaHCO3��Ӧ������CO2����� ��A��ͬ���ࡡ���������������� B��HCl���.����������������������C��HCl��HNO3һ���ࡡ������������ D��CH3COOH���. |
|||
�� |
CD | |||
| ��� | 12 |
|
||
���� |
δ֪ | |||
| ��� | ��pH=3��H2SO4��Һ��pH=10��NaOH��Һ��ϣ�����ǡ���кͣ���������Һ�������Ӧ�� ��A��10��1���������������������� B��1��10������������������������ C��1��100�������������������� D��1��2. |
|||
�� |
B | |||
| ��� | 13 |
|
||
���� |
δ֪ | |||
| ��� | ����ʱ��������Һ��pH����8�����8���� ��A��0.1 mol��L��1��NaOH��Һ�ζ�ϡ���ᣬ�÷�̪��ָʾ���ζ����յ� ��B��pH=6�Ĵ�����ˮϡ��100�� ��C��pH=10������������Һϡ��1000�� ��D��0.1 mol��L��1������100 mL��0.2 mol��L��1 NaOH��Һ150 mL��ȫ��Ӧ |
|||
�� |
AD | |||
| ��� | 14 |
|
||
���� |
δ֪ | |||
| ��� | ����˵������ȷ���� ��A��100 mL pH=3������ʹ�����Һ��������п��Ӧʱ����ʼʱ���߲������������ʻ������. ��B��100 mL 1 mol��L��1�������50 mL 2 mol��L��1������ֱ���������п��Ӧ�����߷ų����������ʺ����������. ��C��100 mL pH=3������ʹ�����Һ��������п��Ӧ�������������������. ��D��100 mL 0.1��mol��L��1�������������Һ��������п��Ӧ��ǰ�߷ų������������Ǻ��߷ų�����������2��. |
|||
�� |
AD | |||
| ��� | 15 |
|
||
���� |
δ֪ | |||
| ��� | ij����Һ��pH=1��������Һ�����ʵ���Ũ�� ��A��0.1 mol��L��1.������ ��B��һ������0.1 mol��L��1. ��C����Ϊǿ��һ������0.1 mol��L��1����Ϊ����һ������0.1 mol��L��1. ��D����Ϊǿ��һ����0.1 mol��L��1����Ϊ����һ����0.1 mol��L��1. |
|||
�� |
D | |||
| ��� | 16 |
|
||
���� |
δ֪ | |||
| ��� | ij�¶��£���ˮD2O�����ӻ�Ϊ1.6��10��15������pHһ���Ķ������涨pD=-lgc(D��)�����¹���pD��������ȷ���� ��A��������Һ��pD=7.0. ��B����0.01 mol��NaOD��D2O��Һ1L����pD=12.0. ��C���ܽ�0.01��mol��DCl��D2O��Һ1L����pD=2.0. ��D����100 mL 0.25 mol��L��1��DCl��ˮ��Һ�У�����50 mL 0.2mol��L��1��NaOD����ˮ��Һ����pD=1.0. |
|||
�� |
CD | |||
| ��� | 17 |
|
||
���� |
δ֪ | |||
| ��� | ������������AG��ʾ��Һ����ȣ�acidity arede����AG�Ķ���ΪAG��lg��[H��]/[OH��]�������б�����ȷ���� ��A����25��ʱ������Һ�����ԣ���pH��7��AG��1 ��B����25��ʱ������Һ�����ԣ���pH��7��AG��0 ��C����25��ʱ������Һ�ʼ��ԣ���pH��7��AG��0 ��D����25��ʱ����Һ��pH��AG�Ļ��㹫ʽΪAG��2(7��pH) |
|||
�� |
D | |||
| ��� | 18 |
|
||
���� |
δ֪ | |||
| ��� | pH=9�� ��Ba(OH)2��Һ��pH=12��KOH��Һ����4�U1������Ȼ�ϣ�������Һ��H+Ũ��Ϊ����λ��mol��L��1�� ��A�� 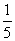 ��(4��10��9+1��10��12)���������������������� B�� ��(4��10��9+1��10��12)���������������������� B�� 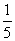 ��(8��10��9+1��10��12) ��(8��10��9+1��10��12) ��C��5��10��10������������������������������������������������ �� D��5��10��12 |
|||
�� |
D | |||
| ��� | 19 |
|
||
���� |
δ֪ | |||
| ��� | ijǿ����ҺpH=a��ǿ����ҺpH=b����֪a��b��12�������Һ���pH=7��������Һ���V(��)�ͼ���Һ���V(��)����ȷ��ϵΪ ��A��V(��)=102V(��)������������ B��V(��)=102V(��) ��C��V(��)��2V(��)�������������� D��V(��)��2V(��) |
|||
�� |
B | |||
| ��� | 20 |
|
||
���� |
δ֪ | |||
| ��� | ����ͬ�¶�ʱ100mL 0.01mol/L�Ĵ�����Һ��10mL 0.01mol/L�Ĵ�����Һ��Ƚϣ�������ֵǰ�ߴ��ں��ߵ��� ��A���к�ʱ����NaOH�������������������������������������������� B������� ��C���Ե����ʵ������������������������������������������������������� D��CH3COOH�����ʵ��� |
|||
�� |
BC | |||
| ��� | 21 |
|
||
���� |
δ֪ | |||
| ��� | ��pH= l������ƽ���ֳ� 2�ݣ�l�ݼ�����ˮ����1�ݼ�������������ʵ���Ũ����ͬ������NaOH��Һ��pH��������1��������ˮ��NaOH��Һ�������Ϊ ��A�� 9���������������������������� B��10���������������������������� C��11������������������������������ D��12 |
|||
�� |
C | |||
| ��� | 22 |
|
||
���� |
δ֪ | |||
| ��� | ��95��ʱ����ˮ��pH�������������������� (����ڡ���С�ڡ������ڡ�)7����ѡ������������������������������������������������������������������������������� �� |
|||
�� |
С�ڣ�250Cʱ��ˮ��pH = 7���������¶�ʱ��ˮ�ĵ���̶�����c(H+)Ҳ����pH��С |
|||
| ��� | 23 |
|
||
���� |
δ֪ | |||
| ��� | ��һ���¶��£��������ˮϡ�����У���Һ�ĵ�����������ͼ��ʾ����ش� ��1����O���㵼������Ϊ��0����������_______________________�� ��2��A��B��C����pHֵ�ɴ�С��˳����_______________________�� ��3��A��B��C��������������____________________��  |
|||
�� |
�ű�����ֻ����ˮ��Һ�е��룬��O����ʱΪ�����ᣬ�ѵ��룬����Ϊ�����硣 (2)C>A>B (3)C |
|||
| ��� | 24 |
|
||
���� |
δ֪ | |||
| ��� | ��25��ʱ����pHΪa��HCl��Һ��pHΪb��NaOH��Һ��ȡVaL��������Һ�ø�NaOH��Һ�кͣ���VbL��NaOH��Һ���ʣ� ��1����a+b=14����Va��Vb������������������������������������ . ��2����a+b=13����Va��Vb������������������������������������ ��3����a+b��14����Va��Vb���������������������������� ����Va������������������ Vb(�����������������) ������a��b��b��8����. |
|||
�� |
��1 �� 1/10��10a + b �C 14��> |
|||
| ��� | 25 |
|
||
���� |
δ֪ | |||
| ��� | ��һpH = 12��NaOH��Һ100 mL ����ʹ����pH��Ϊ11�� ��1�������������ˮ���ͼ���________ mL ��2���������pH = 10��NaOH��Һ��Ӧ����_________ mL ��3���������0.008 mol/L HCl��Һ��Ӧ����__________ mL |
|||
�� |
�� 900 �� 1000 �� 100 |
|||
| ��� | 26 |
|
||
���� |
δ֪ | |||
| ��� | ��ʵ��ȷ��ij��HA��������ʡ���ͬѧ�ķ����ǣ� �ף��ٳ�ȡһ��������HA����0.1mol/L����Һ100mL�� ����PH��ֽ�������Һ��PHֵ������֤��HA��������ʡ� �ң�������֪���ʵ���Ũ�ȵ�HA��Һ�����ᣬ�ֱ�����PH=1����������Һ��100mL�� �ڷֱ�ȡ��������Һ��10mL����ˮϡ��Ϊ100mL�� �۸�ȡ��ͬ���������ϡ��Һװ�������Թܣ�ͬʱ���봿����ͬ��п�����۲�������֤��HA��������ʡ� ��1�������������ĵڢٲ��У���Ҫ�õ��Ķ���������_____________�� ��2�������У�˵��HA��������ʵ������Dz����Һ��PH_________1��ѡ��������������ҷ����У�˵��HA��������ʵ�������_____________����ѡ�۷֣� ��a��װHCl���Թ��зų�H2�����ʿ� ��b��װHA��Һ���Թܵ��зų�H2�����ʿ� ��c�������Թ��в�����������һ���� ��3���������ۣ��ҷ���������ʵ��֮���Ͳ���֮��________________________�� ��4�����������һ���������Ƚ������еķ�����ҩƷ����ȡ������������Ҫ������ |
|||
�� |
��1��100mL����ƿ��ע��δ�������Ŀ۷֣� ��2��>b����ѡ�۷֣� ��3������pH=1��HA��Һ����ʵ�֣�����֮�����ڼ����п�����������������ͬ ��4������NaA��Һ������pHֵ>7��֤��HA��������ʡ� |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |