 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| ����ʡ2023����ͨ����ѧҵˮƽѡ���Կ��Ի�ѧ | |
|---|---|
| �����������⣺18 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | �л��Ļ�ԴԶ��������ѧ���Ļ������ܲ��ɷ֡�����˵��������� A.��ͭ���������𡱵���Ҫ����Ϊ�Ͻ� B.��ɳ����¥��������ľ�����Ҫ�ɷ�����ά�� C.���ײ��ü�Һ�����ƽ�����ֽ���ù��̲��漰��ѧ�仯 D.ͭ��Ҥ�ʴ��������Ϊ��Ҫԭ�ϣ��������ս���� |
|||
�� |
C | |||
| ��� | 2 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | ���л�ѧ�������������� A. HClO�ĵ���ʽ�� 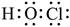 B.������Ϊ10����ԭ�ӣ�188O C. NH3���ӵ�VSEPRģ�ͣ� 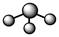 �� �� D.��̬Nԭ�ӵļ۲�����Ų�ͼ��  �� �� |
|||
�� |
C |
|||
| ��� | 3 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | ���в�����������Ӧʵ����ѡ�ò���������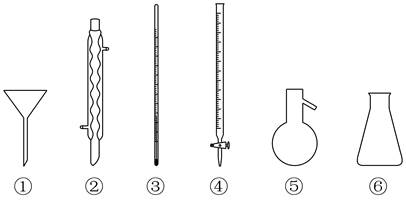 A.�ؽᾧ���ᴿ������٢ڢۡ����� B.������CH2Cl2��CCl4���ۢݢ� C.Ũ������Ҵ��Ʊ���ϩ���ۢݡ��������� D.���ζ����ⶨNaOH��ҺŨ�ȣ��ܢ� |
|||
�� |
A |
|||
| ��� | 4 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | �����й����ʽṹ�����ʵ�˵��������� A.��������̼ԭ�ӵķ��ӽ������Է��� B.���ǻ�����ȩ�ķе���ڶ��ǻ�����ȩ�ķе� C.������������ڲ����ȵ������¿ɷ���ˮ�ⷴӦ D.����(18���ڣ�6)�Ŀ�Ѩ��K+�ߴ����䣬������ͨ����������γɳ����� |
|||
�� |
A |
|||
| ��� | 5 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | �����йص缫����ʽ�����ӷ���ʽ������� A.����п�̵�ص�������Ӧ��MnO2+H2O+e��=MnO(OH)+OH�� B.Ǧ�����س��ʱ��������Ӧ��Pb2++2H2O��2e��=PbO2+4H+ C. K3[Fe(CN)6]��Һ����FeCl2��Һ�У�K++Fe2++[Fe(CN)6]3��=KFe[Fe(CN)6]�� D. TiCl4����ˮ�У�TiCl4+(x+2)H2O=TiO2��xH2O��+4H++4Cl�� |
|||
�� |
B |
|||
| ��� | 6 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | �չ�����õ���ij��ӫ��۵���Ҫ�ɷ�Ϊ3W3(ZX4)2��WY2����֪��X��Y��Z��WΪԭ���������������ǰ20��Ԫ�أ�WΪ����Ԫ�ء���̬Xԭ��s����ϵĵ�������p����ϵĵ�������ȣ���̬X��Y��Zԭ�ӵ�δ�ɶԵ�����֮��Ϊ2��1��3������˵����ȷ���� A.�縺�ԣ�X>Y>Z>W B.ԭ�Ӱ뾶��X D. ZԪ������������Ӧ��ˮ�������ǿ������ |
|||
�� |
C |
|||
| ��� | 7 |
|
|||||||||||||||
���� |
2023���ϸ߿� | ||||||||||||||||
| ��� | ȡһ������������Լ����з�Ӧ���ı������Լ��ĵμ�˳��(�Լ�Ũ�Ⱦ�Ϊ0.1 mol��L��1)����Ӧ����û�����Բ�����
|
||||||||||||||||
�� |
D |
||||||||||||||||
| ��� | 8 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | �����������һ����Ҫ�IJ��Ƽ�����ҵ���������ǡ�̼���Ϊԭ�ϣ����廯����Һ�в��ü�ӵ�������Ӧ�Ʊ���������ƣ�����������Ӧ�������£�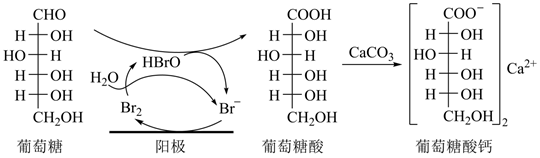 ������ ������ ����˵��������� A.�廯������͵������� B.ÿ����1mol��������ƣ������ϵ�·��ת����2mol���� C.����������ͨ�������ڷ�Ӧ���ɺ�����Ԫ��״�ṹ�IJ��� D.�������ܷ�����������ԭ��ȡ�����ӳɺ���ȥ��Ӧ |
|||
�� |
B |
|||
| ��� | 9 |
|
|||||||||||||||
���� |
2023���ϸ߿� | ||||||||||||||||
| ��� | ����ijͭұ����ˮ(��Cu2+��Fe3+��Zn2����Al3+)�IJ����������£�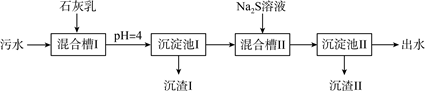 �� �� ��֪������Һ�н������ӿ�ʼ��������ȫ������pH���±���ʾ��
����˵��������� A. ���������к���Fe(OH)3��Al(OH)3 B. Na2S��Һ�ʼ��ԣ�����Ҫԭ����S2��+H2O  HS��+OH�� HS��+OH��C. �������آ��У���Cu2+��Zn2����ȫ����ʱ����Һ�� 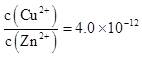 D. ����ˮ���������ӽ�����֬����������������ҵ��ȴѭ����ˮ |
||||||||||||||||
�� |
D |
||||||||||||||||
| ��� | 10 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | �ͻ�����ͨ����Ҫ�õ����������ϡ��о����֣��ڲ�ͬ�Ŀ���ʪ�Ⱥ��������£����ϴƻ�(As2S3)��ɫ����Ҫԭ���Ƿ������������ֻ�ѧ��Ӧ�� �� �� ����˵����ȷ���� A. S2O32����SO42���Ŀռ�ṹ�������������� B.��Ӧ��͢��У�Ԫ��As��S�������� C.��Ӧ��͢��У��μӷ�Ӧ�� 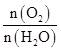 ����<�� ����<��D.��Ӧ��͢��У�����1mol As2S3ת�Ƶĵ�����֮��Ϊ3��7 |
|||
�� |
D |
|||
| ��� | 11 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | ��ѧ�Һϳ���һ�ָ��³������ϣ��侧���ṹ��ͼ��ʾ����������������Ϊapm�������ӵ�������ֵΪNA������˵���������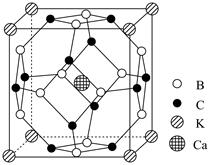 �� �� B.��������K+����Ҿ�����ȵ�Ca2+��8�� C.������B��Cԭ�ӹ��ɵĶ�������12���� D.������ܶ�Ϊ 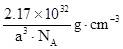 |
|||
�� |
C |
|||
| ��� | 12 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | �����£���Ũ��Ϊ0.0200 mol��L��1��NaOH����Һ�ζ�Ũ�Ⱦ�Ϊ0.0200 mol��L��1��HCl��CH3COOH�Ļ����Һ���ζ���������Һ��pH��� (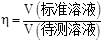 )�ı仯������ͼ��ʾ������˵��������� )�ı仯������ͼ��ʾ������˵���������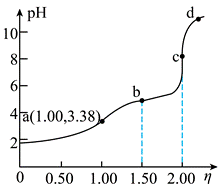 �� �� A. Ka(CH3COOH)ԼΪ10��4.76 B.��a��c(Na+)��c(Cl����c(CH3COOH) +c(CH3COO��) C.��b��c(CH3COOH)��c(CH3COO��)�� D.ˮ�ĵ���̶ȣ�a��b��c��d |
|||
�� |
D |
|||
| ��� | 13 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | ��һ�����ܱ������м���1mol CH4��һ������H2O��������Ӧ��CH4(g)��H2O(g) CO(g)��3H2(g)��CH4��ƽ��ת���ʰ���ͬͶ�ϱ� CO(g)��3H2(g)��CH4��ƽ��ת���ʰ���ͬͶ�ϱ�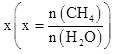 ���¶ȵı仯������ͼ��ʾ������˵��������� ���¶ȵı仯������ͼ��ʾ������˵���������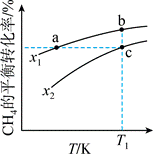 �� �� A. x1��x2 B.��Ӧ���ʣ�Vb����Vc�� C.��a��b��c��Ӧ��ƽ�ⳣ����Ka��Kb��Kc D.��Ӧ�¶�ΪT1����������ѹǿ����ʱ����Ӧ�ﵽƽ��״̬ |
|||
�� |
B | |||
| ��� | 14 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | N2H4��һ��ǿ��ԭ�Եĸ������ʣ��ں��졢��Դ�������й㷺Ӧ�á��ҹ���ѧ�Һϳɵ�ijRu(��)����(��[L�DRu�DNH3]+��ʾ)�ܸ�Ч�������NH3�ϳ�N2H4���䷴Ӧ������ͼ��ʾ��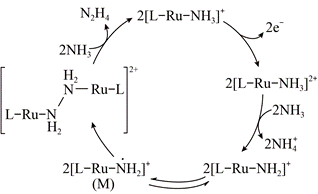 �� �� ����˵��������� A. Ru (��)��������Ru (��)������NH3ʧȥ����������ǿ B. M��Ru�Ļ��ϼ�Ϊ+3 C.�ù����зǼ��Լ����γ� D.�ù��̵��ܷ�Ӧʽ��4NH3�D2e�D=N2H4+2NH4+ |
|||
�� |
B |
|||
| ��� | 15 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | ����Ni��H2��ǿ�������ã����㷺�����������ʻ��Ȳ����ͻ��ŵĴ��⻯��Ӧ������״Niת���ɶ��������Ni���������������ߡ� ��֪��������Ni��¶�ڿ����п�����ȼ�����Ʊ���ʹ��ʱ������ˮ���л��ܼ���������桰ʪ�� �������������ڼ����л��ܼ��и������ڷ�Ӧ�Ľ��С� ijʵ��С���Ʊ�����Ni��̽������⻯���ܵ�ʵ�����£� ����1������Ni���Ʊ�  ����2�������������Ĵ��⻯��Ӧ ��Ӧ��ԭ����ʵ��װ��ͼ����(�г�װ�úͽ���װ����)��װ�â����ڴ���H2�ͼ�ⷴӦ���̡�  �ش��������⣺ ��1������(a)�У���Ӧ�����ӷ���ʽ��_______�� ��2������(d)�У��ж�����Ni��ˮϴ���ķ�����_______�� ��3������(e)�У������ܼ����������ڲ���2���⻯��Ӧ����_______�� A.��ͪ������������������������������������������������������ B.���Ȼ�̼������������������������������������������ C.�Ҵ��������������������������������������������������������� D.������ ��4���������г���H2ʱ����ͨ���Ŀ�·λ������ͼ��ʾ�������⻯��Ӧʱ����������װ�â�������ʱ��·λ�������Ϊ_______�� 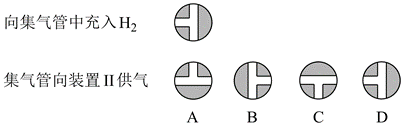 ��5������M��������_______�� ��6����ӦǰӦ��װ�â���ͨ��N2һ��ʱ�䣬Ŀ����_______�� ��7�����������ƿN�еĵ����ܿڲ���Һ�����£����ܵ��µĺ����_______�� ��8���ж��⻯��Ӧ��ȫ��������_______�� |
|||
�� |
��1��2Al+2OH��+2H2O=2AlO2��+3H2�������� ��2��ȡ���һ��ϴ��Һ���Թ��У��μӼ��η�̪�������Һ����ۺ�ɫ����֤��ϴ�Ӹɾ�������û��ϴ�Ӹɾ���������3��C������ ��4��B��������5����ѹ��Һ©�������� ��6���ų�װ���еĿ�������ֹ����Ni��ȼ������ ��7���ܵ����������ȣ������ڼ�ⷴӦ���̡����� ��8����������Һ�治�ٸı� |
|||
| ��� | 16 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | �۱���ϩ��һ����Ҫ�ĸ߷��Ӳ��ϣ���ͨ������ϩ�ۺ��Ƶá� ����ϩ���Ʊ� ��1����֪���з�Ӧ���Ȼ�ѧ����ʽ�� ��C6H5C2H5(g)+ 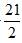 O2(g)��8CO2(g)��5H2O(g)�� ��H1=��4386.9kJ��mol��1 O2(g)��8CO2(g)��5H2O(g)�� ��H1=��4386.9kJ��mol��1��C6H5CH��CH2(g)+ 10O2(g)��8CO2(g)��4H2O(g)�� ��H2=��4263.1kJ��mol��1 ��H2(g)+ 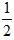 O2(g)��H2O(g)�� ��H3=��241.8kJ��mol��1 O2(g)��H2O(g)�� ��H3=��241.8kJ��mol��1���㷴Ӧ��C6H5C2H5(g)= C6H5CH��CH2(g) + H2(g)����H4=_____kJ��mol��1 ��2����ij�¶ȡ�100kPa�£���Ӧ���г���1mol��̬�ұ�������Ӧ�ܣ���ƽ��ת����Ϊ50%������ƽ��ת���������75%����Ҫ��Ӧ���г���_______molˮ������Ϊϡ����(����ʱ���Ը���Ӧ)�� ��3����913K��100kPa�£���ˮ������ϡ������Fe2O3���������ұ����������ɱ���ϩ�⣬���ᷢ��������������Ӧ�� ��C6H5C2H5(g)����C6H6(g)+CH2��CH2(g) ��C6H5C2H5(g)��H2(g)����C6H5CH3(g)+CH4(g) ���Ϸ�Ӧ��ϵ�У����������ﱽ��ϩ�����ͼױ���ѡ����S(  )���ұ�ת���ʵı仯������ͼ��ʾ����������b�����IJ�����_______��������_______�� )���ұ�ת���ʵı仯������ͼ��ʾ����������b�����IJ�����_______��������_______��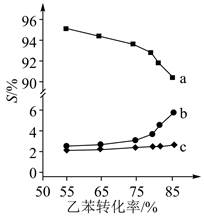 �� �� ��4�����ڱ���Ӧ��ϵ�д���Fe2O3�������������_______�� A. X�������似���ɲⶨFe2O3����ṹ B. Fe2O3�ɸı��ұ�ƽ��ת���� C. Fe2O3�������ұ����ⷴӦ�Ļ�� D.�ı�Fe2O3������С��Ӱ�췴Ӧ���� ����ϩ�ľۺ� ����ϩ�ۺ��ж��ַ���������һ�ַ����Ĺؼ�������ijCu(��)�������ٽ�C6H5CH2X (��������X��ʾ±��)�������ɻ�C6H5CH2∙��ʵ�ֱ���ϩ�ɿؾۺϡ� ��5��������C6H5CH2Cl��C6H5CH2Br��C6H5CH2I�л�����ߵ���_______�� ��6�������£���Cu+������L��ˮ��Һ���γ�[Cu(L)2]+���䷴Ӧƽ�ⳣ��ΪK����CuBr��ˮ�е��ܶȻ�����ΪKsp���ɴ˿�֪��CuBr������L��ˮ��Һ���ܽⷴӦ��ƽ�ⳣ��Ϊ_______(���з���ʽ�м���ϵ����ϵ��Ϊ���������)�� |
|||
�� |
��1��+118������ ��2��5������ ��3�������� ��. �������� ��. ��Ӧ��Ϊ����Ӧ����Ӧ�ݢ�Ϊ����Ӧ������ϩ��ѡ��������ں��º�ѹ�£����ұ�ת���ʵ�����Ӧ�������ƶ�����Ӧ���ƶ���������b�������ﱽ������ ��4��BD������ ��5��C6H5CH2I������ ��6��K∙Ksp |
|||
| ��� | 17 |
|
||||||||||
���� |
2023���ϸ߿� | |||||||||||
| ��� | ����Ga(CH3)3���Ʊ��������뵼���֧��Դ����֮һ�����������ҹ��Ƽ������߿����˳������������������ͳ�����װһϵ�и��¼����������Ƴ���Ga(CH3)3����ȡ���������ɹ�����ҵ���Դ���Ϊԭ�ϣ��Ʊ�����Ga(CH3)3�Ĺ����������£�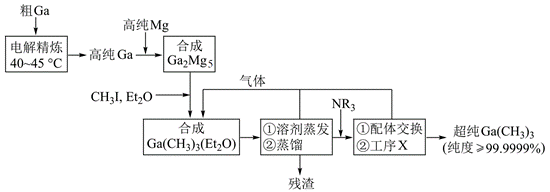 �� �� ��֪���ٽ���Ga�Ļ�ѧ���ʺ�Al���ƣ�Ga���۵�Ϊ29.8�棻 ��Et2O (����)��NR3 (��������)�����������п���Ϊ���壻 ��������ʵķе㣺
��1������Ga(CH3)3�ľ���������_______�� ��2������⾫����װ����ͼ��ʾ�������¶ȿ�����40��45���ԭ����_______�������ĵ缫��ӦʽΪ_______��  �� �� ��3�����ϳ�Ga(CH3)3(Et2O)�������еIJ��ﻹ����MgI2��CH3MgI��д���÷�Ӧ�Ļ�ѧ����ʽ��_______�� ��4��������������ˮ�������ܲ�����ȼ�����壬��������Ҫ�ɷ���_______�� ��5������˵���������_______�� A.������Et2O�õ���ѭ������ B.�����У����ϳ�Ga2Mg5����������X��������ˮ�����������½��� C. ������X���������ǽ���Ga(CH3)3(NR3)��������Ga(CH3)3 D.�ú˴Ź������ײ�������Ga(CH3)3��CH3I ��6��ֱ�ӷֽ�Ga(CH3)3(Et2O)�����Ʊ�����Ga(CH3)3���������̲��á����彻���������Ʊ�����Ga(CH3)3��������_______�� ��7���ȽϷ����е�C��Ga��C���Ǵ�С��Ga(CH3)3_______ Ga(CH3)3(Et2O) (�>����<����=��)����ԭ����_______�� |
|||||||||||
�� |
��1�����Ӿ��塡���� ��2���������ٱ�֤GaΪҺ�壬���ڴ�Ga������������GaO2��+3e��+2H2O=Ga+4OH������[Ga(OH)4]��+3e��=Ga+4OH���������� ��3��8CH3I+2Et2O+Ga2Mg5=2 Ga(CH3)3(Et2O)+3MgI2��2CH3MgI�������� ��4��CH4��������5��D������ ��6��NR3�е�ϸߣ�����Ga(CH3)3���룬Et2O�ķе����Ga(CH3)3��һ�����������Եõ�����Ga(CH3)3������ ��7����>����Ga(CH3)3��GaΪsp2�ӻ�������Ϊƽ��ṹ����Ga(CH3)3(Et2O)��GaΪsp3�ӻ�������Ϊ������ṹ���ʼнǽ�С |
|||||||||||
| ��� | 18 |
|
||
���� |
2023���ϸ߿� | |||
| ��� | ������������ǼܵĻ����ﳣ���п�������������������ԣ�һ�ֺϳɸ�������·������(���ַ�Ӧ�����Ѽ�)��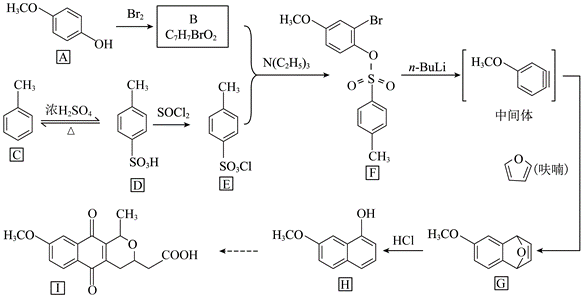 �� �� �ش��������⣺ ��1��B�Ľṹ��ʽΪ_______�� ��2����Fת��ΪG�Ĺ��������漰�ķ�Ӧ������_______��_______�� ��3������G���������ŵ�����Ϊ_______��_______�� ��4���������������ṩ����Ϣ�����з�Ӧ����J�Ľṹ��ʽΪ_______��  �� �� ��5���������ʵ������ɴ�С��˳����_______(д���)�� �� 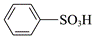 ������ ������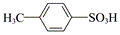 ������ ������ �� �� ��6��  �� (�)��һ����Ҫ�Ļ���ԭ�ϣ����ܹ�����������Ӧ��ͬ���칹���С���H2C=C=CH��CHO�⣬����_______�֣� �� (�)��һ����Ҫ�Ļ���ԭ�ϣ����ܹ�����������Ӧ��ͬ���칹���С���H2C=C=CH��CHO�⣬����_______�֣���7���ױ�������FeBr3���·�����Ӧ����ͬʱ���ɶ���ױ�������ױ���������C��D�ķ�Ӧ��Ϣ������Լױ�Ϊԭ��ѡ���Ժϳ�����ױ���·��_______(���Լ���ѡ)�� |
|||
�� |
��1��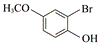 ���������� ���������� ��2����.��ȥ��Ӧ��������.�ӳɷ�Ӧ������ ��3����.̼̼˫����������.�Ѽ������� ��4��  ���������� ���������� ��5����>��>�ڡ����� ��6��4������ ��7�� 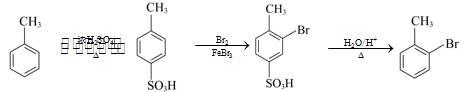 |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |