 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 泉州市2022届高中毕业班质量监测(五) | |
|---|---|
| 本卷共有试题:15 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 青铜器在古时被称为“金”或“吉金”,是红铜与锡、铅等的合金。铜锈大多呈青绿色,主要含有Cu2(OH)3Cl和Cu2(OH)2CO3。下列说法错误的是 A.青铜器中锡、铅对铜有保护作用 B.青铜的熔点低于纯铜 C.可用FeCl3溶液清除青铜器的铜锈 D.古时冶炼铸造青铜器涉及化学变化 |
|||
答案 |
C | |||
| 题号 | 2 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 一定条件下,肉桂醛可转化为苯甲醛: 下列说法错误的是 A.肉桂醛能发生取代、加成、聚合等反应 B.肉桂醛与苯甲醛都能使酸性KMnO4溶液褪色 C.苯甲醛分子的所有原子可能共平面 D.肉桂醛与苯甲醛互为同系物 |
|||
答案 |
D | |||
| 题号 | 3 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | NA是阿伏加德罗常数的值。利用反应2NH3+NaClO= N2H4+ NaCl+ H2O可制备火箭推进剂的燃料N2H4。下列说法正确的是 A. 0.1molNH3溶于水形成的饱和溶液中,NH4+的数目为0.1NA B. 1 L2 mol・L-1的NaClO溶液中,O原子的数目为2NA C.每生成11.7gNaCl,该反应转移电子数为0.4NA D.标准状况下,2.24L的H2O中含有的质子数为1NA |
|||
答案 |
C | |||
| 题号 | 4 |
|
||||||||||||||||||||
出处 |
2022泉州五检 | |||||||||||||||||||||
| 题干 | 下列实验操作、现象及结论均正确的是
|
|||||||||||||||||||||
答案 |
B |
|||||||||||||||||||||
| 题号 | 5 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 用如图所示装置进行NH3与CuO反应的实验。下列说法错误的 A.加入药品前须检验装置的气密性 B. a中药品为氯化铵固体 C. b中固体变红,可能有Cu2O生成 D.c中能收集到氨水,d中可收集到N2 |
|||
答案 |
B | |||
| 题号 | 6 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 某科研团队提出了一种水基Li-CO2二次电池,它由纳米孔Pd膜电极、固体电解质膜等构成,图为工作示意图。下列说法错误的是 A.放电时,Pd膜作正极 B.固体电解质膜可将Li电极与LiCl溶液隔离 C.充电时,Pd膜表面发生反应:HCOOH-2e- =CO2↑+2H+ D.理论上,当消耗7gLi时吸收5.6L CO2 (标准状况) |
|||
答案 |
D | |||
| 题号 | 7 |
|
|||||||||||||||
出处 |
2022泉州五检 | ||||||||||||||||
| 题干 | 对下列粒子组在水溶液中能否大量共存的判断和分析均正确的是
|
||||||||||||||||
答案 |
B | ||||||||||||||||
| 题号 | 8 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 短周期主族元素W、X、Y、Z的原子序数依次增大,W与X同周期且相邻,W、Y的最外层电子数之和与Z的最外层电子数相等,Z的单质与X的氢化物可发生置换反应,常温下Y的单质在浓硫酸中能形成致密氧化膜。下列说法一定正确的是 A.最简单氢化物的沸点:W<X B. Y与Z形成离子化合物 C. W的氧化物是酸性氧化物 D.简单离子的半径:X<Y |
|||
答案 |
A | |||
| 题号 | 9 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 将铜片与足量浓盐酸混合加热,铜片溶解,有气泡产生,溶液呈无色。已知:Cu++3Cl- CuCl32-(无色) K=5.0×105;Ksp(CuCl)=1.2×10-6,下列说法错误的是 CuCl32-(无色) K=5.0×105;Ksp(CuCl)=1.2×10-6,下列说法错误的是A.铜片表面产生的气体为H2 B.金属活泼性顺序是有一定前提条件的 C.将反应后的溶液稀释,无沉淀产生 D.铜不与稀盐酸反应主要因c(Cl-)不够大 |
|||
答案 |
C | |||
| 题号 | 10 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 常温下,H3PO4在水中的各级电离过程如图所示,已知:pKa=-1gKa。 下列说法错误的是 A.反应H3PO4+HPO42-  2 H2PO4-的平衡常数为1.0×105 2 H2PO4-的平衡常数为1.0×105B.若用NaOH溶液滴定Na2HPO4溶液,不可选用酚酞作指示剂 C.将0.2 mol・L-1的H3PO4溶液和0.3 mol・L-1的NaOH溶液等体积混合,pH≈7.2 D. 0.1 mol・L-1 Na2HPO4溶液中,c(HPO42-)>c(PO43-)> c(H2PO4-)> c(H3PO4) |
|||
答案 |
D |
|||
| 题号 | 11 |
|
||||||||||||
出处 |
2022泉州五检 | |||||||||||||
| 题干 | 某湿法炼锌的萃余液中含有Na+、Zn2+、Fe2+、Mn2+、Co2+、Cd2+及30 ~60g・L-1 H2SO4等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图: 已知:
(1)“中和氧化水解”时,先加入适量的石灰石调节溶液的pH为1.0;加入一定量的Na2S2O8;再加入石灰石调节溶液的pH为4.0。 ①氧化”时,Mn2+转化为MnO2除去,反应的离子方程式为_______。 ②“沉渣”的主要成分除MnO2外还有_______。 ③“氧化”时,若加入过量的Na2S2O8,钴元素将会进入“沉渣”中,则水解后的溶液中含钴微粒的浓度为_______mol・L-1。 (2)“除镉”时,主要反应的离子方程式为_______。 (3)“沉锌”时,在近中性条件下加入Na2CO3可得碱式碳酸锌[ZnCO3・2Zn(OH)2・H2O]固体,同时产生大量的气体。 ①产生大量气体的原因是_______。 ②ZnCO3・2Zn(OH)2・H2O需洗涤,检验是否洗净的试剂是_______。 (4)不同质量分数的Na2SO4溶液在不同温度下析出Na2SO4晶体的物种如图所示。欲从含20% Na2SO4及微量杂质的“沉锌后液”中直接析出无水Na2SO4,“操作a”为_______。  |
|||||||||||||
答案 |
(1)①S2O82-+ Mn2++2H2O= MnO2↓+ 2SO42-+4H+ ②Fe(OH)3、CaSO4 ③1.6 ×10-14 (2)Zn+Cd2+= Zn2++Cd (3)①Zn2+和CO32-发生双水解,相互促进,产生ZnCO3・2Zn(OH)2・H2O和CO2气体 ②. BaCl2溶液 (4)蒸发浓缩、趁热过滤 |
|||||||||||||
| 题号 | 12 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 某小组用四氢化萘( ,无色有刺激性气味液体,沸点207°C)、液溴、蒸馏水和纯铁粉为原料,利用反应C10H12+4Br2 ,无色有刺激性气味液体,沸点207°C)、液溴、蒸馏水和纯铁粉为原料,利用反应C10H12+4Br2 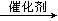 C10H8Br4+4HBr制取少量粗HBr溶液,同时获得四溴化萘(常温下为固态,不溶于水)。 C10H8Br4+4HBr制取少量粗HBr溶液,同时获得四溴化萘(常温下为固态,不溶于水)。实验步骤: ①按一定质量比把四氢化萘和水加入反应器中,加入少量纯铁粉。 ②缓慢滴入液溴,不断搅拌,直到四氢化萘反应完全。 ③_______,得到粗HBr溶液。 回答下列问题: (1)图中适合步骤①和②的装置是乙,不选用甲的理由是_______。  (2)步骤②中,反应完全、达到终点的现象是_______。 (3)乙中玻璃导管的作用是_______、_______。 (4)请将步骤③补充完整:_______。 (5)粗HBr溶液在空气中长期放置,溶液呈黄色。其原因可能是_______ (用离子方程式表示)。 (6)检验实验所得HBr溶液中是否含有Fe2+:取少量粗HBr溶液加入过量AgNO3溶液,静置,取上层清液滴入到KMnO4溶液中,若紫红色的KMnO4溶液褪色,证明溶液中含Fe2+,若紫红色不褪色,则不含Fe2+。该方法是否可行,并说明理由。_______。 (7)有人认为Fe3+起催化作用。欲验证该想法,按上述实验步骤进行实验,只须改动的是:_______。 (8)若得到的粗HBr溶液浓度为4 mol・L-1 (密度为×1.2g・cm-3),则四氢化萘(Mr=132)和水的质量比是_______(列式即可,设溴化反应进行完全)。 |
|||
答案 |
(1)溴易挥发,会污染空气;溴会腐蚀胶头滴管的胶帽 (2)滴入最后一滴液溴时,溶液呈浅黄色 (3) ①.冷凝回流 ②.平衡气压 (4)过滤 (5)4Br -+4H++O2 = 2Br2+ 2H2O (6)不可行,NO3-在酸件条件下能将Fe2+氧化Fe3+,观察不到紫红色的KMnO4溶液褪色 (7)将步骤①中的铁粉改为FeBr3 (8)  |
|||
| 题号 | 13 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | CO2用于催化氧化C2H6合成C2H4,总反应为:CO2(g)+C2H6(g)  C2H4(g)+CO(g)+H2O(g)+ ∆H=+177 kJ・mol-1;反应分两步进行: C2H4(g)+CO(g)+H2O(g)+ ∆H=+177 kJ・mol-1;反应分两步进行:反应i: C2H6(g)  C2H4(g)+ H2(g) ∆H1=+ 137kJ・mol-1 C2H4(g)+ H2(g) ∆H1=+ 137kJ・mol-1反应ii: CO2(g)+H2(g)  CO(g)+ H2O(g) ∆H2 CO(g)+ H2O(g) ∆H2回答下列问题: (1)∆H2 =_______ kJ・mol-1。 (2)已知平衡常数(K)与温度(T)之间存在定量关系,且符合Van’tHoff方程lnK= -  (不同反应中C不同)。上述三个反应的平衡常数(K)与温度(T)之间的关系如图,反应i对应的曲线为_______(填“a”“b”或“c”)。 (不同反应中C不同)。上述三个反应的平衡常数(K)与温度(T)之间的关系如图,反应i对应的曲线为_______(填“a”“b”或“c”)。 (3)按照n(CO2):n(C2H6)=1:1投料,测得C2H6平衡转化率[α(C2H6)]与温度、压强的关系如图所示,则压强P1、P2、P3由大到小的顺序为_______,判断的理由是________。  (4)在C2H4合成体系内会发生副反应。 ①若发生副反应C2H6(g)  3H2(g)+ 2C(s),会降低催化效率,原因是_______。 3H2(g)+ 2C(s),会降低催化效率,原因是_______。②某温度下,若只存在副反应:2CO2(g)+C2H6(g)  4CO(g)+3H2(g)。向aL密闭容器中充入1.2molC2H6和2molCO2,tmin后反应达到平衡,容器内C2H4为0.6mol,CO2为0.4 mol,则v(CO2)=_______ mol・L-1・min-1,C2H6的平衡总转化率为_______%(保留1位小数)。 4CO(g)+3H2(g)。向aL密闭容器中充入1.2molC2H6和2molCO2,tmin后反应达到平衡,容器内C2H4为0.6mol,CO2为0.4 mol,则v(CO2)=_______ mol・L-1・min-1,C2H6的平衡总转化率为_______%(保留1位小数)。(5)我国科学家利用CO2电催化氧化法实现了C2H6制备C2H4,阴极电极反应式为:CO2+2e-=CO+O2-,则阳极电极反应式是_______。 |
|||
答案 |
(1)+40 (2)c (3) ①. P1>P2>P3 ②.温度相同时,加压平衡逆向移动,故压强越大,C2H6的平衡转化率越小 (4) ①.催化剂表面产生积碳,减少与反应物接触从而降低催化效率或导致催化剂失活 ②.  ③. 91.7 ③. 91.7 (5)C2H6+ O2--2e-= C2H4+ H2O |
|||
| 题号 | 14 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 锌的化合物在生产生活中有广泛的应用。 (1)L-赖氨酸锌螯合物X (结构为如图)易被人体吸收。  ①X中元素(除H外)的第一电离能由小到大的顺序为_______,加“*”氧原子的杂化方式为_______。 ②X的晶体中存在的微粒间作用力有._______。 A.离子键 B. π键 C.金属键 D.配位键 E.非极性键 ③L-赖氨酸易溶于水主要原因是_______。 (2)某锌铁氧体[化学式为ZnxFe(III)yOz]制成的磁芯被广泛用于电子行业。 ①组成微粒的原子(或离子)中存在未成对电子,该微粒具有顺磁性。指出锌铁氧体晶体中具有顺磁性的离子,并说明理由_______。 ②锌铁氧体晶胞结构如图所示,该晶胞由4个A型和4个B型小立方体构成。锌铁氧体的化学式为_______。  |
|||
答案 |
(1)①Zn、C、O、N ②sp3杂化 ③.B、D、E ④L-赖氨酸分子与水分子形成分子间氢键 (2)①Fe3+,Fe3+的外围电子排布为3d5,存在5个未成对电子 ②ZnFe2O4 |
|||
| 题号 | 15 |
|
||
出处 |
2022泉州五检 | |||
| 题干 | 有机物M是合成一种应用广泛的杀虫杀螨剂的中间体,合成路线如图: 回答下列问题: (1)A的名称为_______,由E生成F的反应类型是_______。 (2)M中所含官能团的名称是._______,分子中_______(填“有”或“无”)手性碳原子。 (3)由C生成D是取代反应,该反应的化学方程式为_______。 (4)G的结构简式为_______。 (5)写出同时满足下列条件的C的一种同分异构体的结构简式_______。 a.遇FeCl3溶液显紫色 b.能发生银镜反应 c.核磁共振氢谱图显示五组峰,且峰面积比为6:4:2:1:1 |
|||
答案 |
(1)①1,3,5-三甲苯 ②加成反应 (2) ①酯基 ②无 (3)  (4)  (5)  或 或 (写一种即可)。 (写一种即可)。 |
|||
| v福建省实践教学工作室 蔡实践 设计制作 v |