 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 1 | |
|---|---|
| 本卷共有试题:2 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
|||||||||
出处 |
2022泉州三检 | ||||||||||
| 题干 | 某研究性学习小组利用氯型阴离子交换树脂(RCl)从海带中提取I2,并测定反应I2(aq)+I-(aq) I3-(aq)的平衡常数。 I3-(aq)的平衡常数。I.离子交换法提取I2的流程如下:  已知:①交换吸附发生反应:RCl+I3-  RI3+Cl−,RCl+I− RI3+Cl−,RCl+I− RI+Cl−; RI+Cl−;②吸附I−和I3-达饱和的树脂分别呈淡黄色和黑红色。 (1)“氧化”时I−转化为I3-,反应的离子方程式为 。 (2)“一次洗脱”已经完成的现象是 。 (3)向洗脱液1中加入6 mol・L−1 H2SO4调节pH至1.5~2.0,可析出碘晶体。洗脱液1中,碘元素以 (填离子符号)存在。 (4)将分离出碘晶体的洗脱液合并,经酸化后,加入氧化剂,再置于 (填仪器名称)中,加入乙醚,振荡,静置,分液。后经 (填操作名称)回收乙醚。 II.测定反应I2(aq)+I−(aq)  I3-(aq)的平衡常数K I3-(aq)的平衡常数K常温下,取2个碘量瓶分别加入下表中的药品,振荡半小时。取一定体积的上层清液用0.0500mol・L−1Na2S2O3溶液进行滴定,测定I2和I3-的总浓度。 
(6)碘的质量不需要准确称取的理由是 。 (7)碘量瓶①平衡体系中c(I2)与②中c(I2)接近。K≈ (保留3位有效数字)。 |
||||||||||
答案 |
(1)H2O2+3I−+2H+=I3−+2H2O (2)树脂的颜色由黑红色完全褪为淡黄色 (3)I−、IO3−(写IO−亦给分) (4)分液漏斗;蒸馏 (5)使用锥形瓶I-易被空气中氧气氧化(或I2易升华) (6)在水或KI溶液中I2(aq)已经饱和(或I2过量等合理答案) (7)511 |
||||||||||
| 题号 | 2 |
|
||
出处 |
2021北京西城4月 | |||
| 题干 | 相同温度和压强下,研究Cl2在不同溶液中的溶解度(用溶解Cl2的物质的量浓度表示)随溶液浓度的变化。在NaCl溶液和盐酸中Cl2的溶解度以及各种含氯微粒的浓度变化如图。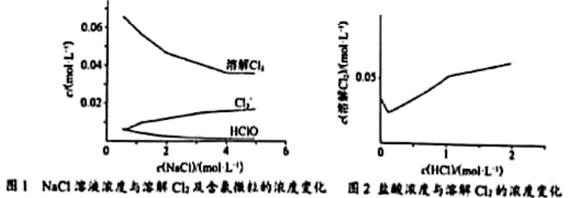 下列说法不正确的是 A.由图1可知,Cl2溶于NaCl溶液时还发生了反应Cl2+Cl-  Cl3- Cl3-B.随NaCl溶液浓度增大,Cl2+H2O  H++Cl-+HClO平衡逆移,Cl2溶解度减小 H++Cl-+HClO平衡逆移,Cl2溶解度减小C.随盐酸浓度增加Cl2与H2O的反应被抑制,生成Cl3-为主要反应从而促进Cl2溶解 D.由上述实验可知,H+浓度增大促进Cl2溶解,由此推知在稀硫酸中,随硫酸浓度增大Cl2的溶解度会增大 |
|||
答案 |
D | |||
| v福建省实践教学工作室 蔡实践 设计制作 v |