 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 物质结构与能量 | |
|---|---|
| 本卷共有试题:35 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
||
出处 |
2021北京西城4月 | |||
| 题干 | 元素周期律的发现是近代化学史上的一座里程碑。下列事实不能用元素周期律解释的是 A. Na2CO3溶液中加盐酸,产生气泡 B.常温下,形状和大小相同的Mg、Al与同浓度盐酸反应,Mg条更剧烈 C.气态氢化物的稳定性:H2O>H2S D. Cl2从NaBr溶液中置换出Br2 |
|||
答案 |
A | |||
| 题号 | 2 |
|
||
出处 |
2021东城期末 | |||
| 题干 | 已知Cl、Se、Br在元素周期表中的位置如下图所示。下列说法不正确的是 A.原子半径:Se>Br>Cl B.还原性:Br‒>Se2‒>Cl‒ C.酸性:HClO4>HBrO4>H2SeO4 D.气态氢化物的稳定性:HCl>HBr>H2Se |
|||
答案 |
B | |||
| 题号 | 3 |
|
||
出处 |
2021海淀期末 | |||
| 题干 | 短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素,Y的原子最外层只有1个电子,Z的单质晶体是应用最广泛的半导体材料。下列说法正确的是( ) A.原子半径:r(W)>r(Z)>r(Y)>r(X) B.Z的非金属性比X的强 C.由X、Y组成的化合物中可能含有共价键 D.Z的最高价氧化物对应的水化物的酸性比W的强 |
|||
答案 |
C | |||
| 题号 | 4 |
|
||
出处 |
2021武汉4月 | |||
| 题干 | “嫦娥五号”带回了富含氦-3的月壤,氦-3可作为未来可控核聚变(3He+3He→4He+21H)的清洁能源。下列说法正确的是 A.氦-3聚变属于化学变化 B.3He和4He具有相同的性质 C.He位于第1周期第IIA族 D.2H和3He具有相同的中子数 |
|||
答案 |
D | |||
| 题号 | 5 |
|
||
出处 |
2021广州综合1 | |||
| 题干 | 2020年我国北斗三号全球卫星导航系统正式开通,其中“铷(Rb)原子钟”被誉为卫星的“心脏”,下列有关说法错误的是 A.铷元素位于IA族 B.铷的金属性比钠弱 C.8537Rb的中子数为48 D.8537Rb和8737Rb具有相同的电子数 |
|||
答案 |
B | |||
| 题号 | 6 |
|
||
出处 |
2021广州综合1 | |||
| 题干 | W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足X+Y=W+Z:化合物XW3与WZ相遇会产生白烟。下列叙述正确的是 A.单质的沸点:W>X B.元素X的含氧酸均为强酸 C.化合物YW中含有离子键 D.简单离子半径:Z>Y>X |
|||
答案 |
C | |||
| 题号 | 7 |
|
||
出处 |
2021深圳二研 | |||
| 题干 | NH4ClO4可用作火箭燃料,其分解反应为2NH4ClO4 N2↑+Cl2↑+2O2↑+4H2O。下列有关该反应中各微粒的描述错误的是 N2↑+Cl2↑+2O2↑+4H2O。下列有关该反应中各微粒的描述错误的是A.NH4ClO4为含有共价键的离子化合物 B.N2的电子式为 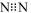 C.C1原子的M电子层有7个电子 D.16O2分子中的质子数与中子数之比为1:1 |
|||
答案 |
B | |||
| 题号 | 8 |
|
||
出处 |
2021深圳二研 | |||
| 题干 | W、X、Y、Z为短周期原子序数依次增大的主族非金属元素。已知W、X、Z分别位于不同周期,Y、Z最外层电子数相等,且Y和Z最外层电子数之和为X最外层电子数的3倍。下列说法错误的是 A.非金属性:Y>X>Z B.简单氢化物的沸点:Y>Z C.X、Y均能与W形成2种或2种以上的二元化合物 D.化合物XZ2中原子均为8电子稳定结构 |
|||
答案 |
A | |||
| 题号 | 9 |
|
||
出处 |
2021广州综合2 | |||
| 题干 | “嫦娥五号”成功着陆月球,实现了中国首次月球无人采样返回。月壤中的3He可用于核 聚变,下列说法正确的是 A.3He和4He核外电子数相等 B. 3He和4He是同种核素 C.3He和4He中子数相等 D.由3He组成的单质为3He2 |
|||
答案 |
A | |||
| 题号 | 10 |
|
||
出处 |
2021广州综合2 | |||
| 题干 | 一种矿石(Z2X2Y5・W2Y)的组成元素W、X、Y、Z为原子序数依次增大的短周期元素,Z单质燃烧发出耀眼的白光,X原子L层比K层多一个电子,W2Y分子中含有10个电子。下列说法正确的是 A.原子半径:Z>Y>X>W B.常温常压下单质沸点:W>Y>X C.Z与Y可形成共价化合物ZY D.X的最高价氧化物的水化物是弱酸 |
|||
答案 |
D | |||
| 题号 | 11 |
|
||
出处 |
2021河北高考 | |||
| 题干 | 用中子轰击ZNX原子产生α粒子(即氮核42He)的核反应为:ZNX+01n→7pY+42He He。已知元素Y在化合物中呈+1价。下列说法正确的是 A.H3XO3可用于中和溅在皮肤上的NaOH溶液 B.Y单质在空气中燃烧的产物是Y2O2 C.X和氢元素形成离子化合物 D.6Y和7Y互为同素异形体 |
|||
答案 |
A | |||
| 题号 | 12 |
|
||
出处 |
2021泉州三检 | |||
| 题干 | X、Y、Z、W 为原子序数依次增大的短周期元素,X 原子最外层电子数是其电子层数的2 倍, X、Y 的核电荷数之比为3∶4,金属单质Z 在空气中燃烧生成的化合物可与水发生氧化还原反应,W 的最高价氧化物的水化物具有两性。下列说法正确的是 A.最简单氢化物的稳定性:X>Y B.原子半径大小:W>Z>Y>X C.X、W 的最高价氧化物的水化物可发生反应 D.X、Y、Z 形成的化合物存在离子键和共价键 |
|||
答案 |
D | |||
| 题号 | 13 |
|
||
出处 |
2021全国乙卷 | |||
| 题干 | 我国嫦娥五号探测器带回1.73 kg的月球土壤,经分析发现其构成与地球士壤类似土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15。X、Y、Z为同周期相邻元素,且均不与W同族,下列结论正确的是 A.原子半径大小顺序为W>X>Y>Z B.化合物XW中的化学键为离子键 C.Y单质的导电性能弱于Z单质的 D.Z的氧化物的水化物的酸性强于碳酸 |
|||
答案 |
B | |||
| 题号 | 14 |
|
||
出处 |
2021全国甲卷 | |||
| 题干 | W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正确的是 A.原子半径:Z>Y>X>W B.W与X只能形成一种化合物 C.Y的氧化物为碱性氧化物,不与强碱反应 D.W、X和Z可形成既含有离子键又含有共价键的化合物 |
|||
答案 |
D | |||
| 题号 | 15 |
|
||
出处 |
2021南京六校一检 | |||
| 题干 | 短周期主族元素W、X、Y、Z的原子序数依次增大,W的原子序数是Z的原子序数的一半,W、X、Y三种元素形成的化合物M结构如图所示。 下列叙述正确的是 A.原子半径:Z>X>W B.气态氢化物的稳定性:Z>W>Y C.Y的最高价氧化物的水化物可溶于X和Z的最高价氧化物的水化物 D.化合物M中所有的原子均满足8电子稳定结构  |
|||
答案 |
D | |||
| 题号 | 16 |
|
||
出处 |
2020广州二测 | |||
| 题干 | 一种化合物Y2ZW3X可用作牙膏的添加剂,W、X、Y、Z为原子序数依次增大的短周期主族元素,其中Z的最高价氧化物的水化物是三元酸,Y的原子半径是短周期主族元素中最大的,W与X的最外层电子数之和为13。下列说法错误的是( ) A.简单氢化物的沸点:W>X B.离子半径:Y>W>X C.Z的最高价氧化物可用作干燥剂 D.Y与X形成的化合物的水溶液呈碱性 |
|||
答案 |
B | |||
| 题号 | 17 |
|
||
出处 |
2020北京高考 | |||
| 题干 | 已知:33As(砷)与P为同族元素。下列说法不正确的是 A.As原子核外最外层有5个电子 B.AsH3的电子式是  C.热稳定性:AsH3<PH3 D.非金属性:As<Cl |
|||
答案 |
B | |||
| 题号 | 18 |
|
||
出处 |
2020浙江1月 | |||
| 题干 | 有共价键的离子化合物是 A. Na2O2 B. H2SO4 C. CH2Cl2 D. SiC |
|||
答案 |
A | |||
| 题号 | 19 |
|
||
出处 |
2020全国II卷 | |||
| 题干 | 一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是 A.该化合物中,W、X、Y之间均为共价键 B.Z的单质既能与水反应,也可与甲醇反应 C.Y的最高化合价氧化物的水化物为强酸 D.X的氟化物XF3中原子均为8电子稳定结构 |
|||
答案 |
D | |||
| 题号 | 20 |
|
||
出处 |
2020全国III卷 | |||
| 题干 | W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足X+Y=W+Z;化合物XW3与WZ相遇会产生白烟。下列叙述正确的是 A.非金属性:W> X>Y> Z B.原子半径:Z>Y>X>W C.元素X的含氧酸均为强酸 D.Y的氧化物水化物为强碱 |
|||
答案 |
D | |||
| 题号 | 21 |
|
||
出处 |
2019北京高考 | |||
| 题干 | 2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(37Rb)同周期。下列说法不正确的是 A.In是第五周期第ⅢA族元素 B. 11549In的中子数与电子数的差值为17 C.原子半径:In>Al D.碱性:In(OH)3>RbOH |
|||
答案 |
D | |||
| 题号 | 22 |
|
||
出处 |
2019海南 | |||
| 题干 | 今年是门捷列夫发现元素周期表150周年,联合国将2019年定为“国际化学元素周期表年”,下列有关化学元素周期表的说法正确的是 A.元素周期表共有18列 B.ⅦA族元素的非金属性自上而下依次减弱 C.主族元素均呈现与其族数相同的最高化合价 D.第二周期主族元素的原子半径自左向右依次增大 |
|||
答案 |
AB | |||
| 题号 | 23 |
|
||
出处 |
2019海南 | |||
| 题干 | 自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题: (1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”。元素Mc可由反应  + + → → +3 +3 得到。该元素的质子数为 , 得到。该元素的质子数为 , 与 与 互为 。 互为 。(2)Mc位于元素周期表中第VA族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式 ,该分子内存在的共价键类型有 。 (3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的分子式为 ,+5价简单含氧酸的分子式为 。 |
|||
答案 |
(1)115 同位素 (2)  极性键和非极性键 极性键和非极性键(3)P2O3 H3PO4 |
|||
| 题号 | 24 |
|
||
出处 |
2019浙江1月学业考 | |||
| 题干 | 冰毒有剧毒,人体摄入后将严重损害心脏、大脑组织甚至导致死亡,严禁吸食。它的分子式为C10H15N,其中的氮元素在周期表中处于 A.第IIA族 B.第IIIA族 C.第IVA族 D.第VA族 |
|||
答案 |
D | |||
| 题号 | 25 |
|
||
出处 |
2019浙江1月学业考 | |||
| 题干 | 四种短周期主族元素X、Y、Z和M在周期表中的位置如图所示。下列说法正确的是 A.原子半径(r):r(X)>r(Z) B.元素的非金属性:Y>M C.Y元素的最高化合价为+7价 D.Z的最高价氧化物的水化物为强酸 |
|||
答案 |
B | |||
| 题号 | 26 |
|
||
出处 |
2019全国联考 | |||
| 题干 | a、b、c、d为短周期主族元素,原子序数依次增大。a原子最外层电子数等于电子层数的3倍;a和b能组成两种常见的离子化合物,其中一种含非极性键;d的最高价氧化物对应的水化物和简单氢化物都是强酸。向d的简单氢化物的水溶液中逐滴加入bca2溶液,开始没有沉淀;随着bca2溶液的不断滴加,逐渐产生白色沉淀。下列推断正确的是 A.原子半径:b>c>a B.最高价氧化物对应水化物的碱性:b<c C.工业上电解熔融cd3可得到c的单质 D.向b2a2中加入cd3溶液一定不产生沉淀 |
|||
答案 |
A | |||
| 题号 | 27 |
|
||
出处 |
2019西城上期末 | |||
| 题干 | 下列性质的比较,不能用元素周期律解释的是( ) A.原子半径:S>Cl B.热稳定性:Na2CO3>NaHCO3 C.还原性:I->Br- D.酸性:H2SO4>H3PO4 |
|||
答案 |
B | |||
| 题号 | 28 |
|
||
出处 |
2018海淀二模 | |||
| 题干 | 三氟化氮(NF3)常用于微电子工业,可用以下反应制备: 4NH3+3F2=NF3+3NH4F 下列说法中,正确的是 A.NF3的电子式为  B.NH4F分子中仅含离子键 B.NH4F分子中仅含离子键C.在制备NF3的反应中,NH3表现出还原性 D.在制备NF3的反应中,各物质均为共价化合物 |
|||
答案 |
C | |||
| 题号 | 29 |
|
||
出处 |
2019广州调研 | |||
| 题干 | 短周期主族元素W、X、Y和Z的原子序数依次增大,W的气态氢化物的水溶液可使酚酞变红,W与X可形成一种红棕色有刺激性气味的气体,Y的原子半径是所有短周期主族元素中最大的,Z原子最外层电子数与W原子的电子总数相同。下列说法中正确的是 A.W的氧化物对应水化物均为强酸 B.简单离子半径:W<X<Y C.简单氢化物沸点:Z<W D.Y与Z形成的化合物的水溶液呈碱性 |
|||
答案 |
C | |||
| 题号 | 30 |
|
||
出处 |
2018郑州一模 | |||
| 题干 | a、b、c、d、e 为原子序数依次增大的短周期主族元素,a原子核外电子数总数与b 原子次外层电子数相同;C所在周期数与族序数相同;d与a同族。下列叙述正确的是 A. 含氧酸的酸性:e>d B. 原子半径:b>c>d>a C. 由a 和b 两种元素形成的化合物不可能含共价键 D. b、c 元素对应最高价氧化物的水化物之间不可能发生反应 |
|||
答案 |
B | |||
| 题号 | 31 |
|
||
出处 |
2018泉州单科质检 | |||
| 题干 | 下列事实不能说明氯的非金属性强于硫的是 A.酸性:HClO3>H2SO3 B.稳定性:HCl>H2S C.3Cl2+2Fe  2FeCl3和S+Fe 2FeCl3和S+Fe FeS D.Cl2+H2S=S↓+2HCl FeS D.Cl2+H2S=S↓+2HCl |
|||
答案 |
A | |||
| 题号 | 32 |
|
||
出处 |
2018全国III卷 | |||
| 题干 | W、X、Y和Z为原子序数依次增大的四种短周期元素。W与X可生成一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;Z原子最外层的电子数与W的电子总数相同。下列叙述正确的是 A.X与其他三种元素均可形成两种或两种以上的二元化合物 B.Y与其他三种元素分别形成的化合物中只含有离子键 C.四种元素的简单离子具有相同的电子层结构 D.W的氧化物对应的水化物均为强酸 |
|||
答案 |
A | |||
| 题号 | 33 |
|
||
出处 |
2017天津高考 | |||
| 题干 | 根据元素周期表和元素周期律,判断下列叙述不正确的是 A.气态氢化物的稳定性:H2O>NH3>SiH4 B.氢元素与其他元素可形成共价化合物或离子化合物 C.图1所示实验可证明元素的非金属性:Cl>C>Si D.用中文“ 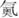 ”(ào)命名的第118号元素在周期表中位于第七周期0族 ”(ào)命名的第118号元素在周期表中位于第七周期0族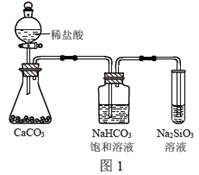 |
|||
答案 |
C | |||
| 题号 | 34 |
|
||
出处 |
2017泉州二检 | |||
| 题干 | 已知X、Y、Z为原子序数依次增大的短周期元素,它们分别位于不同周期不同主族。一定条件下存在如图转化关系,其中A能使湿润的红色石蕊试纸变蓝。下列说法不正确的是 A.Y元素位于周期表第二周期第VA族 B.以上三个反应均属于化合反应 C.C可能是共价化合物 D.Z元素的最高价氧化物的水化物为强酸 |
|||
答案 |
C | |||
| 题号 | 35 |
|
||
出处 |
2016浙江高考 | |||
| 题干 | 短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是其电子层数的2倍,X、Y的核电荷数之比为3:4。W−的最外层为8电子结构。金属单质Z在空气中燃烧生成的化合物可与水发生氧化还原反应。下列说法正确的是 A.X与Y能形成多种化合物,一般条件下都能与Z的最高价氧化物的水化物发生反应 B.原子半径大小:X<Y,Z>W C.化合物Z2Y和ZWY3都只存在离子键 D.Y、W的某些单质或两元素之间形成的某些化合物可作水的消毒剂 |
|||
答案 |
D | |||
| v福建省实践教学工作室 蔡实践 设计制作 v |