 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 高一必修一单元检测 | |
|---|---|
| 本卷共有试题:27 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
||
出处 |
2014上海高考 | |||
| 题干 | “玉兔”号月球车用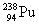 作为热源材料,下列关于 作为热源材料,下列关于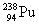 的说法正确的是 的说法正确的是A. 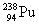 与 与 互为同位素 B. 互为同位素 B.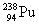 与 与 互为同素异形体 互为同素异形体C. 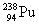 与 与 具有完全相同的化学性质 D. 具有完全相同的化学性质 D.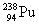 与 与 具有相同的最外层电子 具有相同的最外层电子 |
|||
答案 |
D | |||
| 题号 | 2 |
|
||
出处 |
2012泉州测试 | |||
| 题干 | 某微粒的结构示意图为 ,它表示 ,它表示A.氧原子 B.氧离子 C.氖原子 D.钠离子 |
|||
答案 |
B | |||
| 题号 | 3 |
|
||
出处 |
2009广东会考 | |||
| 题干 | S是元素周期表中第16号元素,下列正确表示S的原子结构示意图的是    |
|||
答案 |
C | |||
| 题号 | 4 |
|
||
出处 |
2014泉州测试 | |||
| 题干 | 下列说法错误的是 A.摩尔是物质的量的单位 B.国际上规定, 0.012kg 12C原子所含有的碳原子数目的物质的量为1摩 C.1 mol H2的质量是 2 g,它所占的体积是 22.4 L D.硫酸根离子的摩尔质量的单位是 96g/mol |
|||
答案 |
C | |||
| 题号 | 5 |
|
||
出处 |
2012广东会考 | |||
| 题干 | 常温下,2L物质的量浓度为0.5mol・L-1KOH溶液含有 A. 0.5mol的K+ B.0.5mol的H+ C.1.0mol的H+ D.1.0mol的OH- |
|||
答案 |
A | |||
| 题号 | 6 |
|
||
出处 |
2014泉州测试 | |||
| 题干 | 胶体区别于其它分散系最本质的特征是 A.外观澄清、透明 B.胶体粒子直径在1~100nm之间 C.丁达尔现象 D.分散质粒子能透过半透膜 |
|||
答案 |
B | |||
| 题号 | 7 |
|
||
出处 |
未知 | |||
| 题干 | 配制500mL 2mol/L NaOH溶液所需NaOH的质量为 A. 40g B. 20g C. 50g D. 80g |
|||
答案 |
A | |||
| 题号 | 8 |
|
||
出处 |
2011上海高考 | |||
| 题干 | 氯元素在自然界有35Cl和37Cl两种同位素,在计算式34.969×75.77%+36.966×24.23% =35.453中 A.75.77%表示35Cl的质量分数 B.24.23%表示35Cl的丰度 C.35. 453表示氯元素的相对原子质量 D.36.966表示37Cl的质量数 |
|||
答案 |
C | |||
| 题号 | 9 |
|
||
出处 |
2008四川高考 | |||
| 题干 | 已知aXm+和bYn-两种离子的电子层结构相同,则a等于 A.b+m+n B.b+m-n C.b-m+n D.b-m-n |
|||
答案 |
A | |||
| 题号 | 10 |
|
||
出处 |
未知 | |||
| 题干 | 能证明胶粒比溶液中溶质的微粒直径大的实验是 A、电泳 B、渗析 C、过滤 D、布朗运动 |
|||
答案 |
B | |||
| 题号 | 11 |
|
||
出处 |
2014龙岩理综质检 | |||
| 题干 | 既能用浓硫酸又能用碱石灰干燥的气体是 A.Cl2 B.SO2 C.CO D.NH3 |
|||
答案 |
C | |||
| 题号 | 12 |
|
||
出处 |
2005泉州跟踪 | |||
| 题干 | 在标准状况下,8 g某气体的分子数与22 g二氧化碳的分子数相等,则该气体的密度是 A、0.714 g / mL B、0.714 g / L C、0.179 g / L D、0.357 g / L |
|||
答案 |
B | |||
| 题号 | 13 |
|
||
出处 |
2011海淀期中 | |||
| 题干 | 同温同压下,等体积的两容器内分别充满14N16O和13C16O气体,下列对两容器中气体判断正确的是 A.中子数相同 B.分子数不同 C.质子数相同 D.气体质量相同 |
|||
答案 |
A | |||
| 题号 | 14 |
|
||
出处 |
未知 | |||
| 题干 | 经测量a滴水的体积为bmL,则1滴水中所含的分子数为 A.a×b×18×6.02×1023 B.  ×6.02×1023 ×6.02×1023C.  ×6.02×1023 D. ×6.02×1023 D.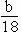 ×6.02×1023 ×6.02×1023 |
|||
答案 |
B | |||
| 题号 | 15 |
|
||
出处 |
未知 | |||
| 题干 | 1gN2中含有x个原子,则阿伏加德罗常数是 A、(x/28)mol-1 B、14x mol-1 C、(x/14)mol-1 D、28x mol-1 |
|||
答案 |
D | |||
| 题号 | 16 |
|
||
出处 |
2007全国I卷 | |||
| 题干 | 在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是 A、 p(Ne)>p(H2)>p(O2) B、 p(O2)>p(Ne)>p(H2) C、 p(H2)>p(O2)>p(Ne) D、 p(H2)>p(Ne)>p(O2) |
|||
答案 |
D | |||
| 题号 | 17 |
|
||
出处 |
未知 | |||
| 题干 | 下列各物质所含原子数目,按由大到小顺序排列的是 ①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL水 ④0.2mol H3PO4 A.①④③② B.④③②① C.②③④① D.①③④② |
|||
答案 |
A | |||
| 题号 | 18 |
|
||
出处 |
未知 | |||
| 题干 | a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是 A、22.4bc/(NA・a) L B、22.4ab/(NA・c) C 、22.4ac/(NA・b) L D、22.4b/(NA・ac)L |
|||
答案 |
A | |||
| 题号 | 19 |
|
||
出处 |
未知 | |||
| 题干 | 标准状况下,112 mL某气体的质量是0.17 g,该气体可能是 A. O2 B. N2 C. H2S D. CO2 |
|||
答案 |
C | |||
| 题号 | 20 |
|
||
出处 |
未知 | |||
| 题干 | 在一定温度和压强下,气体体积主要取决于 A 气体分子间的平均距离 B 气体分子微粒大小 C 气体分子数目的多少 D 气体分子式量的大小 |
|||
答案 |
C | |||
| 题号 | 21 |
|
||
出处 |
1998全国高考 | |||
| 题干 | 将标准状况下的a升氯化氢气体溶于100克水中,得到的盐酸的密度为b克/毫升,则该盐酸的物质的量的浓度是 A、  B、 B、  C、  D、 D、  |
|||
答案 |
D | |||
| 题号 | 22 |
|
||
出处 |
2008全国Ⅱ卷 | |||
| 题干 | 某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子。在a g H mX中所含质子的物质的量是 A.  mol B. mol B. mol molC.  mol D. mol D. mol mol |
|||
答案 |
A | |||
| 题号 | 23 |
|
||||||||||||||||||||
出处 |
2014上海高考 | |||||||||||||||||||||
| 题干 | 右图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是
|
|||||||||||||||||||||
答案 |
C | |||||||||||||||||||||
| 题号 | 24 |
|
||
出处 |
未知 | |||
| 题干 | 已知NH3难溶于CCl4,如下图所示,下列装置中,不宜用于吸收氨气的是 |
|||
答案 |
B | |||
| 题号 | 25 |
|
||
出处 |
2010广州测试 | |||
| 题干 | 下列制备和收集气体的实验装置合理的是   A.用氯化铵和氢氧化钙制NH3 B.用铜片和稀硝酸制NO  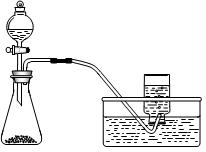 C.用锌粒和稀硫酸制H2 D.用双氧水和二氧化锰制O2 |
|||
答案 |
D | |||
| 题号 | 26 |
|
||
出处 |
2005泉州跟踪 | |||
| 题干 | 实验室要配制1mol/L的稀硫酸250mL,回答下列问题: (1)需要98%密度为1.84g/cm3的浓硫酸 mL (2)配制时,必须使用的仪器有 (填代号) ①烧杯 ②100 mL量筒 ③20 mL量筒 ④1000 mL容量瓶 ⑤250 mL容量瓶 ⑥托盘天平(带砝码) ⑦玻璃棒 还缺少的仪器是 。 (3)配制时,该实验两次用到玻璃棒,其作用分别是 、 。 (4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不影响”) ①没有洗涤烧杯和玻璃棒。 。 ②如果加水超过了刻度线,取出水使液面恰好到刻度线。 。 ③容量瓶没有干燥。 |
|||
答案 |
(1)13.6;①③⑤⑦;胶头滴管 (2)搅拌、引流 (3)偏低、偏低、无影响 |
|||
| 题号 | 27 |
|
||
出处 |
2012宁德质检 | |||
| 题干 | 某化学兴趣小组制备饱和氯水并对饱和氯水与碳酸钙的反应进行研究。 【实验一】制备饱和氯水,使用以下装置并在装置中加入相应试剂,按要求进行操作。请回答:  (1)A装置中发生反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+2H2O+Cl2↑。 MnCl2+2H2O+Cl2↑。往100mL 12mol・L-1的浓盐酸中加入足量二氧化锰并加热,充分反应后,被氧化HCl的物质的量为 A.小于0.6 mol B.等于0.6 mol C.大于0.6 mol D.等于1.2 mol (2)B装置可以除去Cl2气体中的HCl,作用原理是 。 (3)D装置的作用是 。 (4)E装置的作用是 。 (5)若将E装置改成右图所示装置进行实验,可以省去D装置,请解释原因: 。  【实验二】探究饱和氯水与CaCO3的反应。步骤如下: ①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应。有少量气泡产生,溶液浅黄绿色褪去; ②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强; ③为了确定反应产物,将滤液分为三份,分别进行以下实验: 第一份与石灰水混合,立即产生大量白色沉淀; 第二份与稀盐酸混合,立即产生大量无色气体; 第三份进行加热,看到溶液变浑浊且有大量无色气体产生。 经检测,上述实验中产生的无色气体均为CO2。请回答: (6)步骤①为什么浅黄绿色会退去 (7)反应后所得的溶液漂白性增强的原因是 ; (8)依据上述实验可推知,②的滤液中的溶质除CaCl2、HClO外,还含有 。  |
|||
答案 |
(1)A (2)氯化氢可溶于饱和食盐水中,氯气不溶于饱和食盐水中,这样就可以除去氯气中的氯化氢 (3)防止倒吸。 (4)吸收氯气,防止其污染空气 (5)氯气不溶于四氯化碳中,所以不会引起倒吸 (6)氯气中的成分与碳酸钙反应,所以颜色会退去 (7)因为这时起漂白作用的是次氯酸 (8)碳酸氢钙[ Ca(HCO3)2] |
|||
| v福建省实践教学工作室 蔡实践 设计制作 v |