 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| Ȫ����2021����б�ҵ��������⣨���� | |
|---|---|
| �����������⣺15 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2021Ȫ������ | |||
| ��� | ��ѧ��������������ɳ�����չ������ء�����˵��������� A��Ư�۵���Ч�ɷ�Ϊ������ơ���������B����ʳ�ؽ������ӿɺ���ţ�̽ⶾ C��SO2 ������Ư���Ϳ�����������������D����ҵ�ϳ��������MgO ұ��Mg |
|||
�� |
D�� | |||
| ��� | 2 |
|
||
���� |
2021Ȫ������ | |||
| ��� | �����Ƽ���Ҫ��ӦΪNaCl��H2O��NH3��CO2=NaHCO3����NH4Cl������˵��������� A��CO2 �ĵ���ʽ��  �������������������� B��Na+�Ľṹʾ��ͼ�� �������������������� B��Na+�Ľṹʾ��ͼ�� C��������Ӧ�IJ����Ϊ���ӻ��������������D���ܽ�ȣ�NH4HCO3��NaHCO3 |
|||
�� |
A�� | |||
| ��� | 3 |
|
||
���� |
2021Ȫ������ | |||
| ��� | ���ɽ�������ȡ�Ħ£���ϩ����ȡŵ��ͪ��ŵ����ȣ���Ӧԭ�����£� �������£���ϩ���������� ŵ��ͪ���������� ŵ���ᡡ�������� ����� ����˵����ȷ���� A���£���ϩ��ij��ͬ���칹������Ƿ����� B��ŵ��ͪ����������̼ԭ�ӿ��ܹ�ƽ�� C��ŵ���������������NaHCO3 ��Һ���� D�����������л����������ˮ |
|||
�� |
C�� | |||
| ��� | 4 |
|
||
���� |
2021Ȫ������ | |||
| ��� | NA ��ʾ����٤����������ֵ������˵����ȷ���� A��14.0 g ��N2 ��CO �Ļ�������к���NA��ԭ�� B��0.1 mol��L−1 NaHCO3 ��Һ�к���HCO 3������С��0.1NA C��0.5 mol N2 ��1.5 mol H2 ��ַ�Ӧ�ɵ�NH3 ������ΪNA D��2.24 L ��Cl2 ��NaOH ��Һ��ȫ��Ӧ��ת�Ƶĵ�����Ϊ0.2NA�� |
|||
�� |
A�� | |||
| ��� | 5 |
|
||
���� |
2021Ȫ������ | |||
| ��� | X��Y��Z��W Ϊԭ��������������Ķ�����Ԫ�أ�X ԭ������������������Ӳ�����2 ���� X��Y �ĺ˵����֮��Ϊ3��4����������Z �ڿ�����ȼ�����ɵĻ��������ˮ����������ԭ��Ӧ��W ������������ˮ����������ԡ�����˵����ȷ���� A������⻯����ȶ��ԣ�X��Y B��ԭ�Ӱ뾶��С��W��Z��Y��X C��X��W ������������ˮ����ɷ�����Ӧ D��X��Y��Z �γɵĻ�����������Ӽ����ۼ� |
|||
�� |
D�� | |||
| ��� | 6 |
|
||||||||||||||||||||
���� |
2021Ȫ������ | |||||||||||||||||||||
| ��� | ����ʵ�����������ͽ��۶���ȷ����
|
|||||||||||||||||||||
�� |
B���� | |||||||||||||||||||||
| ��� | 7 |
|
||
���� |
2021Ȫ������ | |||
| ��� | ʵ��������ʯ��[��Ҫ�ɷ�ΪCaSO4��������SiO2��Ca3(PO4)2 ������]Ϊԭ���Ʊ�����CaCO3����������ͼ������˵��������� A����ת�����У�������ӦCaSO4 ��CO23��= SO24����CaCO3 B������Һ����pH ԼΪ6.5����������Ҫ��SO 24����CO23�� C�����������ա���Ҫ�������оƾ���ơ�����������ǯ�������ǡ����żܵ� D������ȡ��ʱ���ʵ������¶�������Ca2���Ľ��� |
|||
�� |
B�� | |||
| ��� | 8 |
|
||
���� |
2021Ȫ������ | |||
| ��� | ����ZnBr2/SiO2 Ϊ������ͨ�����廯�ɽ�����ת��Ϊ����顣��·��ʵ���˼���ĵ��»����Ч���ƻ��ò�������������������߲����ѡ���ԣ��䷴Ӧ������ͼ��ʾ������˵��������� A������FeBr2 �滻ZnBr2�������IJ��ʽ����� B�������п��ܻ���CH2Br2 C�����̢����������뻹ԭ�������ʵ���֮��Ϊ2��1 D���ܷ�ӦΪ2CH4��2HBr��O2 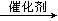 2CH3Br��2H2O 2CH3Br��2H2O
 |
|||
�� |
C���� | |||
| ��� | 9 |
|
||
���� |
2021Ȫ������ | |||
| ��� | ˫��Ĥ��BP����һ���ܽ�ˮ���ӽ����H����OH�����������ӽ���Ĥ��Ӧ��˫��Ĥ��ȡ�ۺ���������ˮ��[Fe2(OH)n(SO4)3-n/2]m��PFS���ĵ绯ѧװ����ͼ��ʾ������˵��������� A��M Ϊ�����ӽ���Ĥ����ΪOH�� B���缫a �ĵ缫��ӦʽΪ2H�� ��2e�� = H2�� C�������ܶȹ���ʹPFS ��Ʒ�������� D�����Ƶ�1 mol [Fe(OH)SO4]3��������ת�Ƶĵ���Ϊ2 mol |
|||
�� |
D �� | |||
| ��� | 10 |
|
||
���� |
2021Ȫ������ | |||
| ��� | ��100 mL 5.0 mol��L−1 ��NaOH ��Һ��ͨ��H2S ���壬�������ڲ�ͬpH ��Һ�еķֲ�ϵ�����ģ���ͼ��ʾ������˵����ȷ����A������M ��ʾpH ��HS−�ı仯��ϵ B��S2−��H+  ��HS−��ƽ�ⳣ��������Ϊ1014 ��HS−��ƽ�ⳣ��������Ϊ1014C��HS−�ĵ���̶ȴ���ˮ��̶� D������Na2S ��Һʱ�ɽ�Na2S ����ֱ������ˮ |
|||
�� |
B | |||
| ��� | 11 |
|
||
���� |
2021Ȫ������ | |||
| ��� | �о���̫���ܵ�ص��ڻ������ղ㣨��Ҫ��CdTe��CdS���л����ھ�����Ҫ�����塣ij���չ��յ��������£� �ش��������⣺ ��1��FeOOH ��Fe Ԫ�صĻ��ϼ�Ϊ�� �� ��2����Ӧ���У���Һ��pH���¶ȣ�T�������ɳ����Ĺ�ϵ����ͼ��ͼ������ֱ��ʾ���Ļ������ȶ����ڵ��������Ʊ�FeOOH ���˵�pH ���¶ȷֱ�Ϊ�� �����ţ���  ����a��2��80�� b��4��90�桡�� c��5��160�桡���������� d��6��25�� ��3���Ʊ�������������ʱ������NaBH4 ǰ��ͨ��N2 ������������������ ��4���ڻ������ղ��е�CdTe ���뷴Ӧ�Ļ�ѧ����ʽΪ�����������������е�һ�ֵ����������� ��5�������£����ں�Cd2+��Te4+��Һ�м���NaOH ��Һ����pH Ϊ7����Һ��c(Cd2+)�����ֵΪ���������� ����֪��Ksp[Cd(OH)2]=5.3��10−15�� ��6����TeO32����Һ�õ�������Te���������������������������������������������� |
|||
�� |
��1��+3 ��2��b ��3�����߿�����������������ֹNaBH4������������������ ��4��CdTe��3H2O2��3H2SO4=CdSO4��Te(SO4)2��6H2O S ��5��0.53mol��L−1 ��6����ԭ�ԡ������ԣ�����ԣ� 1 |
|||
| ��� | 12 |
|
||
���� |
2021Ȫ������ | |||
| ��� | ij��ȤС�����ʵ��̽��SO2 ������Cu(OH)2 ����Һ��Ӧ�IJ�� ��ͼ���Ӻ�װ�ã��г�װ��ʡ�ԣ����Ž�����������20 mL1.00 mol��L−1 ��CuCl2 ��Һ�м���20 mL 2.00 mol��L−1 ��NaOH ��Һ����ͨ��һ����SO2��������ƿ�����ɴ�����ɫ����X���ش��������⣺ ��1�����������ƺ�Ũ����Ϊԭ����ȡSO2�������Ӧѡ���������������A����B��)װ�ã�ͨ��SO2 �����в��Ͻ����Ŀ��������������  ��2������a ������Ϊ�����������������ձ��з�����Ӧ�����ӷ���ʽΪ������������ ��3����SO2 ������������Ʋ�X ����Ϊ����������ȡ����X ����ϡ���������֤���۲쵽�� ��������˵�����Ʋ���� ��4����SO2 �Ļ�ԭ�ԣ��Ʋ�X ����ΪCuCl����������֤ʵ�顣 ��ȡ������X���ӹ����İ�ˮ�ܽ⣬¶���ڿ�����Ѹ�ٵõ�����ɫ��Һ�����������ӵĻ�ѧʽΪ������������������ �� ��������ɫ��Һ���ȼ�������������������� ���ٵμ������������� ��Һ��������ɫ������ ������X �����ӷ���ʽΪ������������ |
|||
�� |
��1��B ����Ӵ�������ӿ췴Ӧ���ʣ�ʹ�����ܳ�ַ�Ӧ ��2������� SO2��2OH��=SO32����H2O ��3��CuSO3�� �����ݲ�����������������Ⱥ����𰸣� ��4��ϡ���ᣬAgNO3��Һ CuCl2Cu(OH)2 ��SO2 ��2Cl��=2CuCl��SO��2H2O |
|||
| ��� | 13 |
|
||||||||
���� |
2021Ȫ������ | |||||||||
| ��� | �о��״��ĺϳɷ�������;������Ҫ�ļ�ֵ�� ��. ���úϳ�����CO ��H2���ϳɼ״����������·�Ӧ�� ��CO(g)��2H2(g)  ��CH3OH(g)���� ��H ��CH3OH(g)���� ��H��1����Ԫ�����ȶ��ĵ�������1mol ��������ʱ�ķ�Ӧ�ȳ�Ϊ�û�����ı�Ħ�������ʣ���Hf�����������ʵı�Ħ�����������±�����H=������������ kJ��mol−1��
��3��T ��ʱ�����ܱյĸ��������У������ʵ���֮��1��1 ����CO ��H2����ƽ��ʱ��������ѹΪp Pa��H2 ��ת����Ϊ50%����T ��ʱ��������Ӧ��ƽ�ⳣ��Kp=������������ Pa−2�� ���ú�p�Ĵ���ʽ��ʾ��Kp Ϊ�÷�ѹ��ʾ��ƽ�ⳣ������ ��. �״�Ҳ����ͨ����������Ӧ�ϳɣ�װ������ͼ��ʾ����  ��4��ʯī�缫�ϵĵ缫��ӦʽΪ������ϵ���¶����ߵ�һ���̶ȣ��缫��Ӧ�����ʷ���Ѹ���½�����Ҫԭ���������������������������� ��. �״�����ˮ�ƶ����������ܵ���ע����Ӧ����ʽΪ�� 2CH3OH(g) ��CH3OCH3(g)��H2O(g) ��H��0��ij����Ӧ�Ļ������£� ����i��CH3OH(g)�� CH3OH�� ���̢���CH3OH��CH3OH�� ��CH3OCH3��H2O�� ���̢������� ����iv��H2O��  H2O(g) ���������У����������������ڴ��������ϡ� H2O(g) ���������У����������������ڴ��������ϡ���5��Ϊ���CH3OH ��ƽ��ת���ʣ��ɲ��õĴ�ʩ���������� �� ����A���ݻ����䣬����һ����He������ B����ʱ�����H2O(g) ����C����һ���Ľ�������������������D�����ͷ�Ӧ�¶� ��6�����̢����������������������������� |
|||||||||
�� |
��1����90.64 ��2���� ��3��3/p2�� ��4��CO2��6H+��6e��=CH3OH��H2O ���������¶ȹ��ߣ�����ʧȥ������ ��5��BD ��6��CH3OCH3������CH3OCH3(g) �� |
|||||||||
| ��� | 14 |
|
||
���� |
2021Ȫ������ | |||
| ��� | LiBH4��MgH2��AlH3 ��һ�־��������������ܵ���Ԫ���ϴ�����ϡ� �ش��������⣺ ��1������˵����ȷ�������������������ţ��� ����A���ò����У�����Ԫ�صĻ�̬ԭ�Ӷ�û�гɶԵ�p ���� ����B���ò����У�����Ԫ�صĵ縺��������H ����C��Li+�����ӿɷ���ԾǨ����Li+����ʱ����Ϊ��ɫ ����D��MgH2 �۵����AlH3��ԭ����Mg2+�뾶��Al3+С����H���γɵĻ�ѧ����ǿ ��2��BH4���Ŀռ乹��Ϊ��������������B ԭ�ӵĹ���ӻ���ʽΪ���������� ��3��LiBH4 �����к��е��������������������������ţ��� ����A�����Ӽ���������B���м� ������C�������������D����λ�� ��4���⻯þ��h��MgH2����һ�ֵ���Ķ�ά���ϣ���ά��������ͼ��ͼ1��  ��h��MgH2�У�M����λ��Ϊ������������ ��3��3��1 ��h��MgH2 �����У�Ϳ�ڴ���Mg ��Mn �滻���γɲ���h��MgH2��������ͼ2 ��ʾ��H ��ʡ�ԣ��Ļ�ѧʽΪ ���������������� |
|||
�� |
��1��B ��2���������塡����������sp3�ӻ��� ��3��AD ��4����6 ��Mg8MnH18 |
|||
| ��� | 15 |
|
||
���� |
2021Ȫ������ | |||
| ��� | ��ݨ�棨E����һ�����������ռ�����������ˮ���Է�ɹ��ױƷ��һ�������ԣ�A��Ϊ��ʼԭ�Ϻϳ���ݨ���·������ͼ��ʾ�� �ش��������⣺ ��1��A �Ĺ���������Ϊ���������� ����Ӧ��Ļ�ѧ����ʽΪ������ ��2����ķ�Ӧ����Ϊ������ ��3���й�C ��E ��˵����ȷ���������� ����a������ʹ���Ը��������Һ��ɫ ����b��1 mol E �������4 mol H2 �����ӳɷ�Ӧ ����c��C �к���6 ������̼ԭ�� ����d��������Ȼ�̼��Һ�ɼ���C ��E ��4����Ӧ��Ϊ�ӳɷ�Ӧ������������кͣ�����X��C8H6O2���Ľṹ��ʽΪ���� ��������Y ��X ��ͬ���칹�壬��˴Ź���������4 ��壬�������Ϊ1��2��2��1��Y ��FeCl3 ��Һ����ɫ��Y �Ľṹ��ʽΪ ������ ��������������дһ�֣��� |
|||
�� |
��1���ʻ� ��2����ȥ��Ӧ ��3��  ��ad�� ��ad�� ��4��  �� �� |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |