 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| 2021�����ʡ��ͨ����ѧҵˮƽѡ���Կ���ģ��������ѧ���� | |
|---|---|
| �����������⣺19 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | ��ѧ������ֶԷ����¹ڲ�����������Ҫ���ã�����һ����ҽ�ÿ��ֵ���Ҫԭ��Ϊ�۱�ϩ��֬������˵���������(������ ) A.�۱�ϩ�ṹ��ʽΪ  ���������� B.�ɱ�ϩ�ϳɾ۱�ϩ�ķ�Ӧ����Ϊ���۷�Ӧ ���������� B.�ɱ�ϩ�ϳɾ۱�ϩ�ķ�Ӧ����Ϊ���۷�ӦC.�۱�ϩΪ�����Ժϳ���֬���������� D.�۱�ϩ����Ȼ�����в������� |
|||
�� |
B | |||
| ��� | 2 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | 146C��˥�䷴ӦΪ �����˥��(��Ӧ����������ĵ����ʼ����һ����Ҫ��ʱ��)Ϊ5730�ꡣ����˵����ȷ����(������ ) �����˥��(��Ӧ����������ĵ����ʼ����һ����Ҫ��ʱ��)Ϊ5730�ꡣ����˵����ȷ����(������ )A. 146C��14ZX��Ϊͬλ�� B. 146C��14ZX����������ͬ C. 126C��146C�ļ۲������������2 D.ij������Ʒ��146C����ӦΪ��11460��ǰ��1/4 |
|||
�� |
D | |||
| ��� | 3 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | NAΪ�����ӵ�������ֵ������˵����ȷ����(������ ) A.1mol H2S�����У�Sԭ�ӵļ۲���Ӷ���ĿΪ4NA B.��״���£�2.24L������ķ�����Ϊ0.1NA C. 1L 0.01mol��L��1  ��Һ�У� ��Һ�У� �� �� ��������Ŀ֮��Ϊ0.01NA ��������Ŀ֮��Ϊ0.01NAD.�缫��ӦLiFePO4��xe-=xLi++Li1��xFePO4��ÿת��1 mol�����ͷ�2NA��Li+ |
|||
�� |
A | |||
| ��� | 4 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ��(������ ) A.��������ˮ�������Na2SO3��Һ�У�Br2+H2O+SO32-=2Br-+2H++SO42- B.������Fe2(SO4)3��Һ����Mg(OH)2��Һ�У�2Fe3++3 Mg(OH)2=2Fe(OH)3+3Mg2+ C.������SO2ͨ��K2S��Һ�У�5SO2+2S2-+2H2O=3S��+4HSO3- D.����������Һ������������Һ���ȣ� CH2OH(CHOH)4CHO+2[Ag(NH3)2]++2OH-  CH2OH(CHOH)4COO-+NH4++2Ag++3NH3+H2O CH2OH(CHOH)4COO-+NH4++2Ag++3NH3+H2O |
|||
�� |
A | |||
| ��� | 5 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | ������Ԫ��W��X��Y��Z��ԭ��������������W����������ḻ��Ԫ�أ�W2X��ά���������̵ı������ʣ�WY�����ڲ����Ŀ�ʴ��ZX2���������Ҫ�γ�ԭ��֮һ�������»�����ZY4�����塣����˵���������(������ ) A.Y�ĵ�һ������������Ԫ����������������� B.W2X��ZX2������ԭ�ӷֱ�Ϊsp3��sp2�ӻ� C. W2X�ķе����W2Z�ķе㡡������������ D. ZY4������ԭ�Ӿ�Ϊ8���ӽṹ |
|||
�� |
D | |||
| ��� | 6 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | �������ױ������л�С���ӿɴ����������ȡ����Ӧ��������ͼ��ʾ�� ����˵���������(������ ) A.2�Ǵ��� B.4��7���Ƿ�Ӧ�м��� C.2��4��ת���������зǼ��Լ��뼫�Խ��Ķ������γ� D.5Ϊ  ʱ��1�� ʱ��1�� |
|||
�� |
C | |||
| ��� | 7 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | �����л������� ������˵���������(������ ) ������˵���������(������ )A.����ʽΪC14H18O2 B.����2������̼ԭ�� C.�����ȵ�����������ͭ����Һ��Ӧ D.���л����ͬ���칹���������廯���� |
|||
�� |
D | |||
| ��� | 8 |
|
||||||||||||
���� |
2021������Ӧ���� | |||||||||||||
| ��� | ����ʵ�������װ����ȷ����(������ )
|
|||||||||||||
�� |
C | |||||||||||||
| ��� | 9 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | B��AlΪͬ��Ԫ�أ�����˵���������(������ ) A. BF3��AlF3��������F���γ���λ�� B. H3BO3Ϊ��Ԫ�ᣬAl(OH)3������ C.���ۼ��ķ�����ʹ����B�д��ԣ�ԭ�Ӳ����Ի���ʹ����Al����չ�� D. B��Al�ֱ���N�γɵĹ��۾��壬�����нϸ�Ӳ�Ⱥ��۵� |
|||
�� |
B | |||
| ��� | 10 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | �о����֣��������Ҵ�ȼ�ϵ���м������ᣬ��ʹ��س���������ŵ磬�乤��ԭ����ͼ��ʾ�� ����˵���������(������ ) A.����HNO3������������Ӧ�Ļ�� B.��ع���ʱ��������Һ��pH���� C. 1mol CH3CH2OH����ȫ����ʱ��3mol O2����ԭ D.������ӦΪCH3CH2OH+3H2O-12e-=2CO2+12H+ |
|||
�� |
B | |||
| ��� | 11 |
|
||||||||||||||||||||
���� |
2021������Ӧ���� | |||||||||||||||||||||
| ��� | ����ʵ������������ͽ��۶���ȷ����(������ )
|
|||||||||||||||||||||
�� |
A | |||||||||||||||||||||
| ��� | 12 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | �ڼ�����Һ�У�Cu2+�������������γ���ɫ�����ӣ���ṹ��ͼ��ʾ�� ����˵���������(������ ) A.����������ˮ�����γ������ԭ��ֻ��N��O B.����������ͭ���ӵ���λ����4 C.��̬Cuԭ�ӵļ۵����Ų�ʽ��3d104s1 D.���������зǽ���Ԫ�صĵ縺�Դ�С˳��ΪO��N��C��H |
|||
�� |
A | |||
| ��� | 13 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | ��֪NixMg1��xO������������ϵ�������߳�a����Li+���ӵ��þ����У��ɵõ�һ�ָ����ܵ�p��̫���ܵ�ز��ϣ���ṹ��Ԫ��ͼ��ʾ�� �ٶ����Ӻ�ľ��������������仯������˵����ȷ����(������ ) A.�ýṹ��Ԫ��Oԭ����Ϊ3���������� B.Ni��Mg�����̾�����  C.Ni����λ��Ϊ4������������ D.�����ʵĻ�ѧʽΪLi0.5Mg1.12Ni2.38O4 |
|||
�� |
B | |||
| ��� | 14 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | ˮ����������ΰ��ķ���֮һ����Ҫ�ɷ�Ϊ��������(3CaO∙SiO2)��������������ˮ��Ӧ���γ�������Ľṹ����Ӧʽ����2(3CaO∙SiO2)+6H2O=3CaO∙2SiO2∙3H2O+3Ca(OH)2 ∆H��0�����ǣ���Ҫ���⽻�����������ͼ�������ˮ�����ڽ����ṹ����ɿ�϶���ҹ���Ͽ��ӵĽ�������ȫ�����״����Ա���ˮ�Ľ��������Ч�������һ���⣬��֤�˴�ӽ�������������˵���������(������ ) A.ˮ���������ʯ��ʯ����ĥ�������Ƶ� B.ˮ�����������м���ʯ�࣬���Ե���ˮ���Ӳ������ C.ˮ���������ṩ�ᾧˮ���ȶ������ṹ D.�Ա���ˮ���ŵ��Ǽ����������ͼ�ˮ�����IJ��� |
|||
�� |
C | |||
| ��� | 15 |
|
|||||||||
���� |
2021������Ӧ���� | ||||||||||
| ��� | 25��ʱ�����±�����������Һ.
A.��Һ���У�c(A��)��c(Na+)��c(H+)��c(OH-) B. ��͢��pH���1.0��˵��  C.��Ϣ�͢�c(Na+)��c(H+)��c(OH-)��c(A��)��c(B��) D.��Ϣ�͢�c(HA) ��c(HB) |
||||||||||
�� |
B | ||||||||||
| ��� | 16 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | ��ˮFeCl3�dz��õķ�����ȡ����Ӧ��������������ˮ�⡢�����������ʡ�������������Ӧ�Ʊ���ˮFeCl3��ʵ��װ����ͼ��ʾ�� E��G�����ռ�����ش��������⣺ (1)ͨ��������A�й۲쵽������������C��P2O5��������_______�� (2)��E��G���ռ�������������FeCl3_______�����ʡ� (3)ʵ���������F�����ֶ���������B���ɹ۲쵽��������_______����ͨ��_______(�����)��ʹʵ���ܼ������С� (4)���з�Ӧ�����ӷ���ʽΪ_______�� (5)ijͬѧ��5.60 g���������Ƶ���ˮFeCl3��Ʒ13.00 g���ô�ʵ��IJ�����_______�� (6)ʵ�����л�����SOCl2��FeCl3��6H2O���干���Ʊ���ˮFeCl3���仯ѧ��Ӧ����ʽΪ_______.����ˮ�����Ȼ���ԭ�����Ƿ����FeCl2���Լ���_______�� |
|||
�� |
(1)��ȥ���� (2)������ (3)B�������ݲ������ʵ�����F�� (4)Cl2+2OH��=Cl��+ClO��+H2O (5)80.00% (6)FeCl3��6H2O+6SOCl2=FeCl3+12HCl+6SO2���������軯�� |
|||
| ��� | 17 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | ������ͪ�Ǵ���ҩ�������ȡ����Ч�ɷ֣�������F�Ǻϳ�������ͪ��һ���м��壬�ϳ�·����ͼ��ʾ��   ��֪��  �ش��������⣺ (1)F�к��������ŵ�������_______�� (2)A��B�ķ�Ӧ����Ϊ_______�� (3)C�ĺ˴Ź���������_______�����շ塣 (4)D�Ľṹ��ʽ��_______�� (5)E��F_______ͬ���칹��(��ǡ����ǡ�)�� (6)������  �Ǻϳɿ���ҩ�ǰ������һ���м��壬д�����Ҷ���ͱ�ͪ( �Ǻϳɿ���ҩ�ǰ������һ���м��壬д�����Ҷ���ͱ�ͪ( )Ϊԭ�Ϻϳɸû�����ķ�Ӧ����ʽ_______(���������л��Լ���ѡ)�� )Ϊԭ�Ϻϳɸû�����ķ�Ӧ����ʽ_______(���������л��Լ���ѡ)�� |
|||
�� |
(1)�Ѽ����ǻ������� (2)����(ȡ��)��Ӧ������ (3)6 (4)  ��������(5)�� ��������(5)��(6)CH3CH2OH��HOOCCOOH 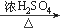 CH3CH2OOCCOOCH2CH3�� CH3CH2OOCCOOCH2CH3��   |
|||
| ��� | 18 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | �����ˮ������������Ҫ������������Ӧ�� ��CH4(g)+H2O(g)��CO(g)��3H2(g)����H=+206kJ/mol ��CO(g)��3H2O(g)��CO2(g) +H2(g)����H=��41kJ/mol �㶨ѹǿΪ100kPaʱ����n(CH4)��n(H2O)=1��3�Ļ������Ͷ�뷴Ӧ���У�ƽ��ʱ������ֵ����ʵ����������¶ȵĹ�ϵ��ͼ��ʾ��  �ش��������⣺ (1)д��CH4��CO2����H2��CO���Ȼ�ѧ����ʽ��_______�� (2)���ڼ����ˮ���������ⷴӦ������������ȷ����_______(����)�� A�����¡����������£�����������壬ѹǿ����Ӧ���ʼӿ� B�����¡����������£�����ˮ����������Ӱٷ�������Ӧ���ʼӿ� C�������¶ȣ�����Ӱٷ���������Ч��ײƵ������Ӧ���ʼӿ� D��������ʵĴ��������ͷ�Ӧ�¶�Ҳ��ʵ�ֵ�λʱ��ת���ʲ��� (3)ϵͳ��H2�ĺ�������700�����ҳ��ַ�ֵ���Դӻ�ѧƽ��ĽǶȽ��ͳ��ַ�ֵ��ԭ�� �ٵ���700�棬_______�� �ڸ���700�棬_______�� (4)��֪Ͷ�ϱ�Ϊn(CH4)��n(H2O)=1��3�Ļ�����壬p=100kPa��600��ʱ��CH4��ƽ��ת����Ϊ_______����Ӧ�ٵ�ƽ�ⳣ���ļ���ʽΪKp��_______(Kp���Է�ѹ��ʾ��ƽ�ⳣ������ѹ=��ѹ�����ʵ�������)�� |
|||
�� |
(1) CH4(g)+CO2(g)��2CO(g)��2H2(g)����H=247kJ/mol (2)C (3)����������Ӧ�������ȣ������¶ȵ����ߣ���Ӧ������Ӧ������еij̶Ƚϴ����������ʵ������������ŷ�Ӧ�Ľ��У�һ����̼�����ʵ�����������Ӧ�ڣ���Ӧ������Ӧ���ȣ����¶�����ʱ��ƽ�������ƶ���ʹ���������ʵ�����С (4)77.78%��3906.25 |
|||
| ��� | 19 |
|
||
���� |
2021������Ӧ���� | |||
| ��� | ij��ѧ��ȤС��ͨ���������ף�����˴�ij��������(�ɷ�ΪCu��Ag2Se��Au��Pt)�л��չ��ؽ����Ĺ��գ���������ͼ��ʾ�� �ش��������⣺ (1)д�������ա�ʱ������SeO2�Ļ�ѧ��Ӧ����ʽ_______�� (2)����Һ���еĽ�����������_______���������������ͨ��������Ŀ����_______��_______�� (3)�����ܡ�ʱPt��Au�ֱ�ת��Ϊ[PtCl6]2����[AuCl4]����д��Au�ܽ�����ӷ���ʽ_______�� (4)�ɴӡ��л��㡱���յĽ�����_______��ʵ���ҡ���ȡ��Һ���IJ���������_______��_______�� (5)���NH4[Au(SO3)2]��Һ����Au��������ӦʽΪ_______�� |
|||
�� |
(1)2Ag2Se+3O2=2SeO2+2Ag2O (2)Cu2+��Ag+���������ܴ��ڵ�Cu��SeO2����ֹ���������NO�ŷŵ���������Ⱦ���� (3)2Au+3Cl2+2Cl��=2[AuCl4]���� (4)Pt�����ձ�����Һ©�� (5)Au3++3e��=Au |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |