 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 2021年河北省普通髙中学业水平选择性考试模拟演练 | |
|---|---|
| 本卷共有试题:20 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 化学与生活密切相关。下列叙述不涉及氧化还原反应的是 A.牙膏中添加氟化物用于预防龋齿 B.绿化造林助力实现碳中和目标 C.氯化铁用于蚀刻金属眼镜架 D.可降解包装材料的完全降解有利于减少白色污染 |
|||
答案 |
A | |||
| 题号 | 2 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 聚丙烯是日用品及合成纤维的重要原料之一,其单体为丙烯,下列说法错误的是( ) A.丙烯可使Br2的CCl4溶液褪色 B.丙烯可与Cl2在光照条件下发生取代反应 C.聚丙烯的结构简式为  D.丙烯与乙烯互为同系物 |
|||
答案 |
C | |||
| 题号 | 3 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 下列说法正确的是 A.氕、氘和氚互称同素异形体 B.对于ΔH>0自发进行的化学反应,有ΔS>0 C.对于相同质量的水而言,其体积V的相对大小有:V(g)>V(l)>V(s) D.两原子形成化学键时要有电子得失或电子偏移 |
|||
答案 |
B | |||
| 题号 | 4 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 下列说法错误的是 A. CaO2的电子式为  B.Na不能从MgCl2溶液中置换出Mg C. [SiO4]四面体广泛存在于硅的含氧化合物中 D.利用FeCl3的水解反应可以制备Fe(OH)3胶体 |
|||
答案 |
A | |||
| 题号 | 5 |
|
||||||||||||||||||||
出处 |
2021河北适应考试 | |||||||||||||||||||||
| 题干 | 下列实验中,实验现象与结论不匹配的是
|
|||||||||||||||||||||
答案 |
C |
|||||||||||||||||||||
| 题号 | 6 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | NA是阿伏加德罗常数的值。下列叙述错误的是 A.1mol氮气分子中含有π键的数目为2NA B.1mol氩气分子中含有原子的数目为NA C.1mol氯化钠中含有Na+的数目为NA D.1mol白磷中含有P-P共价键的数目为4NA |
|||
答案 |
D | |||
| 题号 | 7 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 已知25℃、101kPa下,1 mol水蒸发为水蒸气需要吸热44.01 kJ 2H2O(l)=2H2(g)+O2(g) ΔH=+571.54 kJ·mol-1 C(s)+ 2H2O(g)=CO(g)+ H2(g) ΔH=+131.29 kJ·mol-1 则反应C(s)+  O2(g)=CO(g)的反应热为 O2(g)=CO(g)的反应热为A.ΔH=-396.36 kJ·mol-1 B. ΔH=-198.55 kJ·mol-1 C.ΔH=-154.54 kJ·mol-1 D. ΔH=-110.53kJ·mol-1 |
|||
答案 |
D | |||
| 题号 | 8 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 2-甲基-2-氯丙烷是重要的化工原料,实验室中可由叔丁醇与浓盐酸反应制备,路线如下: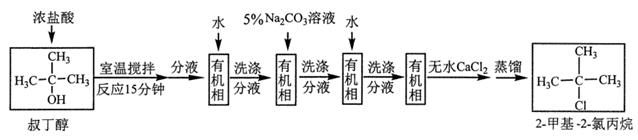 下列说法错误的是 A.由叔丁醇制备2-甲基-2-氯丙烷的反应类型为取代反应 B.用5%Na2CO3溶液洗涤分液时,有机相在分液漏斗的下层 C.无水CaCl2的作用是除去有机相中残存的少量水 D.蒸馏除去残余反应物叔丁醇时,产物先蒸馏出体系 |
|||
答案 |
B | |||
| 题号 | 9 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 醋酸为一元弱酸,25℃时,其电离常数Ka=1.75×10-5。下列说法错误的是 A. 0.1mol·L—1 CH3COOH溶液的pH在2-3范围内 B. CH3COONa溶液中,c(CH3COOH)+c(H+)=c(OH-) C.将0.1mol·L—1 CH3COOH溶液加水稀释,其电离常数和  均不变 均不变D.等体积的0.1mol·L—1 NaOH溶液和0.1mol·L—1 CH3COOH溶液混合后,溶液pH>7,且c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
|||
答案 |
C | |||
| 题号 | 10 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 氯化钯可以催化乙烯制备乙醛(Wacker法),反应过程如图: 下列叙述错误的是 A.CuCl被氧化的反应为2CuCl+2HCl+  O2=2CuCl2+H2O O2=2CuCl2+H2OB.催化剂PdCl2再生的反应为2CuCl2+Pd=PdCl2+2CuCl C.制备乙醛的总反应为CH2=CH2+  O2 O2  CH3CHO CH3CHOD.如果原料为丙烯,则主要产物是丙醛 |
|||
答案 |
D | |||
| 题号 | 11 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 短周期主族元素X、Y、Z、W原子序数依次增大,且原子序数Y+Z=X+W,X和W同主族,Z的族序数与周期数相等,四种元素中只有一种金属元素。下列说法正确的是 A.W有两种常见氧化物 B.原子半径Y<X<W<Z C.X的最高价氧化物的水化物是强酸 D.Y元素的氢化物分子间可以形成氢键 |
|||
答案 |
BD | |||
| 题号 | 12 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 葡酚酮是由葡萄籽提取的一种花青素类衍生物(结构简式如图),具有良好的抗氧化活性。下列关于葡酚酮叙述错误的是 A.可形成分子内氢键 B. 有6种含氧官能团 C.可使酸性高锰酸钾溶液褪色 D. 不与Na2CO3水溶液发生反应 |
|||
答案 |
BD | |||
| 题号 | 13 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 乙醚是常用的有机试剂,久置容易产生过氧化物,带来安全隐患。以下不可用来定性检出过氧化物的试剂是 A. K3[Fe(CN)6]溶液 B.弱酸性淀粉KI溶液 C. Na2Cr2O7和稀H2SO4溶液 D. (NH4)2Fe(SO4)2的稀H2SO4溶液和KSCN溶液 |
|||
答案 |
A | |||
| 题号 | 14 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | H3PO4的电离是分步进行的,常温下Ka1=7.6×10-3,Ka2=6.3×10-8,Ka3=4.4×10-13。下列说法正确的是( ) A.浓度均为0.1 mol/L的NaOH溶液和H3PO4溶液按照体积比2∶1混合,混合液的pH<7 B.Na2HPO4溶液中,c(H+)+c(H2PO4-)+2c(H3PO4)=c(PO43-) + c(OH-) C.向0.1 mol/L的H3PO4溶液中通入HCl气体(忽略溶液体积的变化),溶液pH=1时,溶液中大约有7.1%的H3PO4电离 D.在H3PO4溶液中加入NaOH溶液,随着NaOH的加入,溶液的pH增大,当溶液的pH=11时,c(PO43-)>c(HPO42-) |
|||
答案 |
B | |||
| 题号 | 15 |
|
||||||||||||||||||||||||
出处 |
2021河北适应考试 | |||||||||||||||||||||||||
| 题干 | 一定条件下,反应H2(g)+Br2(g) 2HBr(g)的速率方程为v=kcα(H)2·cβ(Br2) ·cγ(HBr),某温度下,该反应在不同浓度下的反应速率如下: 2HBr(g)的速率方程为v=kcα(H)2·cβ(Br2) ·cγ(HBr),某温度下,该反应在不同浓度下的反应速率如下:
A.表中c的值为4 B.α、β、γ的值分别为1、2、-1 C.反应体系的三种物质中,Br2(g)的浓度对反应速率影响最大 D.在反应体系中保持其他物质浓度不变,增大HBr(g)浓度,会使反应速率降低 |
|||||||||||||||||||||||||
答案 |
AB | |||||||||||||||||||||||||
| 题号 | 16 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 碘是人体必需的微量元素,也可用于工业、医药等领域。大量的碘富集于海藻灰〔主要成分是NaI)中,因此从海藻灰中提取碘,可有效利用海洋资源。 (1)某兴趣小组以海藻灰为原料进行I2的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了NaI溶液,将适量Na2SO3固体溶于NaI溶液,再将CuSO4饱和溶液滴入上述溶液中,生成白色CuI沉淀,该反应的离子方程式为______。 (2)待I-沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓HNO3,观察到______(颜色)气体放出,______(颜色)晶体析出。出于安全和环保考虑,该实验操作需在______(条件)下进行。该反应的化学方程式为______。 (3)用倾析法弃去上清液,固体物质用少量水洗涤后得到粗I2,进一步精制时,选择必需的仪器搭建装置,并按次序排列:______(夹持装置略)。 A.  B. B. C. C. D. D. E. E. F. F. (4)将精制得到的I2配成浓度为c mol·L—1的标准溶液,用来测定某样品中维生素C(相对分子质量为M的含量。具体操作如下:准确称量ag样品,溶于新煮沸过并冷却至室温的蒸馏水中,煮沸蒸馏水的目的是______。用250mL容量瓶定容,使用______(仪器)量取25.00 mL样品溶液于锥形瓶中,再加入10mL1∶1醋酸溶液和适量的______指示剂,立即用I2标准溶液滴定,溶液显稳定的______(颜色)即为滴定终点,消耗I2标准溶液V mL,则样品中维生素C的质量分数是______(写出表达式)。已知滴定反应方程式: 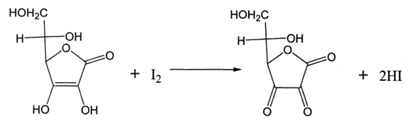 |
|||
答案 |
(1)2Cu2++SO32-+2I-+H2O=2CuI+SO42-+2H+ (2)红棕色;紫黑色;通风条件下;2CuI+8HNO3(浓)=2Cu(NO3)2+2NO2+4H2O (3)DCAF (4)除去蒸馏水中溶解的氧,防止干扰实验;滴定管;淀粉;蓝色; 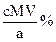 |
|||
| 题号 | 17 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 合理利用工厂烟灰,变废为宝,对保护环境具有重要意义。以某钢铁厂烟灰(主要成分为ZnO,并含少量的CuO、MnO2、Fe2O3等)为原料制备氧化锌的工艺流程如下: 回答下列问题: (1)“浸取”工序中加入过量氨水的目的:①使ZnO、CuO溶解,转化为[Zn(NH3)4]2+和[Cu(NH3)4]2+配离子;②______。 (2)ZnO转化反应的离子方程式为______。 (3)“除杂”工序中,反应的离子方程式为______。 (4)滤渣②的主要成分有______(填化学式),回收后可用作冶金原料。 (5)“蒸氨沉锌”工序中,“蒸氨”是将氨及其盐从固液混合物中蒸出,相应的化学方程式为______,蒸出物冷凝吸收后得到的碳化氨水可返回______工序循环使用。 (6)从碱式碳酸锌得到氧化锌的工序名称为______。 (7)将滤渣①用H2SO4溶液处理后得到______溶液和______固体(均填化学式)。 |
|||
答案 |
(1)使MnO2、Fe2O3沉淀除去 (2)ZnO+2NH3·H2O+2NH4+=[Zn(NH3)4]2++3H2O (3)Zn+[Cu(NH3)4]2+=Cu+[Zn(NH3)4]2+ (4)Zn、Cu (5)Zn(NH3)4(HCO3)2  4NH3↑+Zn(HCO3)2;浸出 4NH3↑+Zn(HCO3)2;浸出(6)煅烧 (7)Fe2(SO4)3;MnO2 |
|||
| 题号 | 18 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 我国科学家最近发明了一种Zn-PbO2电池,电解质为K2SO4、H2SO4和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下: 回答下列问题: (1)电池中,Zn为______极,B区域的电解质为______(填“K2SO4”、“H2SO4”或“KOH”)。 (2)电池反应的离子方程式为______。 (3)阳离子交换膜为图中的______膜(填“a”或“b”)。 (4)此电池中,消耗6.5 g Zn,理论上可产生的容量(电量)为______毫安时(mAh)(1 mol电子的电量为1 F,F=96500 C·mol-1,结果保留整数) (5)已知E为电池电动势(电池电动势即电池的理论电压,是两个电极电位之差,E=E(+)-E(-)),ΔG为电池反应的自由能变,则该电池与传统铅酸蓄电池相比较,EZn-PbO2______ EPb-PbO2;ΔG Zn-PbO2______ΔG Pb-PbO2(填“>”或“<”)。 (6)Zn是一种重要的金属材料,工业上一般先将ZnS氧化,再采用热还原或者电解法制备。利用H2还原ZnS也可得到Zn,其反应式如下:ZnS(s)+H2(g)  Zn(s)+H2S(g)。727℃时,上述反应的平衡常数Kp=2.24×10-6。此温度下,在盛有ZnS的刚性容器内通入压强为1.01×105Pa的H2,达平衡时H2S的分压为______Pa(结果保留两位小数)。 Zn(s)+H2S(g)。727℃时,上述反应的平衡常数Kp=2.24×10-6。此温度下,在盛有ZnS的刚性容器内通入压强为1.01×105Pa的H2,达平衡时H2S的分压为______Pa(结果保留两位小数)。 |
|||
答案 |
(1)负;K2SO4 (2)PbO2+SO42-+Zn+2H2O=PbSO4+Zn(OH)42- (3)a (4)5360 (5)>;< (6)0.23 |
|||
| 题号 | 19 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 科学工作者合成了含镁、镍、碳3种元素的超导材料,具有良好的应用前景。回答下列问题: (1)镍元素位于周期表第______列,基态镍原子d轨道中成对电子与单电子的数量比为______。 (2)在CO分子中,C与O之间形成______个σ键、______个π键,在这些化学键中,O原子共提供了______个电子。 (3)第二周期元素的第一电离能(I1)随原子序数(Z)的变化情况如图。I1随Z的递增而呈增大趋势的原因是______,原子核对外层电子的引力增大。导致I1在a点出现齿峰的原因是______。  (4)下列分子或离子与CO2具有相同类型化学键和立体构型的是______(填标号)。 A.SO2 B.OCN- C.HF2- D.NO2+ (5)过渡金属与O形成羰基配合物时,每个CO分子向中心原子提供2个电子,最终使中心原子的电子总数与同周期的稀有气体原子相同,称为有效原子序数规则。根据此规则推断,镍与CO形成的羰基配合物Ni(CO)x中,x=______。 (6)在某种含镁、镍、碳3种元素的超导材料晶体中,镁原子和镍原子一起以立方最密堆积方式形成有序结构。结构中的两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空隙中,晶胞如图所示。 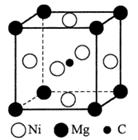 ①组成该晶体的化学式为______。 ②完全由镍原子构成的八面体空隙与由镍原子和镁原子共同构成的八面体空隙的数量比为______,由镍原子和镁原子共同构成的八面体空隙中镍原子和镁原子的数量比为______。 ③若取碳原子为晶胞顶点,则镍原子位于晶胞的______位置。 |
|||
答案 |
(1)10;3:1 (2)1;2;4 (3)随原子序数增大,核电荷数增大,原子半径逐渐减小;N元素原子的2p能级轨道半满,更稳定 (4)BD (5)4 (6)MgNi3C;1:3 ;2:1;棱心 |
|||
| 题号 | 20 |
|
||
出处 |
2021河北适应考试 | |||
| 题干 | 手性过渡金属配合物催化的不对称合成反应具有高效、高对映选择性的特点,是有机合成化学研究的前沿和热点。近年来,我国科学家在手性螺环配合物催化的不对称合成研究及应用方面取得了举世瞩目的成就。某螺环二酚类手性螺环配体(K)的合成路线如下: 已知如下信息:RCHO+CH3COR|   ,R,R′=烃基 ,R,R′=烃基回答下列问题: (1)化合物A是一种重要的化工产品,常用于医院等公共场所的消毒,可与FeCl3溶液发生显色反应,其结构简式为______;反应①的反应类型为______。 (2)化合物C可发生银镜反应,其名称为______,化合物C的结构简式为______。D的结构简式为______、G的结构简式为______、J的结构简式为______。 (3)C的一种同分异构体可与FeCl3溶液发生显色反应,其核磁共振氢谱有4组峰,峰面积比为3∶2∶2∶1,该异构体的结构简式为______。 (4)反应⑤的反应条件为______。 (5)在反应⑥的条件下,若以化合物E为原料,相应的反应产物为______和______,上述反应结果表明,中间体F中Br原子在E→H的合成过程中的作用为______。 |
|||
答案 |
(1)  ;取代反应 ;取代反应(2)间甲氧基苯甲醛; 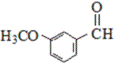 ; ; ; ;  (3)  ; ;(4)液溴、FeBr3 (5)  ; ; ;促进G→H成环反应的发生 ;促进G→H成环反应的发生 |
|||
| v福建省实践教学工作室 蔡实践 设计制作 v |