 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| �绯ѧ�ۺ� | |
|---|---|
| �����������⣺9 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2017�����ĵ����� | |||
| ��� | ��ͼװ���з�����Ӧ�����ӷ���ʽΪ��Zn+2H+ = Zn2++H2��������˵������ȷ���� ��A��a��b��������ͬ�ֲ��ϵĵ缫 ��B����װ�ÿ����ǵ��أ��������ҺΪϡ���� ��C����װ�ÿ�����ԭ��أ��������ҺΪϡ���� ��D����װ�ÿɿ�����ͭ-пԭ��أ��������ҺΪϡ����  |
|||
�� |
A | |||
| ��� | 2 |
|
||
���� |
2016���߿� | |||
| ��� | �����Ƿ�չ�е�����Դ���������ð�������Ʊ��������Ӧ���������ڡ��ش��������⣺ ��1����������ȣ�������Ϊȼ�ϵ��ŵ���_________�����ٴ�����㣩����������ֱ��ȼ�յ�����ת����Զ����ȼ�ϵ�أ�д����������ȼ�ϵ�صĸ�����Ӧʽ��____________�� ��2�������������Ʊ�H2O2����֪�� ��H2��g��+A��l������B��l������ ��H1 ��O2��g��+B��l������A��l��+H2O2��l���� ��H2 ����A��BΪ�л������Ӧ��Ϊ�Է���Ӧ����H2��g��+ O2��g����H2O2��l���Ħ�H____0���>������<����=������ ��3���ں��º��ݵ��ܱ������У�ij���ⷴӦ��MHx��s��+yH2��g����MHx+2y��s����H<0�ﵽ��ѧƽ�⡣�����й�������ȷ����________�� ��a.����������ѹǿ���ֲ��� ��b.����ymol H2ֻ��1 mol MHx ��c.�����£��÷�Ӧ��ƽ�ⳣ������ ��d.����������ͨ��������������v�����⣩>v�����⣩ ��4������̫����ֱ�ӷֽ�ˮ���⣬�����������������;����������ת����ʽΪ_______�� ��5�����������ĸ�����Ҳ����������Դ����ⷨ��ȡ�й㷺��;��Na2FeO4��ͬʱ���������Fe+2H2O+2OH−  FeO42−+3H2��������ԭ����ͼ1��ʾ��װ��ͨ������缫���������Ϻ�ɫ��FeO42−�����缫�����ݲ�����������������ҺŨ�ȹ��ߣ����缫����������ɫ���ʡ���֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ�� FeO42−+3H2��������ԭ����ͼ1��ʾ��װ��ͨ������缫���������Ϻ�ɫ��FeO42−�����缫�����ݲ�����������������ҺŨ�ȹ��ߣ����缫����������ɫ���ʡ���֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ�� ���ٵ��һ��ʱ���c��OH−�����͵�������_______��������ҡ��������ҡ����� ���ڵ������У��뽫�������������弰ʱ�ų�����ԭ����_______�� ����c��Na2FeO4�����ʼc��NaOH���ı仯��ͼ2����ѡM��N�����е�һ�㣬���� c��Na2FeO4���������ֵ��ԭ��_____________�� |
|||
�� |
(1)��ȾС������������Դ�㣻��Դ�ḻ��ȼ����ֵ�ߣ�H2+2OH��-2e��=2H2O (2)�� (3)ac (4)����ת��Ϊ��ѧ�� (5)�������� �ڷ�ֹNa2FeO4����H2��Ӧʹ���ʽ��� ��M�㣺c(OH��)�ͣ�Na2FeO4�ȶ��Բ�ҷ�Ӧ��(��N�㣺c(OH��)���ߣ����缫���������������ɣ�ʹNa2FeO4���ʽ���)�� |
|||
| ��� | 3 |
|
||
���� |
2015�����ۺ�1 | |||
| ��� | ijͬѧ��װ����ͼ��ʾ�ĵ绯ѧװ�ã��缫���Ϣ�~����Ϊʯī���պ�K������������ȷ���� ��A�����ӷ��缫������ ��B���缫��缫��Ӧ��O2+2H2O+4e-��4OH- ��C���缫������ԭ��Ӧ ��D���缫�������۲쵽����ɫ����  |
|||
�� |
B | |||
| ��� | 4 |
|
||
���� |
δ֪ | |||
| ��� | ��ͼ����������ʯī������ʢ�б���NaCl��Һ��U���У����з�����ȷ���� ��A��K1�պϣ���������Һ����ְ�ɫ���������ҳ������ձ�Ϊ���ɫ ��B��K1��  K2�պϣ�ʯī����Χ��ҺpH������ K2�պϣ�ʯī����Χ��ҺpH��������C��K2�պϣ������Ϸ����ķ�ӦΪ2Cl�D�D2e��=C12�� ��D��K2�պϣ���  ·��ͨ��0.002 NA������ʱ������������0.002mol���� ·��ͨ��0.002 NA������ʱ������������0.002mol���� |
|||
�� |
D | |||
| ��� | 5 |
|
||
���� |
2015������ĩ | |||
| ��� | ��������װ�õ�˵����ȷ���ǡ�����  ���������������١��������������������������������� ��A��װ�â��������ڵ�K+����CuSO4��Һ ��B��װ�âٽ�����ת��Ϊ��ѧ�� ��C����װ�â�����������ͭ����N��Ϊ���� ��D����װ�â����ڵ�⾫��ͭ����Һ�е�Cu2+Ũ�ȱ��ֲ��� |
|||
�� |
A | |||
| ��� | 6 |
|
||
���� |
2014�����ʼ� | |||
| ��� | ������ͼװ�ý���ʵ�飬�������ؾ�Ϊ1 mol��L-1��AgNO3��Һ��A��B��ΪAg�缫��ʵ�鿪ʼ�ȱպ�K1,�Ͽ�K2��һ��ʱ��Ͽ�K1���պ�K2���γ�Ũ���أ�������ָ��ƫת(Ag+Ũ��Խ��������Խǿ)������˵������ȷ���� ��A���պ�K1���Ͽ�K2��A�缫���� ��B���պ�K1���Ͽ�K2���ҳ���ҺŨ������ ��C���Ͽ�K1���պ�K2��NO3-��B�缫�ƶ� ��D���Ͽ�K1���պ�K2��A�缫����������Ӧ  |
|||
�� |
C | |||
| ��� | 7 |
|
||
���� |
2013���ݲ��� | |||
| ��� | ����ʵ������Ԥ����ȷ���� ��A.ʵ��I:������Aָ��ƫת��̼�����к�ɫ�������� ��Bʵ��II:������Aָ��ƫת������������ɫ������� ��C.ʵ��III:̼��������ɫ����������������л���ɫ������� ��D.ʵ��IV:��ͭ�ܽ⣬��ͭ���к�ɫ�������� |
|||
�� |
AD | |||
| ��� | 8 |
|
||
���� |
2012Ȫ�ݶ��� | |||
| ��� | ������ͼ�������ж�������ȷ���� ��A��ͨ��O2�ĵ缫�ĵ缫��ӦʽΪ�� O2 + 2H2O + 4e��= 4OH�� ��B����Ӧһ��ʱ��׳�����Һ��pH���� ��C���ҳ��е缫B�Ϸ�����ԭ��Ӧ ��D�����ҳ��е�ijһ�缫�������� 10.80gʱ�� �����ϼ׳������ĵ���������Ϊ840mL����״���£� 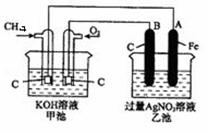 |
|||
�� |
C | |||
| ��� | 9 |
|
||
���� |
2005Ȫ��ģ�� | |||
| ��� | ijѧ����X��Y��װ�ã�����ͼ������ͭ�ĵ�⾫��ʵ�飨��ͭ����п���������������ʣ�������˵����ȷ���ǡ��� ��A��aӦ��c�����ӣ�bӦ��d������ ��B�����һ��ʱ�䣬b��d�����������ʵ����ʵ������ ��C�����һ��ʱ�䣬b��������Һ��pH���� ��D���������У�Yװ����Cu2+��Ũ��ʼ�ղ���  |
|||
�� |
B | |||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |