 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| �㶫ʡ������2017�����12��ģ�����ۻ�ѧ���� | |
|---|---|
| �����������⣺12 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
|||||||||||||||
���� |
2017����12��ģ�� | ||||||||||||||||
| ��� | ��ѧ�����������Ź㷺��Ӧ�ã����ж�Ӧ��ϵ�������
|
||||||||||||||||
�� |
A | ||||||||||||||||
| ��� | 2 |
|
||
���� |
2017����12��ģ�� | |||
| ��� | ����ʵ������ܴﵽʵ��Ŀ�ĵ��� ��A������ˮ���ռ�ͭ����Ũ���ᷴӦ������NO2 ��B���ð�ˮ����NaCl��MgCl2��AlCl3��NH4Cl������Һ ��C��������KMnO4��Һ��֤����Ļ�ԭ�� ��D���ñ���NaHCO3��Һ��ȥCl2�л��е�HCl |
|||
�� |
C | |||
| ��� | 3 |
|
||
���� |
2017����12��ģ�� | |||
| ��� | ��NAΪ�����ӵ�������ֵ�������й�������ȷ���� ��A����״���£� 22.4 LCH4���еĹ��ۼ���ΪNA ��B��1 mol Fe��1mol Cl2��ַ�Ӧ������ת����Ϊ3NA ��C�������£�pH =2�Ĵ�����Һ�к��е�H+��ĿΪ0.02NA ��D�����³�ѹ�£� 46g��NO2��N2O4������庬�е�ԭ����Ϊ3NA |
|||
�� |
D | |||
| ��� | 4 |
|
||
���� |
2017����12��ģ�� | |||
| ��� | �õ绯ѧ���Ʊ�LiOH��ʵ��װ����ͼ�����ö��Ե缫��a�ڵ���LiCl��Һ��b�ڵ���LiOH��Һ������������ȷ���� ��A��ͨ�����������ҺpH���� ��B���������ĵ缫��ӦʽΪ4OH���C4e����O2��+2H2O ��C������·��ͨ��1mol���ӵĵ���ʱ������0.25mol��Cl2���� ��D��ͨ���Li+ͨ������Ĥ��������Ǩ�ƣ�LiOHŨ��Һ��d�ڵ��� |
|||
�� |
D | |||
| ��� | 5 |
|
||
���� |
2017����12��ģ�� | |||
| ��� | ������װ��������ʵ�飬�������� ��  ��������������ͼ�١����������������� ����ͼ�ڡ���������������ͼ�ۡ���������������ͼ�� ��A��ͼ�٣���֤H2CO3����ǿ��H2SiO3 ��B��ͼ�ڣ��ռ�CO2��NH3 ��C��ͼ�ۣ�����Na2CO3��Һ��CH3COOC2H5 ��D��ͼ�ܣ�����CH3CH2OH��CH3COOC2H5 |
|||
�� |
B | |||
| ��� | 6 |
|
||
���� |
2017����12��ģ�� | |||
| ��� | ������Ԫ��W��X��Y��Z��ԭ��������������W�ĵ�����H2�ڰ����ܻ��ϲ�������ը��X��ͬ�����н�������ǿ��Ԫ�أ�Yԭ�ӵ��������������ڵ��Ӳ�����W��Zԭ�ӵ�������������ͬ������˵��������� ��A�����ʵķе㣺Z��W ��B�������Ӱ뾶��X��W ��C��Ԫ��X�������γɼȺ����Ӽ�Ҳ���Ǽ��Թ��ۼ��Ļ����� ��D��X��Y��Z������������Ӧ��ˮ���������Ӧ |
|||
�� |
B | |||
| ��� | 7 |
|
||
���� |
2017����12��ģ�� | |||
| ��� | 25��ʱ����0.1000 mol��L��1NaOH��Һ�ֱ�ζ�20.00ml 0.1000 mol��L��1������ʹ��ᣬ�ζ�������ͼ��ʾ������˵����ȷ���� ��A����ֱ��ʾ����ʹ���ĵζ����� ��B��pH=7ʱ���ζ�����ʹ�������NaOH��Һ�������� ��C��V(NaOH) =10.00mLʱ��������Һ�У�c(CH3COO��)��c(Na+)��c(H+)��c(OH��) ��D��V(NaOH) =20.00mLʱ������Һ��c(CH3COO��)��c(Cl��)  |
|||
�� |
C | |||
| ��� | 8 |
|
||||||||||||
���� |
2017����12��ģ�� | |||||||||||||
| ��� | Na2S2O3����Ҫ�Ļ���ԭ�ϣ�������ˮ�������Ի���Ի������ȶ��������Ի������ֽ�����S��SO2��ijС�����������ʵ��װ���Ʊ�Na2S2O3���гּ����������ԣ����ܷ�ӦΪ2Na2S+Na2CO3+4SO2 ��3Na2S2O3+CO2���ش��������⣺ ��1��װ��A���������Ʊ�________����Ӧ�Ļ�ѧ����ʽΪ________�� ��2������±�ʵ����̣�
|
|||||||||||||
�� |
��1��SO2���� H2SO4+Na2SO3 ��SO2��+H2O+Na2SO4 ��2����S2��+ H2O  ��HS��+ OH�������� ��HS��+ OH�������� ����Һ���ֵ���ɫ���ǣ�Ȼ�����壨����Ǽ��٣������� �ۼ�С���������� �ܹر�K1��K2����K3 ��SO2������ʹ��Һ������ӣ�ʹ����ֽ⣬���Ͳ��� ��3������������ᣬ���ˣ�����Һ�еμ�BaCl2��Һ���а�ɫ�������� |
|||||||||||||
| ��� | 9 |
|
||||||||||||||||||||||||
���� |
2017����12��ģ�� | |||||||||||||||||||||||||
| ��� | �о�CO��NOx��SO2�ȵĴ��������Ի�����������Ҫ���塣 ��1����ѧ�������о����ô�������β���е�NO��COת���CO2��N2���䷴ӦΪ�� 2NO(g)��2CO(g) 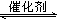 2CO2(g)��N2(g)����������H=��746.8kJ��mol-1 2CO2(g)��N2(g)����������H=��746.8kJ��mol-1��Ϊ���о���������Ը÷�Ӧ��Ӱ�죬�����±�����ʵ�飬��ò�ͬʱ��NO��Ũ��(c)��ʱ��仯��������ͼ1��ʾ��1��2��3������ʵ����������___________�� ����֪��ʹ�õ���������ʱ����������ȱ���������ѧ��Ӧ���ʡ���
 ������2��һ���¶��£���NO2��SO2�������1:2�����ܱ������з�����ӦNO2(g)+SO2(g)  SO3(g)+NO(g)���ﵽƽ��ʱSO3���������Ϊ25%���÷�Ӧ��ƽ�ⳣ��K=_______�� SO3(g)+NO(g)���ﵽƽ��ʱSO3���������Ϊ25%���÷�Ӧ��ƽ�ⳣ��K=_______����3������ԭ��ط�Ӧ��ʵ��NO2���������ܷ�ӦΪ6NO2+8NH3��7N2+12H2O���������ҺΪ���ԡ�����һ��ʱ��õ�ظ�����������ҺpH________����������С�����䡱���������缫��ӦʽΪ________�� |
|||||||||||||||||||||||||
�� |
��1���٢� ���¶ȡ����÷�ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�������ƶ�����(NO)���ͣ��÷�ӦΪ�����������С�ķ�Ӧ��ѹǿ����ƽ�������ƶ�����(NO)����4�֣����� ѹǿ������< ��2��1.8 ��3����С�� 2NO2+8e��+4H2O��N2+8OH�� |
|||||||||||||||||||||||||
| ��� | 10 |
|
||
���� |
2017����12��ģ�� | |||
| ��� | �����仯������;�㷺��ij��������Ҫ�ɷ���NiFe2O4������������NiO��FeO��CaO��SiO2�ȣ������ǴӸÿ����л���NiSO4�Ĺ���·�ߣ� ��֪��(NH4)2SO4�� 350�����ϻ�ֽ�����NH3��H2SO4��NiFe2O4�ڱ��չ���������NiSO4��Fe2(SO4)3������Sn��λ�ڵ������ڵڢ�A�塣 ��1������ǰ��������(NH4)2SO4�����ĥ�������ĥ��Ŀ����________�� ��2�������ݡ�������Fe2(SO4)3����FeO(OH)�����ӷ���ʽΪ________�����������ijɷֳ�Fe2O3��FeO(OH)�����________���ѧʽ���� ��3��Ϊ��֤��Ʒ���ȣ�Ҫ��⡰����Һ������������ȡһ������Ľ���Һ���������ữ����SnCl2��Fe3+��ԭΪFe2+������SnCl2�����ʵ���������Fe3+���ʵ�����________������ȥ������SnCl2����������K2Cr2O7����Һ�ζ���Һ�е�Fe2+����ԭ����ΪCr3+���ζ�ʱ��Ӧ�����ӷ���ʽΪ________��  ��4��������Һ����c(Ca2+) = 1.0��10��3mol��L��1���������ʴﵽ99%ʱ����Һ��c(F��) = ________ mol��L��1��[��֪Ksp(CaF2)=4.0��10��11] ��5���������У���ȡ������Һ������ȣ�V0/VA������Һ��Ni2+��Fe2+����ȡ��Ӱ����ͼ��ʾ��V0/VA�����ȡֵ��________�� |
|||
�� |
��1������Ӵ�������ӿ췴Ӧ���ʣ�ʹ��Ӧ����� ��2��Fe3++2H2O  FeO(OH)��+3H+����SiO2��CaSO4 FeO(OH)��+3H+����SiO2��CaSO4��3��0.5�� Cr2O72��+6Fe2++14H+��2Cr3++6Fe3++7H2O ��4��2.0��10��3 ��5��0.25 |
|||
| ��� | 11 |
|
||
���� |
2017����12��ģ�� | |||
| ��� | CuSO4��Cu(NO3)2����Ȼ������Ҫ��ͭ�Ρ��ش��������⣺ ��1��CuSO4��Cu(NO3)2�������ӻ�̬��������Ų�ʽΪ________��S��O��N����Ԫ�صĵ�һ�������ɴ�СΪ________�� ��2��SO42�������幹����________����SO42����Ϊ�ȵ������һ�ַ���Ϊ________���ѧʽ���� ��3����Cu(NO3)2��Һ��ͨ������NH3�����������[Cu(NH3)4](NO3)2������NO3������ԭ�ӵ��ӻ��������Ϊ________��[Cu(NH3)4](NO3)2�д��ڵĻ�ѧ�����ͳ��˼��Թ��ۼ��⣬����________�� ��4��CuSO4���۵�Ϊ 560�棬Cu(NO3)2���۵�Ϊ 115�棬CuSO4�۵���ߵ�ԭ����________�� ��5������CuSO4��NaOH�Ʊ���Cu(OH)2����ȩ��ʱ�����ɺ�ɫ��Cu2O���侧���ṹ��ͼ��ʾ��  �����ٸþ���ԭ���������AΪ��0��0��0����BΪ��1��0��0����CΪ��  �� �� �� �� ������Dԭ�ӵ��������Ϊ________��������________ԭ�ӡ� ������Dԭ�ӵ��������Ϊ________��������________ԭ�ӡ���������Cu2O�����ܶ�Ϊd g��cm��3����������Ϊapm�����ӵ�����ֵNA=________�� |
|||
�� |
��1��[Ar]3d9�������� N>O>S ��2���������塡���� CCl4����SiF4�ȣ� ��3��sp2������������λ�������Ӽ� ��4��CuSO4��Cu(NO3)2��Ϊ���Ӿ��壬SO42-������ɱ�NO3-��CuSO4�����ܽϴ��۵�ϸߡ� ��5����(  �� �� �� �� )������ Cu�������������� )������ Cu�������������� |
|||
| ��� | 12 |
|
||
���� |
2017����12��ģ�� | |||
| ��� | ������M��һ�����ϣ�A��D�dz������л�����ԭ�ϣ�������·�ߺϳɻ�����M�� ��֪������Ϣ�� ��A����Է�������Ϊ28  �ش��������⣺ ��1��A��������________��D�Ľṹ��ʽ��________�� ��2��A����B�ķ�Ӧ����Ϊ________��C�й���������Ϊ________�� ��3��E����F�ĵĻ�ѧ����ʽΪ________�� ��4�����й���G��˵����ȷ����________�������ţ� ����a�����ڷ����� ����b������FeCl3��Һ��Ӧ����ɫ ����c���������Ƶ�Cu(OH)2�������ɺ�ɫ���� ����d��G�����������14��ԭ�ӹ�ƽ�� ��5��������M��ͬϵ��N��M����Է���������14��N��ͬ���칹����ͬʱ�������������Ĺ���________�֣������������칹���� �������뻯����M������ͬ�Ĺ����ţ��ڱ�����������ȡ���� ��6�����������ϳ�·�ߣ�������X��Y�����ʵ���֮��2:1��Ӧ�ɵõ�������  |
|||
�� |
��1����ϩ�� ��2���ӳɷ�Ӧ����ȩ�� ��3��  ��4��cd�� ��5��18��3�֣� ��6��CH3CH2CHO����������  |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |