 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| �ϰ�һ��2011��2012ѧ��ȸ�һ��ѧ����ĩ�� | |
|---|---|
| �����������⣺22 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
δ֪ | |||
| ��� | ���и������ʣ���ѧ��������ͬ����������Ҳ��ͬ���� ��A��SO2��SiO2������������ B��Na2O2��Na2O ����������C��CO2��H2S ������ D��CCl4��KCl |
|||
�� |
C | |||
| ��� | 2 |
|
||
���� |
δ֪ | |||
| ��� | ��ȷ���ջ�ѧ������ѧ�û�ѧ�Ļ��������л�ѧ��������ȷ���� ��A����ϩ�Ľṹ��ʽΪCH2CH2�������������������� ������B���ǻ��ĵ���ʽ��  ���� ���� ��C��Ca2+�Ľṹʾ��ͼΪ  ���������� D���Ҵ��ķ���ʽ��CH3CH2OH�� ���������� D���Ҵ��ķ���ʽ��CH3CH2OH�� |
|||
�� |
C | |||
| ��� | 3 |
|
||
���� |
2009���ջῼ | |||
| ��� | ��ͼΪ���ѵ�أ�����˵����ȷ���� ��A��һ��ʱ���пƬ�������С ��B��ͭ�缫�����������ɫ ��C��������ͭͨ����������п ��D��п�缫�Ǹõ�ص�����  |
|||
�� |
A | |||
| ��� | 4 |
|
||
���� |
2007�����߿� | |||
| ��� | X��YΪ������Ԫ�أ�Xλ��IA�壬X��Y���γɻ�����X2Y������˵����ȷ���� ��A��X��ԭ�Ӱ뾶һ������Y��ԭ�Ӱ뾶 ��B��X��Y�ļ����Ӳ����ܾ�����ͬ�ĵ��Ӳ�ṹ ��C����Ԫ���γɵĻ������У�ԭ�Ӹ����Ȳ�����Ϊ1�U1 ��D��X2Y���������ӻ����Ҳ�����ǹ��ۻ����� |
|||
�� |
D | |||
| ��� | 5 |
|
||
���� |
δ֪ | |||
| ��� | ������ˮ���ܼ����һ�������� ��A���������顢���Ȼ�̼������������B�����������Ҵ������Ȼ�̼ ��C�������Ҵ������Ȼ�̼������������ D�����������Ҵ������� |
|||
�� |
C | |||
| ��� | 6 |
|
||
���� |
δ֪ | |||
| ��� | ����100mL 1mol/L������п���ķ�Ӧ����ȡ���д�ʩ��ʹ��Ӧ���ʼӿ���� �������¶ȣ����ڸ���100mL 3mol/L������۸���300mL 1mol/L��� ���õ���п�۴���п������������ѹǿ ��A���٢ۢܢݡ�����������B���٢ڢܡ��������� C���٢ڢۢܡ������� D���٢ڢܢ� |
|||
�� |
B | |||
| ��� | 8 |
|
||
���� |
δ֪ | |||
| ��� |  �� �� ��������������������ȷ���� ��������������������ȷ������A��һ�����������ӡ����ӡ�������ɵ� ��B����ѧ���ʼ�����ȫ��ͬ ��C���˵�����ͺ��������һ����� ��D��������һ����ͬ����������������һ������ͬ |
|||
�� |
D | |||
| ��� | 9 |
|
||
���� |
δ֪ | |||
| ��� | Ϊ�о�������ʴ�����������ʣ�ij����С��ѧ���ý���˿��������С��ͬ�������ֱ�̶���ͼʾ������װ���У��ٷ����ڲ��������ﱣ����ͬ��һ��ʱ�䣬���ж�ʵ�����ʱ�������������ȷ���� ��A��װ�â�����Һ��һ�����½����� B�����Һ��װ�â��װ�â�ĵ� ��C��װ�â��е�������ʴ������ D��װ�â��е���������û����ʴ  |
|||
�� |
B | |||
| ��� | 10 |
|
||
���� |
δ֪ | |||
| ��� | ��Ϊ�������ڡ���VA��Ԫ�أ���������Ԫ�����ڱ��е�λ���Ʋ⣬�鲻���ܾ��е������� ��A������ͨ��״�����ǹ��塡������������������������ B�������ǣ�5����3����3�ȶ��ֻ��ϼ� ��C��AS2O5��Ӧˮ��������Ա�H3PO4ǿ�� D����Ļ�ԭ�Ա���ǿ |
|||
�� |
C | |||
| ��� | 11 |
|
||
���� |
δ֪ | |||
| ��� | һ���¶��£���3 mol SO2��1 mol O2 ����һ�����ܱ������У��ڴ��������½������з�Ӧ: 2SO2��g��+ O2��g�� ��2SO3��g������H=��197 kJ/ mol�����ﵽƽ��״̬ʱ������˵������ȷ���� ��2SO3��g������H=��197 kJ/ mol�����ﵽƽ��״̬ʱ������˵������ȷ������A������SO3Ϊ2 mol����������������B��SO2��SO3 ���ʵ���֮��һ��Ϊ3 mol ��C���ų�197 kJ�������������������� D��SO2�����ʵ�����SO3 ���ʵ���һ����� |
|||
�� |
B | |||
| ��� | 13 |
|
||
���� |
δ֪ | |||
| ��� | Ԫ��R�����·�Ӧ��RO��5R����6H��===3R2��3H2O������˵����ȷ���� ��A��Ԫ��Rλ�����ڱ��еڢ�A�� ��B��RO�е�Rֻ�ܱ���ԭ ��C��ÿ��Ӧ����1 mol RO��ת�Ƶ��ӵ����ʵ���Ϊ5 mol ��D��R2�ڳ��³�ѹ��һ�������� |
|||
�� |
C | |||
| ��� | 14 |
|
||
���� |
δ֪ | |||
| ��� | ��ƻ��֭������Һ����ɫ����ƻ���ܻ�ԭ������Һ����˵�� ��A����ƻ����ֻ�����۲������ࡡ������������ B����ƻ����ֻ����������� ��C��ƻ������ʱ����ˮ��Ϊ�����ǡ����������� D��ƻ������ʱ���Ǿۺϳɵ��� |
|||
�� |
C | |||
| ��� | 15 |
|
||
���� |
δ֪ | |||
| ��� | �������¸�˵���� ����ˮ���⡢��ԭ�Ӽ���Ի�ѧ�����ϡ� �ڽ����ͷǽ��������γ����Ӽ��� �����Ӽ��������ӡ������ӵ�������� �ܸ��ݵ��뷽��ʽHCl��H����Cl�����ж�HCl������������Ӽ��� ��H2���Ӻ�Cl2���ӵķ�Ӧ������H2��Cl2�����ﹲ�ۼ�������������H��Clԭ�ӣ�����H��Clԭ���γ����Ӽ��Ĺ��̡� ��������˵����ȷ���� ��A.�٢ڢ���ȷ�������������������������������������������� B��������ȷ ��C.����ȷ����������ȷ ����������������������������������������D�����ٲ���ȷ |
|||
�� |
B | |||
| ��� | 16 |
|
||
���� |
2010�����ʼ� | |||
| ��� | ��ͼ��һЩ�����л����ת����ϵ�����ڷ�Ӧ�١��ߵ�˵������ȷ���� ��A����Ӧ���Ǽӳɷ�Ӧ���������������������������������� ��B��ֻ�з�Ӧ���ǼӾ۷�Ӧ ��C��ֻ�з�Ӧ����ȡ����Ӧ�������������������������� ��D����Ӧ�ܢݢ���ȡ����Ӧ  |
|||
�� |
C | |||
| ��� | 18 |
|
||
���� |
δ֪ | |||
| ��� | ��һ���¶��£�������ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯��������ͼ�����б�������ȷ���� ��A����Ӧ�Ļ�ѧ����ʽΪ.2M  N N ��B��T2ʱ�����淴Ӧ������ȣ��ﵽƽ�� ��C��T3ʱ������Ӧ���ʴ����淴Ӧ���� ��D��T1ʱ��N��Ũ����MŨ�ȵ�2��  |
|||
�� |
D | |||
| ��� | 19 |
|
||
���� |
δ֪ | |||
| ��� | ��1����6 mol A�����5 mol B�����Ϸ��� 4L�ܱ������У���һ�������·�����Ӧ�� 3A(g)+B(g) 2C(g)+xD(g)����5min�ﵽƽ�⣬��ʱ����2 mol C�����D��ƽ����Ӧ����Ϊ0.15 mol/(L��min)����ƽ��ʱA�����ʵ���Ũ����____________��B��ת������__________��x��ֵ��___________�� 2C(g)+xD(g)����5min�ﵽƽ�⣬��ʱ����2 mol C�����D��ƽ����Ӧ����Ϊ0.15 mol/(L��min)����ƽ��ʱA�����ʵ���Ũ����____________��B��ת������__________��x��ֵ��___________����2����Ӧ2H2��g��+ O2��g����2H2O��g�� �������仯��ͼ��ʾ����֪��1molH2��1molO2��1molH-O�еĻ�ѧ���ֱ���Ҫ����436KJ��496KJ��463KJ��������÷�Ӧ�������������� ��������ա��ų����� ���������� ��KJ������  ��3����������������ɴ���ʹ����һ������װ�ã��乹���� ��ͼ��ʾ��a��b�����缫���ɶ��̼����ɡ�д��a���ĵ缫��Ӧʽ���������������������������� ��  ��4����ҵ���õ�ⱥ��ʳ��ˮ�ķ�����ȡ������������Ӧ�� ������ת����ʽ���������������������������� ���������������� ���ϲ�������Ӧ����Һ��pH���������� ���������С������ |
|||
�� |
��1��0.75mol/L �� 20%���� 3 ��2���ų����� 484 ��3��H2 +2OH����2e����2H2O ��4������ת��Ϊ��ѧ�ܡ��������������� |
|||
| ��� | 20 |
|
||
���� |
δ֪ | |||
| ��� | ��ϩ����ʯ�͵���Ҫ����ԭ�ϣ��������һ������ʯ�ͻ���ˮƽ�ı�־����ش� ��1��(3��)��ϩͨ��������Ȼ�̼��Һ�У��۲쵽���������������������������䷴Ӧ����ʽΪ��������������������������������ϩ��һ�������·����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ�������������������������� ��2�����⣬��ϩ�������������������飬����������Ҫ�����֣� ����һ����  ���ն��� 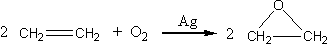 �� �� ������ɫ��ѧ��ԭ�����������������ԭ�Ӿ����Ժõķ�Ӧ����ˣ���ʵ�������У�Ӧ���ù������������������� �������������á� |
|||
�� |
��1����Һ��ɫ����   ��2���� |
|||
| ��� | 21 |
|
||
���� |
δ֪ | |||
| ��� | ij�о���ѧϰС�������һ��ʵ����̽��Ԫ�������ɡ���ͬѧ����Ԫ�طǽ��������Ӧ��ۺ�����֮��Ĺ�ϵ���������ͼװ����һ�������N��C��Si�ķǽ�����ǿ���Ƚϵ�ʵ���о�����ͬѧ�����û���Ӧ�Ĺ��ɣ�������ͼװ�������OԪ�صķǽ����Ա�Sǿ��ʵ���о��� �ش��������⣺ ��1��ͼ��Dװ�������������������������������������������� �� ��2��N��C��Si�ķǽ�������ǿ������˳���ǣ����������������������������������� �� ����������������ѡ����ͬѧ��Ƶ�ʵ�����õ����ʣ� �Լ�AΪ_________���Լ�CΪ_________������ţ��� ��ϡHNO3��Һ��ϡ�����̼��Ƣ�Na2SiO3��Һ��SiO2 ��3����ͬѧ��Ƶ�ʵ�����õ��Լ�AΪ________���Լ�BΪ________���Լ�CΪ________�� |
|||
�� |
��1������©�� ��2��N��C��Si���������١������������� ��3��˫��ˮ�����������������̡������������������������Һ�� |
|||
| ��� | 22 |
|
||||||||||||||
���� |
δ֪ | |||||||||||||||
| ��� | ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������100mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ������ѻ���ɱ�״̬����
��2����2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ���ʣ�����Һ������䣩������������������ �� ��3�������Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ������������������������зֱ����������������Һ�� ��A������ˮ���������������� B��NaCl��Һ������������ C��Na2CO3��Һ���������� D��CuSO4��Һ ����Ϊ���е��ǣ����ţ������������������������������� |
|||||||||||||||
�� |
��1��2��3��������Ϊ�Ƿ��ȷ�Ӧ���¶����ߣ���Ӧ���ʼӿ� ��2��0.1mol/(L��min) ��3��A B |
|||||||||||||||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |