 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| ������2010-2011ѧ�꣨�£���һ������� | |
|---|---|
| �����������⣺26 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | 2011��3��11���ձ�����9.0����������Х����ʹ���ֺ˵�վ�˵���鱬ը�ų����з����ԡ� 13153I,�Ӷ�����������˺�����Ԫ��ԭ�ӵ��������� ��A.53������ B .78������ C.131���� D.25 |
|||
�� |
B | |||
| ��� | 2 |
|
||
���� |
2008Ȫ�ݲ��� | |||
| ��� | ʳƷ�����DZ�֤ʳƷ��ȫ����Ҫ��ʩ�����в�����ʳƷ��ȫ���ָ����� ��A�����۵ĺ����������� �� B�������谷�ĺ������������� C���������εĺ��������� D����ȩ�ĺ��� |
|||
�� |
A | |||
| ��� | 3 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | Ԫ�صĻ�ѧ������Ҫ������ ��A.��������������������� B.���������������������� C.������������������������ D.���������� |
|||
�� |
D | |||
| ��� | 4 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ��ȷ���ջ�ѧ������ѧ�û�ѧ�Ļ��������л�ѧ������ȷ���� ��A.��ϩ�Ľṹ��ʽΪCH2CH2���������������������������� B. ���ķ���ʽΪC6H6 ��C. Cl���Ľṹʾ��ͼΪ��  ������������D.NaCl�ĵ���ʽ�� ������������D.NaCl�ĵ���ʽ�� |
|||
�� |
B | |||
| ��� | 5 |
|
||
���� |
2011ɽ���߿� | |||
| ��� | Ԫ�ص�ԭ�ӽṹ���������ʺ����ڱ��е�λ�á�����˵����ȷ���� ��A.Ԫ��ԭ�ӵ���������������Ԫ�ص�����ϼ� ��B.�����ԭ���У�����˽Ͻ����������˶��ĵ��ӵ������ϸ� ��C.P��S��Cl�õ�������������������Ӧˮ��������Ծ�������ǿ ��D.Ԫ�����ڱ���λ�ڽ����ͷǽ����ֽ��߸�����Ԫ�����ڹ���Ԫ�� |
|||
�� |
C | |||
| ��� | 6 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ����˵��������� ��A.������ˮ����Եõ������� ��B.���м�������ʯ�࣬��ʹ��������Ϊ���� ��C.���������Ƶ�������ͭ������Һ�е������� ��D.  �� �� ��Ϊͬ���칹�� ��Ϊͬ���칹�� |
|||
�� |
D | |||
| ��� | 7 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ���й���������;�������У�����ȷ���� ��A.ʯӢ�����������������ѧ�������� ������B.���������������������ά ��C.ʯī��������Ե���ϡ�����������D.��������������ѹ������о���� |
|||
�� |
C | |||
| ��� | 8 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ���������У������ӳɷ�Ӧ���������� ��A.��ϩʹ���Ը��������ɫ������������ ������������B.����������ˮ�У���ˮ��ӽ���ɫ ��C.��ϩʹ������Ȼ�̼��Һ��ɫ���� ������������D.�������ˮ��ϣ�����һ��ʱ����ɫɫ��ʧ |
|||
�� |
C | |||
| ��� | 9 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | �����������ʱ仯�ıȽϣ���ȷ���� ��A.ԭ�Ӱ뾶��С��Al>Mg>Na������������������ B.����ǿ��:KOH>NaOH>LiOH ��C.��̬�⻯���ȶ���:HBr>HCl>HF�������������� D.��ԭ��ǿ��:F-->Cl-->Br-->I-- |
|||
�� |
B | |||
| ��� | 10 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ����ɫ��ѧ������Ҫ����֮һ��ָ�Ӽ�������������ƿ��еĻ�ѧ��Ӧ��ʹԭ�ӳ�����ã���������Ⱦ�����ͭΪԭ����ȡ����ͭ������ͭ�������������Ϊ���ϡ���ɫ��ѧ��˼��ķ�Ӧ·�ߣ��û�ѧ����ʽ��ʾ���ǣ� ��A.��CuSO4��Cu + 2H2SO4(Ũ)  CuSO4 + SO2��+ 2H2O CuSO4 + SO2��+ 2H2O��B.��CuSO4��2Cu + O2  2CuO����CuO+H2SO4��ϡ��==CuSO4+H2O 2CuO����CuO+H2SO4��ϡ��==CuSO4+H2O ��C.��Cu(NO3)2��Cu+4HNO3(Ũ)==Cu(NO3)2+2NO2��+2H2O ��D.��Cu(NO3)2��3Cu + 8HNO3(ϡ) == 3Cu(NO3)2 + 2NO��+ 4H2O |
|||
�� |
B | |||
| ��� | 11 |
|
||
���� |
2011ɽ���߿� | |||
| ��� | Al��Fe��Cu������Ҫ�Ľ���Ԫ�ء�����˵����ȷ���� ��A.���߶�Ӧ���������Ϊ���������� ��B.���ߵĵ��ʷ����ڿ����о�ֻ���������� ��C.�Ʊ�AlCl3��FeCl3��CuCl2�����ܲ��ý���Һֱ�����ɵķ��� ��D.���AlCl3��FeCl3��CuCl2�Ļ����Һʱ��������������Al��Fe��Cu |
|||
�� |
C | |||
| ��� | 12 |
|
||
���� |
2005�㶫�߿� | |||
| ��� | ���з�Ӧ���ӷ���ʽ��ȷ���� ��A�����Ȼ�����Һ�м����������������Һ��Al3+ + 4OH���� AlO2�� + 2H2O ��B��������Һ��ͨ�������̼��CO2 + H2O + 2C6H5O���� 2C6H5OH + CO32�� ��C����С�մ���Һ�м��������Һ��HCO3�� + H+��CO2��+ H2O ��D�����廯������Һ��ͨ�����������Fe2+ + 2Br �� + 2Cl2��Fe3+ +Br2 + 4Cl �� |
|||
�� |
A | |||
| ��� | 13 |
|
|||||||||||||||
���� |
2011�����߿� | ||||||||||||||||
| ��� | �±���ѡ���У����������û���Ӧͨ��Y�õ�W��һ�黯������
|
||||||||||||||||
�� |
D | ||||||||||||||||
| ��� | 14 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ���ڻ�ѧ����ʽSiO2+ 3C=SiC+2CO��,����˵����ȷ���� ��A.��Ӧ��SiO2����������C�ǻ�ԭ�� ��B.��Ԫ�ر���ԭ��̼Ԫ�ر����� ��C.�ڷ�Ӧ��ֻ̼����ԭ�� ��D.�ڷ�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ1:2 |
|||
�� |
D | |||
| ��� | 15 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | д�������йط�Ӧ�Ļ�ѧ����ʽ ��1�������������ڹ�������������һ�ȼ�����Ȼ������� �� ��2����������������������Һ��Ӧ�������� ��3����ϩʹ������Ȼ�̼��Һ��ɫ�� �� |
|||
�� |
��1��CH4��Cl2 ��CH3Cl��HCl ��CH3Cl��HCl��2��SiO2��2NaOH��Na2SiO3��H2O ��3��CH2��CH2 ��Br2����  ����CH2BrCH2Br ����CH2BrCH2Br |
|||
| ��� | 16 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ��1�������и����е����У���H2O��H2O2��D2O����H��D��T���� 12C�� 13C���ܽ��ʯ��ʯī���������顢�춡�飬����ͬλ�ص��������������� ������ͬ��������������������������� ������ͬ���칹����������������������� ��������ţ� ��2��������A��һ�������¿���ˮ�����ӳɷ�Ӧ�õ���ѧʽΪC2H4O�Ļ�����B,�û���������������ʣ� ��B + Na  ���������������� Na���ڵײ��������������� ���������������� Na���ڵײ�����������������B + CH3COOH 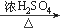 ����ζ�IJ��� ����ζ�IJ�����д��A�Ľṹʽ������������ �� ��B���������Ϊ75%��ˮ��Һ���������������������� �� ������B��Na��Ӧ�Ļ�ѧ����ʽΪ������������������ �� |
|||
�� |
��1���� �ۣ��ܡ��� ���� ��2����.  ��ҽ���õ������� �� 2C2H5OH + 2Na�� 2C2H5ONa + H2������ �� |
|||
| ��� | 17 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ��ʵ�������ǿ�������ͼ��ʾ��װ����ȡ�����������ش��������⣺ ��1�������йظ�ʵ��������У���ȷ���������������������� ������ţ� ����a�Թ����ȼ���Ũ���ᣬȻ���ҡ���Թܱ����������Ҵ����ټ����� �ڱ���̼������Һ���Գ�ȥ���������в��������� ������������һ����ɫ��������ζ����״Һ�� ����a�Թ��м��뼸�����Ƭ�������Ƿ�ֹ����ʱҺ�屩�� ��2��Ũ������˴����������⣬��һ�����ǣ������������������������������������� �� ��3��װ���������ĵ���Ҫ���ڱ���̼������Һ��Һ���ϣ����ܲ�����Һ�У� ��ͬѧ��������ͼװ�������վͿɲ�����Һ�У�������Ƿ������������ ����ǡ�����  ��4����Ҫ���Ƶõ������������������Ӧ���õ�ʵ������������������������������� �� ��5��a�Թ��з�����Ӧ�Ļ�ѧ����ʽ���������������������������������������������������������� �������� |
|||
�� |
��1���ڢۢ� ��2����ˮ��������������3�� �ǡ���������4����Һ�� ��5��CH3COOH + C2H5OH�� 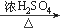 CH3COO C2H5 + H2O CH3COO C2H5 + H2O |
|||
| ��� | 18 |
|
|||||||||||||||||||||||||||
���� |
2011���Ÿ�һ�ʼ� | ||||||||||||||||||||||||||||
| ��� | �±���Ԫ�����ڱ���һ���֣��ش������й����⣺
��2��������ԭ�ӵĽṹʾ��ͼ���������������� �� �ۺ͢�Ԫ���γɵĻ������к��������� ������д��ѧ�����ͣ� ��3���ڢ�---���Ԫ���У���������ǿ��Ԫ������������ ���ǽ�������ǿ��Ԫ�������� ������õ�Ԫ������������ ��(����Ԫ�ط��ű�ʾ) ��4���������������Ӧ��ˮ���ﻯѧʽ�������������� �� ��5��Ԫ�آ���Ԫ�آ���ȣ��ǽ����Խ�ǿ���������� ����Ԫ�ط��ű�ʾ������һ��ѧ��Ӧ����ʽ������һ��ʵ�������������������� �� |
||||||||||||||||||||||||||||
�� |
��1��N����Si ��2��  �������Ӽ��� �������Ӽ��� ��3��Na����F����Ar �� ��4��HClO4 ��5��Cl ����Na 2S ��Cl2 ��2NaCl ��S�� |
||||||||||||||||||||||||||||
| ��� | 19 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ȼ�շ��Dzⶨ�л����������ʽ��һ����Ҫ��������ش��������⣺ ��1������������ȫȼ��ʱ�����ɵĶ�����̼��ˮ�����ʵ���֮��Ϊ1:2������������ ������ţ� ��CH4������ ��C2H6�� ������������C3H6 ����������C6H6 ��2��0.1molij��B��ȫȼ�պ����ɵ�CO2�������Ϊ 4.48L��STP�������ɵ�ˮΪ 5.4g����ͨ�����㣨д��������̣��Ƶ���B�ķ���ʽ�� |
|||
�� |
��1�� �١� ��2��n(C)=n(CO2) = 4.48L/ 22.4L•mol-1= 0.2mol������������ n(H)=2n(H2O) =2��( 5.4g/ 18g•mol-1)= 0.6mol������ n������: n(C): n(H) =0.1:0.2:0.6 = 1:2:6���������� ������ ��B�ķ���ʽΪ��C2H6 |
|||
| ��� | 20 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ����װ�û�����ܴﵽʵ��Ŀ�ĵ��� �������� �������� ���������� ���������� ���������������� ���������������� �ٴӵ�ˮ�з���ⵥ�ʡ�����ͭ��ϡ������ȡ����NO����֤��������������뷴Ӧ���ܼ���װ�������� ��A.�٢ڡ��� ��B.�ۢܡ�����C.�ڢۢܡ��� D.�٢ڢۢ� |
|||
�� |
B������������������ | |||
| ��� | 21 |
|
||
���� |
2006�������� | |||
| ��� | ��֪������KMnO4����μ�Ũ���ᣬ��������ɫ���壻����FeCl2��Һ��ͨ������ʵ��ٲ��������壬��Һ���ɫ����ȡʵ������ɵ���Һ���ڵ���KI��ֽ�ϣ���ֽ����ɫ�������ж���ȷ���� ��A������ʵ��֤�������ԣ�MnO4����Cl2��Fe3����I2 ��B������ʵ���У���������������ԭ��Ӧ ��C��ʵ������ɵ����岻��ʹʪ��ĵ���KI��ֽ���� ��D��ʵ���֤��Fe2���������������л�ԭ�� |
|||
�� |
A | |||
| ��� | 22 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | 1���ij��̬��ֻ����1������������ӳɷ�Ӧ�������ȴ��顣1mol���ȴ������6mol����������ȫ��ȡ����Ӧ��������Ľṹ��ʽΪ ��A .CH2=CH2��������B .CH3CH=CH 2 ����C.CH3CH3��������D. CH3CH2CH=CH2 |
|||
�� |
B�������������������� | |||
| ��� | 23 |
|
||
���� |
2012���ϸ߿� | |||
| ��� | NAΪ�����ӵ���������ֵ������˵������ȷ���� ��A�����ܱ������м���l.5mol H2��0.5molN2����ַ�Ӧ��ɵõ�NH3������ΪNA ��B��һ�������£� 2.3g��Na��ȫ��O2��Ӧ���� 3.6g����ʱʧȥ�ĵ�����Ϊ0.1NA ��C�� 1.0L��0.1 mol��L-1Na2S��Һ�к��е�S2-������Ϊ0.1NA ��D����״���£�22.4L��CCl4�к��е�CCl4������ΪNA |
|||
�� |
B |
|||
| ��� | 24 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ��0.2molij�л����0.5mol������һ�ܱ�������ȼ�յò���ΪCO2��CO��H2O(��������������ͨ��Ũ����ʱ��Ũ��������������� 10.8g;��ͨ�����ȵ�����ͭʱ������ͭ������������ 3.2g;��ͨ����ʯ��ʱ����ʯ�ҵ����������� 17.6g�����л���Ļ�ѧʽ�� ��A. C2H4 ������������B. C2H4O����������C. C2H6O2����������D. C3H6O3 |
|||
�� |
B | |||
| ��� | 25 |
|
||
���� |
2011���߿� | |||
| ��� | ͼ��X��Y��ZΪ���ʣ�����Ϊ���������֮���������ת����ϵ�����ֲ�������ȥ�������У�A�׳ƴ�����������E�Dz�����ˮ�������������������ᷴӦ�� �ش��������⣺ ����ɵ���Y��Ԫ�������ڱ��е�λ������������ ��M�д��ڵĻ�ѧ������Ϊ������ ��R�Ļ�ѧʽ���������������� �� ��һ�������£�Z��H2��Ӧת��ΪZH4��ZH4�ĵ���ʽΪ�������������������������� �� ����֪A��1mol Al��Ӧת��ΪXʱ���������ʾ�Ϊ���壩���ų�akJ������д���÷�Ӧ���Ȼ�ѧ����ʽ�������������������������������������������� �� ��д��A��D��ϡ��Һ��Ӧ����G�����ӷ���ʽ�������������������������������� �� ����4mol D��ϡ��Һ�У�����X��ĩ���������������ɵ�����ֻ��һ�֣���������ϵ�л���n(X2+)��n(X)�仯��ʾ��ͼ�������n(X2+)�����ֵ�� 
|
|||
�� |
�ŵڶ����ڵ�VIA�� ���Ӽ������ۼ� H2SiO3(��H4SiO4) ��  �� �� ��8Al(s)+3Fe3O4(s)=9Fe(s)+4Al2O3(s)����H=- 8a kJ/mol ��3Fe3O4+28H��+NO3����9Fe3��+NO��+14H2O����  |
|||
| ��� | 26 |
|
||
���� |
2011���Ÿ�һ�ʼ� | |||
| ��� | ij��ѧ��ȤС���ͬѧ������ͼ��ʾʵ��װ�ý���ʵ�飨ͼ��a��b��c��d��ʾֹˮ�У����� ��  �� ����1��B��һ�ֿ����濪���ƣ������ͣ���Ʊ������װ�á�����װ��B�������Է��� ���������� ���� ��2����������������������д��ţ��������װ�ÿ�������ȡ���ռ�������д��ʵ������ȡ�����Ļ�ѧ����ʽ�������������������������� �� ��3��B��D��Eװ����������B��ʢװŨ�����ͭƬ�������п����ϰ��ϣ������Ƶ�NO2�������й�ʵ�顣 �� ������Dװ����֤NO2��ˮ�ķ�Ӧ�����������Ϊ���ȹر�ֹˮ������������������������������ �����ٴ�ֹˮ������������������������������ ����ʹ�ձ��е�ˮ�����Թܶ��IJ����� �������������������������������� �� ���Թܶ��е�NO2��ˮ��ַ�Ӧ�������Թ��ڻ���ͨ��һ������O2��ֱ���Թ�ȫ��������Һ����NO2��ͨ��O2�����ʵ�����Ϊ �������������������������������� |
|||
�� |
��1��(1)�ȹ�d����������©����ˮ��©����Һ������Թ���Һ�棬һ��ʱ��߶Ȳ�䣬˵���������Ǻõġ� ��2��A��C��E������ MnO2 + 4HCl��Ũ��  ��MnCl2 + Cl2��+ 2H2O�� ��MnCl2 + Cl2��+ 2H2O�� ��3����ab ��c ˫�ֽ��գ����ȣ��Թܶ�ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ� ��4��1 |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |