 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 福州市2011—2012学年度第二学期期末高一质量检查化学试卷 | |
|---|---|
| 本卷共有试题:24 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
||
出处 |
2003上海高考 | |||
| 题干 | 上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于 A 无机物 B 有机物 C 盐类 D 非金属单质 |
|||
答案 |
B | |||
| 题号 | 2 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是 A.氨气分子的比例模型  B.Cl-的结构示意图为 B.Cl-的结构示意图为 C.乙烯的结构简式为C2H4 D.质量数为37的氯原子为1737Cl |
|||
答案 |
B | |||
| 题号 | 3 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 下列关于化学键的叙述正确的是 A.离子化合物可能含共价键 B.共价化合物可能含离子键 C.离子化合物中只含离子键 D.离子化合物中一定含有金属离子 |
|||
答案 |
A | |||
| 题号 | 4 |
|
||
出处 |
未知 | |||
| 题干 | A、B、C均为短周期元素,它们在周期表中的位置如下图.已知B、C两元素在周期表中族序数之和是A元素序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C 所在的一组是 A.Be、Na、Al B.B、Mg、Si C.O、P、Cl D.C、Al、P  |
|||
答案 |
C | |||
| 题号 | 5 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 关于苯 的下列叙述正确的是 的下列叙述正确的是A.它既有单键又有双键 B能发生取代反应 C.它有双键,容易发生加成反应D.乙烯和苯都能使溴水因反应而褪色 |
|||
答案 |
B | |||
| 题号 | 6 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 据报道,意大利科学家合成了一种新型氧分子,它是由四个氧原子构成的。下列关于该分子的叙述正确的是 A.O2、O3、O4互为同位素 B.O2、O3、O4互为同素异形体 C.O4的摩尔质量为64 D.O2、O3、O4互称为同分异构体 |
|||
答案 |
B | |||
| 题号 | 7 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 下列装置中导线上无电流通过的是 A B C D |
|||
答案 |
D | |||
| 题号 | 8 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 将甲、乙两种金属的性质相比较,下列不能说明甲的金属性比乙强的是 A.甲与水反应比乙与水反应剧烈 B.甲单质能从乙的盐溶液中置换出单质乙 C.与某非金属反应时甲原子失电子数目比乙的多 D.甲的最高价氧化物的水化物比乙的最高价氧化物的水化物碱性强 |
|||
答案 |
C | |||
| 题号 | 9 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 下列措施不符合节能减排的是 A.大力发展火力发电,解决广东电力紧张问题 B.在屋顶安装太阳能热水器为居民提供生活用热水 C.尽量少开私家车,多骑自行车。 D.用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气 |
|||
答案 |
A | |||
| 题号 | 10 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 下列反应属于吸热反应的是 A.木炭的燃烧 B.氢氧化钡晶体与氯化铵晶体混合 C.镁条与稀硫酸的反应D.生石灰溶于水 |
|||
答案 |
B | |||
| 题号 | 11 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 下列物质性质比较正确的是 A.热稳定性:HCl>H2S>H2O B.离子半径:Na+>Cl一>F— C.碱性:NaOH>Mg(OH)2>Al(OH)3 D.熔点:金刚石>干冰>食盐 |
|||
答案 |
C | |||
| 题号 | 12 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 下列过程需要克服分子之间作用力的是 A.HCl气体溶于水 B.液氯汽化 C.氯化镁受热熔化 D.二氧化硅受热熔化 |
|||
答案 |
B | |||
| 题号 | 13 |
|
||||||||||||||||||||||||||||||
出处 |
2012福州高一质检 | |||||||||||||||||||||||||||||||
| 题干 | 下列各组反应(表中物质均为反应物),反应刚开始时,放出H2的速率最大的是
|
|||||||||||||||||||||||||||||||
答案 |
D | |||||||||||||||||||||||||||||||
| 题号 | 14 |
|
||
出处 |
未知 | |||
| 题干 | 在一定的温度下逆反应A(g)+3 B(g) 2 C(g)达到平衡的标志是 2 C(g)达到平衡的标志是A、 C生成的速率与C分解的速率相等 B、单位时间内生成3n mol A,同时生成3n mol B C、 A、B、C的浓度不再变化 D、A、B、C的分子数比为1:3:2 |
|||
答案 |
AC | |||
| 题号 | 15 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | X、Y、Z三种金属,X、Y组成原电池,X是负极;把Y浸入Z的硝酸盐溶液中,Y表面有Z析出。则X、Y、Z活动性顺序为 A.X>Y>Z B.Z>Y>X C.X>Z>Y D.Y>X>Z |
|||
答案 |
A | |||
| 题号 | 16 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在 5L密闭容器中进行,30秒后,NO的物质的量增加了0.3 mol,则此反应的平均速率v(x)(表示反应物的消耗速率或生成物的生成速率)为 A.v (O2)= 0.0l mol·L-1·s-1 B.v (NO)=0.002 mol·L-1·min-1 C.v (H2O)=0.003 mol·L-1·s-1 Dv (NH3)=0.001 mol·L-1·s-1 |
|||
答案 |
C | |||
| 题号 | 17 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 下列物质中,不能使酸性KMnO4溶液褪色的物质是 ①  ②乙烯 ③CH3COOH ④乙炔 ⑤SO2 ⑥苯 ②乙烯 ③CH3COOH ④乙炔 ⑤SO2 ⑥苯A.①⑥ B.①②③⑥ C.①④ D.①③⑥ |
|||
答案 |
D | |||
| 题号 | 18 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,由此可以得出该有机物 A.分子中C、H、O的个数比1:2:3 B.分子中C和H的个数比为l:2 C.分子中肯定不含氧原子 D.分子中肯定含有氧原子 |
|||
答案 |
B | |||
| 题号 | 19 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 乙醇分子结构式如图所示,下列反应及断键部位不正确的是 A.乙醇与钠的反应是①键断裂 B.乙醇的催化氧化反应是②③键断裂 C.乙醇的催化氧化反应是①③键断裂 D.乙醇与乙酸发生酯化反应是①键断裂  |
|||
答案 |
B | |||
| 题号 | 20 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 下列叙述中,不正确的是 A.糖类和蛋白质都是人体重要的营养物质 B.蛋白质溶液遇硫酸铜后产生的沉淀不能重新溶于水 C.液化石油气和天然气的主要成分都是甲烷 D.利用油脂在碱性条件下的水解,可以制得肥皂和甘油 |
|||
答案 |
C | |||
| 题号 | 21 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 下表为元素周期表的一部分,参照元素①一⑧在表中的位置回答下列问题: (1)④、⑤、⑥的原子半径由大到小的顺序为 。(用元素符号表示) (2)②、③、⑧的最高价氧化物对应水化物的酸性由强到弱的顺序是 。(用化学式表示) (3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的电子式: 。 (4)由①、②、④组成的多种常见有机物中,有两种作为家庭厨房中常用调味品的主要成份,且相互可以反应生成一种具有果香味的液体,该液体也常用作香料原料。写出该反应的化学方程式: 。该反应属于 反应。 (5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:(其中Z为白色沉淀)  写出X溶液与Y溶液反应的离子方程式为 。 |
|||
答案 |
(1)Na>Al>0 (2)HclO4>HNO3>H 2C03 (3)Na+[:O:H]-或 (4)CH3COOH+CH3CH2OH 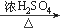 CH3COOCH2CH3 +H2O CH3COOCH2CH3 +H2O 酯化反应(或取代反应) (5)A13+ +3NH3·H20=A1(OH) 3↓+3NH4+ |
|||
| 题号 | 22 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 汽车已经成为重要的交通工具,其主要以石油的加工产品汽油为燃料,但其排放的尾气是空气的主要污染物之一。已知汽车尾气中的主要污染物有:SO2、NOx、CO和C等。请回答下列有关问题: (1)假设汽油的主要成分是丁烷(C4H10),当Imol气态丁烷完全燃烧并生成CO2和液态水时,放出的热量为2900kJ,试写出丁烷燃烧的热化学方程式: ,汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由 能转化为 ,最终转化为机械能。 (2)目前汽车尾气多采用催化转化的方法加以治理,此方法能将汽车尾气中的有毒气体转化为参与大气循环的气体,请写出在催化剂作用下NO2与CO反应的化学方程式 。 |
|||
答案 |
(1)2C4H10(g) +13O2(g)= 8C02(g)+1OH20(1)△H=-5800kJ·mol-1 (2)2NO2+ 4C0  N2+ 4C02
N2+ 4C02 |
|||
| 题号 | 23 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 图-I是电解CuCl2溶液的装置,其中c、d为石墨电极。 (1)正极为 (填“a”或“b”)阳极为 。(填“c”或“d”) (2)阳极电极反应式为 检验该阳极产物的方法是 。 (3)电解一段时间后发现阴极增重6. 4g,则外电路中通过的电子的物质的量是 摩尔,若该电解反应所需的电子全部由氢氧燃料电池提供,则至少需要消耗 L氢气(标准状况下)才能满足需要。 
|
|||
答案 |
(1)a c (2)2Cl-一2e一=C12 ↑ 湿润的淀粉碘化钾试纸 (3)0.2 2.24 |
|||
| 题号 | 24 |
|
||
出处 |
2012福州高一质检 | |||
| 题干 | 在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图-2所示的实验装置以确认上述混合气体中是否含有SO2和C2H4。请回答下列问题: (1)I、II、Ill、IV装置可盛放的试剂是:(请将下列有关试剂的序号填入对应装置内,可重复选用)。A.品红溶液 B.NaOH溶液 C.浓硫酸 D.溴水  I ; Ⅱ ; Ⅲ ; IV ; (2)能说明SO2气体存在的现象是 ; (3)使用装置Ⅱ的目的是 ; (4)确定含有乙烯的现象是 ; (5)写出装置Ⅳ发生的化学反应 ;反应类型 ; (6)为了制备重要的有机原料——氯乙烷(CH3—CH2Cl),下面是两位同学设计的方案。 甲同学:选乙烷和适量氯气在光照条件下制备,原理是: CH3—CH3+Cl2  CH3—CH2Cl+HCl CH3—CH2Cl+HCl乙同学:选乙烯和适量氯化氢在一定条件下制备,原理是: CH2=CH2+HCl →CH3—CH2Cl 你认为上述两位同学的方案中,合理的是 ,简述你的理由: 。 |
|||
答案 |
(1)A B A D (2)I中品红溶液褪色 (3)除二氧化硫 (4)Ⅲ中品红溶液不褪色,IV中溴水褪色 (5)CH2=CH2+Br—Br→CH2Br—CH2Br 加成反应 (5)乙同学的方案; 由于烷烃的取代反应是分步进行的,反应很难停留在某一步,所以得到的产物往往是混合物;而用乙烯与HCl反应只有一种加成产物,所以可以得到相对纯净的产物。 |
|||
| v福建省实践教学工作室 蔡实践 设计制作 v |