 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 2012年全国各校试题精选(13) | |
|---|---|
| 本卷共有试题:7 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
||
出处 |
未知 | |||
| 题干 | 下列说法正确的是 A. (NH4)2SO4溶液能使蛋白质变性 B.分子式为C2H4O2的有机物不一定是羧酸 C.煤的干馏是物理变化,煤的气化和液化是化学变化 D.纤维素、蛋白质、油脂、葡萄糖在一定条件下都能发生水解反应 |
|||
答案 |
B | |||
| 题号 | 2 |
|
||
出处 |
未知 | |||
| 题干 | 根据下图海水综合利用的工业流程图,判断下列说法正确的是 已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。 A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 C.在过程④、⑥反应中每氧化0.2 mol Br- 需消耗0.1mol Cl2 D.过程⑤在生产中无需解决其对金属设备的腐蚀问题 |
|||
答案 |
C | |||
| 题号 | 3 |
|
||
出处 |
未知 | |||
| 题干 | 在容积为2L的容器内发生反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0,起始时充入1mol CO和0.8mol H2O,经过2min后,反应达到平衡状态,此时CO2的浓度为0.2mol·L-1,下列说法正确的是 CO2(g)+H2(g) △H<0,起始时充入1mol CO和0.8mol H2O,经过2min后,反应达到平衡状态,此时CO2的浓度为0.2mol·L-1,下列说法正确的是A.该反应的平衡常数为:K=2/15 B.CO和H2O的转化率相同 C.2min内,用H2表示的反应速率为:v(H2)=0.lmol/(L·min) D.升高温度时,V正减小,v逆增大 |
|||
答案 |
C | |||
| 题号 | 4 |
|
||
出处 |
2012莆田质检 | |||
| 题干 | 酸性溶液中,Fe2+会被空气缓慢氧化为Fe3+。不同条件下,一定浓度的Fe2+的氧化率随时间变化关系如右图所示。 下列有关说法正确的是 A.该氧化过程的离子方程式为:Fe2++O2+4H+=Fe3++2H2O B.pH=1.5时Fe2+的氧化率一定比pH=2.5的大 C.Fe2+的氧化率仅与溶液的pH和温度有关 D.其他条件相同时,80℃时Fe2+的氧化率比50℃的大  |
|||
答案 |
D | |||
| 题号 | 5 |
|
||
出处 |
未知 | |||
| 题干 | 过氧化钙(CaO2)常用作种子消毒剂、药物制造、油脂漂白及高温氧化剂,还可以作为鱼池增氧剂。将SO2通入过氧化钙固体粉末中有气体生成。有人提出:CO2、SO2与过氧化钙的反应原理相同;但也有人提出:SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。 实验一、通过气体体积的测量判断发生的化学反应,实验装置如下:  (1)试剂A可以选用____________,试剂B的作用是____________________________。 (2)装置E用于测定氧气的体积,请在框中画出装置图。 (3)实验测得装置C增重m1 g,装置D增重m2 g,装置E中收集到V L气体(已换算成标准状况下),用上述有关测量数据判断,当SO2未氧化、部分氧化、完全氧化时,V与m的关系式。 未氧化____________________,部分氧化______________________,完全氧化____________________________。 若SO2完全氧化,写出反应的化学方程式:______________________________。 实验二、向一定量的过氧化钠固体中通入足量SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。 提出假设: 假设1:反应后固体中只有__________,SO2未氧化; 假设2:反应后固体中只有__________,SO2完全氧化; 假设3:_____________________________。 实验探究: (4)设计实验证明假设3是正确的,简要回答实验过程、现象和结论:________________________________________________________________________ ________________________________________________________________________ ________________________________________________________________________。 实验评价: (5)实验过程中SO2的通入量直接影响探究实验结果的科学性,请简要说明原因:________________________________________________________________________ ________________________________________________________________________。 |
|||
答案 |
(1)浓硫酸 吸收未反应的SO2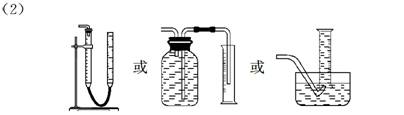 (3)V=7m1/30 V<7m1/30 V=0 CaO2+SO2===CaSO4 Na2SO3 Na2SO4 反应后固体为Na2SO3、Na2SO4的混合物,SO2部分氧化 (4)取少量反应后的固体放入试管中,加适量水溶解,加入BaCl2溶液有白色沉淀产生。再加入稀盐酸,沉淀部分溶解,证明原固体中既有亚硫酸钠也有硫酸钠,即Na2O2将SO2部分氧化 (5)若Na2O2剩余,固体加水溶解,过氧化钠能将SO氧化成SO |
|||
| 题号 | 6 |
|
||
出处 |
未知 | |||
| 题干 | 碳酸钠与工农业生产、日常生活紧密相关。工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题: 方案一:沉淀分析法 (1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀______________(填操作)、洗涤、烘干、称量,洗涤沉淀的操作是__________________________________。 方案二:气体分析法 (2)把一定量的样品与足量盐酸反应后,用下图所示装置测定产生CO2的体积,为了确保测定结果的准确性,B中的溶液最好采用______________________,但选用该溶液后实验结果仍然不够准确,其原因是____________________________________________________________________________。  方案三:质量差分析法 (3)把一定质量的样品和足量的稀硫酸反应,采用下图所示装置,通过称量反应前后盛有碱石灰的干燥管的质量,利用其质量差求算样品的纯度。  该实验的操作步骤有:①在干燥管内填满碱石灰,质量为m g;②取n g样品装入广口瓶中;③检验装置的气密性;④缓慢鼓入空气数分钟,再称量干燥管质量为w g;⑤关闭止水夹;⑥打开止水夹;⑦缓慢加入稀硫酸至不再产生气体为止;⑧缓慢鼓入空气数分钟。 Ⅰ.正确的操作顺序是(填序号): ③―→__________―→⑥―→________―→⑤―→________―→⑦―→________―→④。 Ⅱ.若去掉装置A,测定结果________;若去掉装置B,测定结果________(填“偏大”、“偏小”或“无影响”)。 |
|||
答案 |
(1)过滤 沿玻璃棒缓慢地向过滤器中加蒸馏水至浸没沉淀物,使水自然流下,重复2~3次 (2)饱和NaHCO3溶液 CO2中混有的HCl与NaHCO3溶液反应生成CO2 (3)Ⅰ.② ⑧ ① ⑥ Ⅱ.偏大 偏大 |
|||
| 题号 | 7 |
|
||
出处 |
未知 | |||
| 题干 | 铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某铝镁合金(设不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。 [探究一] 实验方案:铝镁合金  测定剩余固体质量 测定剩余固体质量问题讨论: (1)称取一定质量的铝镁合金粉末样品,加入过量的NaOH溶液,充分反应。实验中发生反应的化学方程式是___________________________。 (2)过滤、洗涤、干燥、称量剩余固体。若未洗涤固体,测得镁的质量分数将_____(填“偏高”或“偏低”)。 [探究二] 实验方案:铝镁合金  测定生成气体的体积 测定生成气体的体积实验装置:  问题讨论: (1)某同学提出该实验装置不够完善,应在A、B之间添加一个装有碱石灰的干燥装置。你的意见是:_________ (填“需要”或“不需要”)。 (2)为准确测定生成气体的体积,实验中应注意的问题是(只要求写出其中一点): [探究三] 实验方案:称量x g铝镁合金粉末,放在如右图所示装置的惰性电热板上,通电使其充分灼烧。  问题讨论: (1)欲计算Mg的质量分数,该实验中还需测定的数据是_____________。 (2)若用空气代替O2进行实验,对测定结果是否有影响? ________(填“是”或“否”)。 |
|||
答案 |
[探究一] (1)2A1+2NaOH+2H2O=2NaA1O2+3H2↑ (或2A1+2NaOH+6H2O=2Na[A1(OH)4]+3H2↑) (2)偏高 [探究二] (1)不需要 (2)检查装置的气密性(或合金完全溶解,或加入足量盐酸,或调整 量气管C的高度,使C中液面与B液面相平等合理答案) [探究三] (1)灼烧后固体的质量 (2)是 |
|||
| v福建省实践教学工作室 蔡实践 设计制作 v |