| A | B | C | D |
 人面鱼纹陶盆 人面鱼纹陶盆 |  “马踏飞燕”铜奔马 |  宇航员的航天服 |  光导纤维 |
| 无机非金属材料 | 金属材料 | 有机高分子材料 | 复合材料 |
2.家用暖气片大多用低碳钢材料制成,一旦生锈不仅影响美观,也会造成安全隐患。下列防止生锈的方法中,存在安全隐患的是
A.在暖气片表面镀锡 B. 在暖气片表面涂漆
C.在暖气片表面涂铝粉 D. 非供暖期在暖气内充满弱碱性的无氧水
3.常温下,将2种一元酸HX和HY分别和NaOH溶液等体积混合,实验数据如下:
| 组别 | 混合前 | 混合后 | |
| 甲 | c(HX)=0.1 mol·L-1 | c(NaOH) = 0.1mol·L-1 | pH = 9 |
| 乙 | c(HY)=0.1 mol·L-1 | c(NaOH) = 0.1mol·L-1 | pH = 7 |
A.HY为强酸 B.HX溶液的pH=1
C.甲的混合液中c(X-) = c(Na+) D.乙的混合液中c(Na+) > c(Y-)
4.NaCl是我们生活中必不可少的物质。将NaCl溶于水配成1 mol·L-1的溶液,溶解过程如图所示,下列说法正确的是
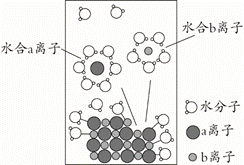
A.a离子为Na+
B.溶液中含有NA个Na+
C.水合b离子的图示不科学
D.室温下测定该NaCl溶液的pH小于7,是由于Cl-水解导致
5.114号元素为Fl(中文名“
 ”),它是主族元素,其原子核外最外层电子数是4。下列说法不正确的是
”),它是主族元素,其原子核外最外层电子数是4。下列说法不正确的是A.Fl的原子核外有114个电子 B.Fl是第七周期第IVA族元素
C.Fl在同主族元素中金属性最强 D.Fl的原子半径小于同主族其他元素
6.锌锰碱性干电池是依据原电池原理制成的化学电源。电池中负极与电解质溶液接触直接反应会降低电池的能量转化效率,称为自放电现象。
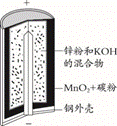

下列关于原电池和干电池的说法不正确的是
A.两者正极材料不同
B.MnO2的放电产物可能是KMnO4
C.两者负极反应式均为Zn失电子
D.原电池中Zn与稀H2SO4存在自放电现象
7.取1 mL 0.1 mol·L-1 AgNO3溶液进行如下实验(实验中所用试剂浓度均为0.1 mol·L-1):
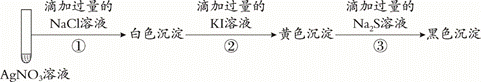
下列说法不正确的是
A.实验①白色沉淀是难溶的AgCl B.由实验②说明AgI比AgCl更难溶
C.若按①③顺序实验,看不到黑色沉淀 D. 若按②①顺序实验,看不到白色沉淀
8.下列事实与所对应的离子方程式正确的是
A.室温下,测定醋酸钠溶液的pH > 7:CH3COONa === CH3COO-+Na+
B.实验室用氯化铝溶液和氨水制备氢氧化铝:Al3+ +3OH- ===Al(OH)3↓
C.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:Na2S2O3 + 2H+ === SO2 ↑ + S↓+ 2Na+ + H2O
D.用碳酸钠溶液处理锅炉水垢中的硫酸钙:CaSO4(s) + CO32-(aq) === CaCO3(s) + SO42-(aq)
9.为探究电解的放电规律,进行如下实验:
| 序号 | 阳极材料 | 阴极材料 | 电解质 | 阳极产物 | 阴极产物 |
| ① | 石墨 | 石墨 | 0.1 mol·L-1 CuCl2溶液 | Cl2 | Cu |
| ② | 石墨 | 石墨 | 0.1 mol·L-1 NaCl溶液 | Cl2 | H2 |
| ③ | 石墨 | 石墨 | 0.2 mol·L-1 CuSO4溶液 | O2 | Cu |
| ④ | 铜 | 石墨 | 0.2 mol·L-1 CuSO4溶液 | Cu2+ | Cu |
| ⑤ | 石墨 | 石墨 | 熔融NaCl | Cl2 | Na |
A.对比①②可知,阴极放电顺序是:Cu2+ > H+ > Na+
B.对比①③可知,阳极放电顺序是:Cl- > OH- > SO42-
C.对比③④可知,阳极是铜时,会先于溶液中的离子放电
D.对比①⑤可知,电解得到金属只能用熔融态,不能用水溶液
10.以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:
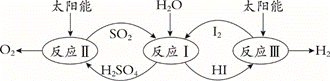
相关反应的热化学方程式为:
反应I:SO2(g) + I2(g) + 2H2O(l) === 2HI(aq) + H2SO4(aq) ΔH1 =﹣213 kJ·mol-1
反应II:H2SO4(aq) === SO2(g) + H2O(l) +
 O2(g) ΔH2 = +327 kJ·mol-1
O2(g) ΔH2 = +327 kJ·mol-1反应III:2HI(aq) === H2(g) + I2(g) ΔH3 = +172 kJ·mol-1
下列说法不正确的是:
A.该过程实现了太阳能到化学能的转化
B.SO2和I2对总反应起到了催化剂的作用
C.总反应的热化学方程式为:2H2O(l) === 2H2 (g)+O2(g) ΔH = +286 kJ·mol-1
D.该过程降低了水分解制氢反应的活化能,但总反应的ΔH不变
11.科学家很早就提出锂-空气电池的概念,它直接使用金属锂作电极,从空气中获得O2,和以LiFePO4作电极的锂离子电池相比,增大了电池的能量密度(指标之一是单位质量电池所储存的能量)。右图是某种锂-空气电池的装置示意图,放电时,下列说法不正确的是
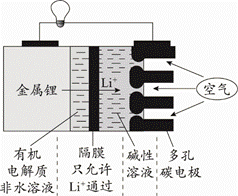
A.金属锂为负极
B.若隔膜被腐蚀,不会影响该电池正常使用
C.多孔碳电极上发生的电极反应为:O2 + 2H2O + 4e- === 4OH-
D.锂-空气电池能量密度大的原因之一是转移等量电子时,金属锂比LiFePO4质量小
12.H2O2是一种“绿色”试剂,许多物质都会使较高浓度的H2O2溶液发生催化分解。实验发现,向H2O2溶液中加入Br2可以加快其分解速率。有人提出反应机理可能有2步,第1步反应为:H2O2 + Br2 === 2H+ + O2↑+ 2Br-。下列说法正确的是
A.H2O2分子中含有离子键和非极性键
B.在第1步反应中,每生成0.1 mol O2,转移0.4 mol电子
C.机理中第2步反应为:2H+ + H2O2 + 2Br- === 2H2O + Br2
D.若在加入Br2的H2O2溶液中检出Br-,则说明第1步反应发生了
13.某电路板生产企业的水质情况及国家允许排放的污水标准如下表所示。为研究废水中Cu2+处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。
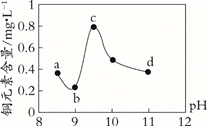
查阅资料,平衡I:Cu(OH)2 + 4NH3
 [Cu(NH3)4]2+ + 2OH-;
[Cu(NH3)4]2+ + 2OH-;平衡II:Cu(OH)2 + 2OH-
 [Cu(OH-)4]2-
[Cu(OH-)4]2-| 项目 | 废水水质 | 排放标准 |
| pH | 1.0 | 6~9 |
| Cu2+/ mg·L-1 | 72 | ≤0.5 |
| NH4+/ mg·L-1 | 2632 | ≤15 |
A.废水中Cu2+处理的最佳pH约为9
B.b~c段:随pH升高,Cu(OH)2的量增加,平衡I正向移动,铜元素含量上升
C.c~d段:随pH升高,c(OH-)增加,平衡I逆向移动,铜元素含量下降
D.d点以后,随c(OH-)增加,铜元素含量可能上升
14.以废治废、变废为宝可以实现资源的综合利用。用废铁块、废盐酸可以生产净水剂聚合氯化铁和高铁酸钠,转化关系如图所示:
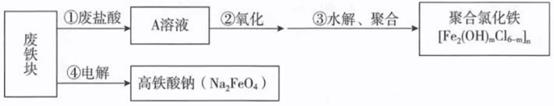
(1)A溶液中一定含有的溶质是_______。
(2)若使③中水解程度变大,可采取的措施是_______(填字母序号)。
a.加热 b.加入NaHCO 3 c.加入NH4Cl
(3)写出③中水解生成Fe2(OH) m Cl6-m反应的化学方程式:______。
(4)将废铁块进行预处理制成电极,通过电解制备高铁酸钠,该装置原理示意图如图所示。铁块做_______(填“阳极”或“阴极”),对应的电极反应式为_______。

(5)高铁酸钠在水中缓慢产生红褐色沉淀和一种气体,该反应的离子方程式:_______。
15.含氮、磷污水过量排放引起的水体富营养化是当前备受关注的环境问题。
(1)氮肥、磷肥都可以促进作物生长。氮、磷元素在周期表中处于同一主族,从原子结构角度分析它们性质相似的原因是_______,性质有差异的原因是_______。
(2)氮的化合物在水中被细菌分解,当氧气不充足时,在反硝化细菌的作用下,细菌利用有机物(又称碳源,如甲醇)作为电子供体,将硝态氮的化合物(含NO3-)连续还原最终生成N2,发生反硝化作用,完成下述反应的方程式:
+ 5CH3OH
 ↑ + CO32- + 4HCO3- +
↑ + CO32- + 4HCO3- + (3)某小组研究温度对反硝化作用的影响。在反应器内添加等量的相同浓度的甲醇溶液,从中取污泥水混合液分置于4个烧杯中,使4个烧杯内的温度不同,将实验数据作图如图。由图像分析产生差异的原因是:_______。
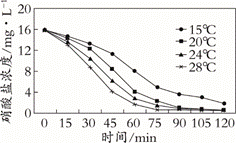
(4)某小组研究浓度对反硝化作用的影响。
①保持其他条件相同,在反应器内添加不等量的甲醇溶液,使4个烧杯碳源浓度依次为183 mg•L-1、236 mg•L-1、279 mg•L-1和313 mg•L-1。该小组预测反硝化速率变化的趋势是增大,预测依据是_______。
②碳源为183 mg•L-1的污水经过2 h的反硝化试验,可使NO3-由15.0 mg•L-1降至8.8 mg•L-1。已知M(NO3-) = 62 g•mol-1,NO3-的转化速率是________mol (L•h)-1。
16.某冶炼厂利用含ZnO的烟灰脱除工业废气中的SO2,最终得到锌盐。该厂所用烟灰的主要成分如下表所示:
| 主要成分 | ZnO | CaO | Fe2O3 | SiO2 | 其它 |
| 质量分数/% | 81 | 0.098 | 1.14 | 0.5 | ———— |
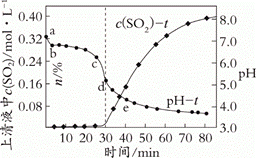
(1)纯ZnO浆液的pH为6.8,但上述烟灰浆液的初始pH为7.2。在开始脱硫后3 min内(a~b段),pH迅速降至6.8,引起pH迅速变化的原因是_____(结合化学用语解释)。
(2)生产中脱除SO2效果最佳的时间范围是_____(填字母序号)。
A.20~30 min B.30~40 min C.50~60 min D.70~80 min
(3)在脱硫过程中涉及到的主要反应原理:
Ⅰ.ZnO+ SO2 === ZnSO3↓
Ⅱ.ZnSO3 + SO2 + H2O ===Zn(HSO3)2
①在30~40 min时,主要发生反应II,生成可溶性的Zn(HSO3)2。上清液中c(SO2)上升的原因可能是______。
②在30~80 min时,pH降低的原因可能是______(写出2点)。
③将脱硫后的混合物利用空气氧化技术处理,该过程中发生反应:2ZnSO3 + O2 === 2ZnSO4和______。