 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 泉州市2021届高中毕业班质量监测(五) | |
|---|---|
| 本卷共有试题:14 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 三星堆遗址最近出土了青铜神树、黄金权杖、玉器等文物,下列有关说法不正确的是 A.青铜神树体现了中国古代高超的冶金技术 B.青铜表面的绿色物质主要为Cu2(OH)2CO3 C.青铜神树、黄金权杖、玉器均为合金材料 D.玉器因含有不同金属氧化物而显现不同颜色 |
|||
答案 |
C | |||
| 题号 | 2 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 设NA为阿伏加德罗常数的值,下列说法正确的是 A.标准状况下,2.24LC3H8分子中的σ键的数目为1.1NA B.5.6gFe在7.1gCl2中充分燃烧,转移电子数为0.2NA C.0.1molNO与0.1molO2混合物中质子数为2.3NA D.室温下,pH=9的CH3COONa溶液中,由水电离的H+数目为10-9NA |
|||
答案 |
B | |||
| 题号 | 3 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 二氢黄樟油素是一种常见的日化香料,可用香桂油为原料制取,反应如下:下列说法不正确的是 A.香桂油能发生聚合反应、还原反应 B.香桂油分子中所有碳原子可能共平面 C.二氢黄樟油素的一氯代物有6种 D.可用溴水鉴别以上两种有机物 |
|||
答案 |
C | |||
| 题号 | 4 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 常温下,下列各组离子在指定溶液中能大量共存的是 A. 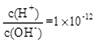 的溶液中:Na+、K+、SO32-、AlO2- 的溶液中:Na+、K+、SO32-、AlO2-B.c(Fe2+)=0.5mol・L-1的溶液中:H+、Mg2+、SO42-、ClO― C.无色溶液中:Na+、Fe3+、SO42-、HCO3- D.能使酚酞变红的溶液中:Al3+、NH4+、Cl―、NO3- |
|||
答案 |
A | |||
| 题号 | 5 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | X、Y、Z、W为原子序数依次增大的短周期主族元素,四种元素组成的某种化合物可用于防治蛀牙,该化合物的结构如图所示,以下有关说法正确的是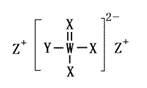 A.简单离子半径:Z>Y>X B.最简单氢化物稳定性:Y>X>W C.Y、Z形成的化合物水溶液呈中性 D.WY5所有原子最外层均为8电子结构 |
|||
答案 |
B | |||
| 题号 | 6 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 以CO2和甲醇(MeOH)为原料合成碳酸二甲酯(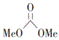 )的催化反应机理如图所示。下列说法不正确的是 )的催化反应机理如图所示。下列说法不正确的是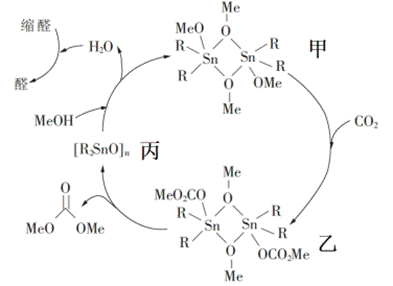 A.总反应为:2MeOH+CO2= 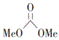 +H2O +H2OB.乙是该反应的中间体 C.甲→乙过程中Sn的配位数未发生改变 D.加入缩醛能使总反应平衡逆向移动 |
|||
答案 |
D | |||
| 题号 | 7 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 从含砷(As)的有毒工业废水中提取粗As2O3,流程如下: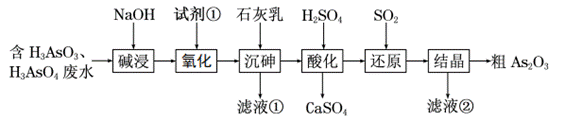 已知:As与P同为VA族元素;Ca3(AsO3)2微溶于水,Ca3(AsO4)2难溶于水。 下列说法不正确的是 A.试剂①的作用是将AsO33-氧化为AsO43- B.滤液①主要成分为NaOH溶液 C.滤液②主要成分可以循环利用 D. “还原”的离子方程式:2H++2AsO43-+2SO2=2SO42-+As2O3↓+H2O |
|||
答案 |
D | |||
| 题号 | 8 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 利用CO2电催化还原法制取清洁燃料HCOOH,可实现温室气体CO2的资源化利用。其工作原理如图。下列有关说法不正确的是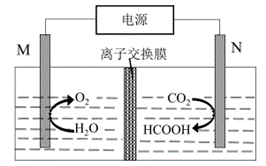 A.M为阳极 B.离子交换膜为阴离子交换膜 C.N极的电极反应式为CO2+2e-+2H+=HCOOH D.消耗的CO2与生成的O2物质的量之比为2:1 |
|||
答案 |
B | |||
| 题号 | 9 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 下列装置能达成相应实验目的的是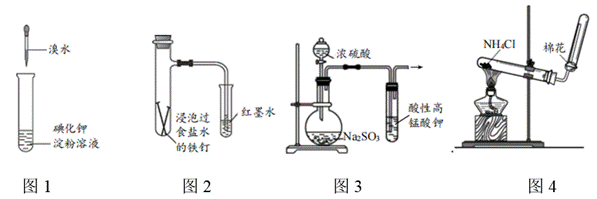 A.图1:比较溴与碘的非金属性强弱 B. 图2:探究铁钉的析氢腐蚀 C.图3:验证二氧化硫的漂白性 D. 图4:制备并收集氨气 |
|||
答案 |
A | |||
| 题号 | 10 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 25℃时,不同pH环境下H 2C2O4不同形态的粒子的分布系数(δ)如图1.用0.200mol・L-1H 2C2O4溶液滴定20.00mL0.400mol・L-1NaOH溶液所得滴定曲线如图2.下列说法不正确的是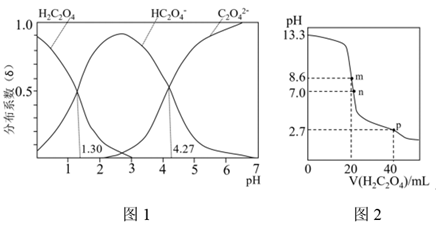 A.H 2C2O4的Ka1=1×10-1.30 B.点n所示溶液中:c(HC2O4-)+ 2c(C2O42-)=c(Na+) C.点m到p的溶液中:水的电离程度逐渐减小 D.点p所示溶液中:c(Na+)>c(HC2O4-)>c(H 2C2O4)>c(C2O42-) |
|||
答案 |
D | |||
| 题号 | 11 |
|
||||||||||||||||||||||||||||||||||||
出处 |
2021泉州五检 | |||||||||||||||||||||||||||||||||||||
| 题干 | 工厂处理电镀废水会产生电镀污泥。某镀镍污泥酸浸的滤液含Ni2+、Al3+、Fe2+、Cr3+、Cu2+等离子,可用如下工艺流程回收硫酸镍晶体。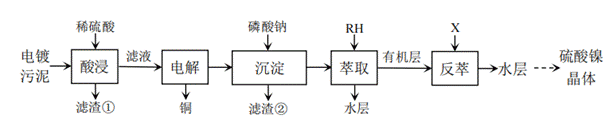 已知:镍的萃取、反萃过程反应为2RN+Ni2+  R2Ni+2H+ R2Ni+2H+(1)检验酸浸滤液中含Fe2+的试剂为_______。 (2)“电解”过程,阴极的电极反应式为_______。 (3)滤渣②主要成分为AlPO4、FePO4、CrPO4不同电解电压、电解时间下Fe2+、Cr4+离子的检测结果如下表所示,电解酸浸滤液的最佳电压和时间分别是_______。
(5)“反萃”中,加入的X是_______。 (6)为测定硫酸镍晶体(NiSO4・nH2O)组成,进行如下实验:取 5.260g样品,配成250mL溶液,量取25.00mL溶液,用0.100mol・L-1的EDTA(Na2H2Y)标准液滴定(反应为Ni2++H2Y2-=NiY2-+2H+)。重复滴定3次,平均消耗EDTA标准液20.00mL,则硫酸镍的化学式为_______。 |
|||||||||||||||||||||||||||||||||||||
答案 |
(1)KSCN溶液和氯水或酸性KMnO4溶液或K3[Fe(CN)6]溶液 (2)Cu2++2e-=Cu (3)2.5V,3.1h (4)2.46×10-12mol・L-1 (5)稀硫酸(或H2SO4) (6)NiSO4・6H2O |
|||||||||||||||||||||||||||||||||||||
| 题号 | 12 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 瑞尼镍是一种多孔活性金属镍,某兴趣小组用瑞尼镍作催化剂制取氢化肉桂酸: 已知:①金属镍(Ni)常温难以被氧气氧化; ②瑞尼镍孔隙会吸附大量氢气而活化,活化的瑞尼镍接触空气易自燃。 实验步骤如下: I.制取瑞尼镍:在烧杯中加入浓NaOH溶液,在冰水浴中分批加入铝镍合金(1:1),不断搅拌,充分反应后,分离得到瑞尼镍,保存于无水乙醇中。 II.用如图装置(夹持、搅拌及加热装置省略)制取氢化肉桂酸,步骤如下: 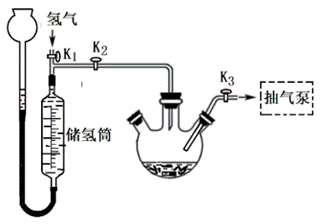 ①检查装置气密性,往三颈烧瓶中加入ag肉桂酸、一定量乙醇和I中制得的瑞尼镍。 ②通过反复抽气与充气将装置内空气替换成氢气,关闭K3、K2,打开K1,充入氢气至储氢筒充满氢气,…… ③搅拌并加热三颈烧瓶,充分反应后分离出氢化肉桂酸。 回答以下问题: (1)铝镍合金与NaOH溶液反应的化学方程式为_______。 (2)制取瑞尼镍的有关说法不正确的是_______。 A.该反应为放热反应 B.合金中铝含量过低会减少瑞尼镍的孔隙数量 C.分离得到活性瑞尼镍的方法:过滤 D.检验活性瑞尼镍的方法:取少量样品,用滤纸吸干表面的乙醇,放置于空气中,观察现象 (3)将步骤②的操作补充完整:_______。 (4)三颈烧瓶加热的方式为_______。反应过程中,保持长颈漏斗中液面始终高于储氢筒内液面较多的目的:将储氢筒内的氢气压入三颈烧瓶、_______。判断反应已充分进行的现象为_______。 (5)若参加反应的氢气体积为bmL(标准状况),则氢化肉桂酸的产率为_______。(用含a、b的代数式) (6)从三颈烧瓶中分离出瑞尼镍,得到混合液。从混合液中回收乙醇的操作方法是_______。 |
|||
答案 |
(1)2Al+2NaOH+2H2O=2NaAlO2+3H2↑或2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑ (2)C (3)关闭K1,打开K2(或打开K2,关闭K1) (4)水浴加热 增大压强,加快反应速率 储氢筒中液面不再上升或保持不变(或长颈漏斗中液面不再下降) (5) 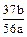 % %(6)蒸馏 |
|||
| 题号 | 13 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 近日,我国研究人员利用硫氰酸甲基铵{[CH3NH3]+[SCN]-}气相辅助生长技术,成功制得稳定的钙钛矿型甲脒铅碘(FAPbI3)。请回答下列问题: (1)基态S原子的价电子排布图为_______。 (2)硫氰酸根离子(SCN-)的结构式为_______。 (3)甲脒(FA)的结构简式为 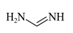 ①其组成元素的电负性由小到大的排序为_______,其中碳原子的杂化方式为_______。 ②甲脒比丙烷的熔点更高的原因是_______。 (4)水中铅测定方法是用双硫腙与铅反应生成红色双硫腙铅络合物(图1) 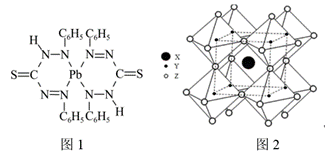 ①该络合物可溶于四氯化碳,其晶体类型为_______。 ②该络合物分子内不存在的微粒间作用力有_______。(选填序号) a.σ键 b.π键 c.非极性键 d.配位健 e.离子键 (5)FAPbI3的晶体结构单元如图2所示,图中Y表示Pb,位于八面体中心,则甲脒的碘配位数为___。 |
|||
答案 |
(1)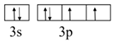 (2)[S-C≡N]-或[S=C=N]- (3)H<C<N sp2杂化 脒存在分子间氢键,丙烷分子间只存在范德华力 (4)分子晶体 e (5)12 |
|||
| 题号 | 14 |
|
||
出处 |
2021泉州五检 | |||
| 题干 | 新假荆芥内酯(neonepetalactone)可用作杀虫剂,其合成路线如下: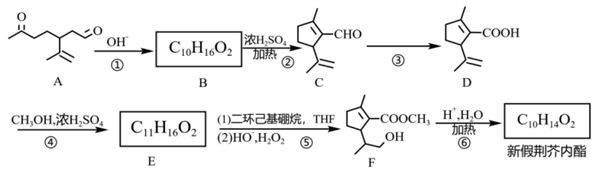 已知: ① 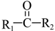 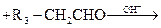 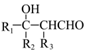 ② 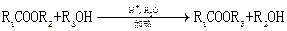 (1)B的含氧官能团名称为_______ (2)下列有关说法正确的是_______ A.A的分子式为C10H16O2 B.C分子中有手性碳原子 C.③的反应条件可为“酸性KMnO4溶液” D.1molD最多与3molH2加成 (3)E的结构简式为_______ (4)已知新假荆芥内酯分子结构含两个环,⑥的化学方程式为_______ (5)D的同分异构体中能同时满足以下三个条件的有_______种(不考虑立体异构) ①属于芳香族化合物 ②苯环上有两种不同化学环境的氢原子且个数比为1:2 ③1mol有机物最多能与2molNaOH溶液反应 |
|||
答案 |
(1)羟基、醛基 (2)AB (3) 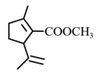 (4) 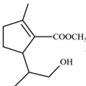  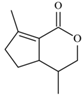 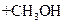 (5)8 |
|||
| v福建省实践教学工作室 蔡实践 设计制作 v |