 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出
登录 注册
注册 首页
首页 题库检索
题库检索 我的试卷夹
我的试卷夹 编辑板
编辑板 试卷库
试卷库 个人菜单
个人菜单 化学社区
化学社区 实践课堂
实践课堂 退出
退出 |
| 我的试卷夹 | 编辑板 | 试题检索 | 新建试卷 | 个人菜单 | 组卷帮助 |
|---|
| 惠州市2019届高三第三次调研考理科综合化学试题 | |
|---|---|
| 本卷共有试题:9 | 【下载本试卷】【下载试卷答案】 【整份卷另存在我的试卷夹】【 整份卷放入试卷编辑板】 |
| 题号 | 1 |
|
||
出处 |
2019惠州调研 | |||
| 题干 | 下列有关物质性质与用途具有对应关系的是 A.H2O2具有还原性,可用作丝织品的漂白剂 B.BaCO3能与盐酸反应,可用作胃酸的中和剂 C.碳的非金属性强于硅,可用作工业上制粗硅 D.FeCl3溶液具有氧化性,可用作铜制线路板的蚀刻液 |
|||
答案 |
C | |||
| 题号 | 2 |
|
||
出处 |
2019惠州调研 | |||
| 题干 | 某同学取海带灰加蒸馏水煮沸2~3 min,冷却,过滤,获得含I−的溶液,并设计以下实验方案,从中提取I2。 下列说法中错误的是 A.试剂b可能是CCl4 B. “I2的悬浊液→粗碘”需萃取 C.“下层溶液”可在流程中循环利用 D.反应1、反应2、反应3都是氧化还原反应 |
|||
答案 |
B | |||
| 题号 | 3 |
|
||
出处 |
2019惠州调研 | |||
| 题干 | 化合物(a) 、(b) 、(b) 、(c) 、(c)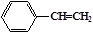 ,(d) ,(d)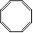 ,下列说法不正确的是 ,下列说法不正确的是A.a、b、c、d互为同分异构体 B.除a外均可发生加成反应 C.c中所有原子不可能处于同一平面 D.一氯代物同分异构体最多的是c |
|||
答案 |
C | |||
| 题号 | 4 |
|
||
出处 |
2019惠州调研 | |||
| 题干 | 设NA为阿伏加德罗常数的值,下列说法不正确的是(Na-23 C-12 O-16 Fe-56) A.8.4gNaHCO3晶体中离子总数为0.2NA B.12g金刚石中含有的共价键数为2NA C.pH=13的NaOH溶液中含有的OH-数目为0.1NA D.5.6gFe与过量的氯气充分反应转移的电子总数为0.3NA |
|||
答案 |
C | |||
| 题号 | 5 |
|
||
出处 |
2019惠州调研 | |||
| 题干 | 短周期主族元素X、Y、Z、W原子序数依次增大,X、Y、Z的最外层电子数之和与W的最外层电子数相等,X的最高正价为+4,Y是海水中含量最多的金属元素。下列说法不正确的是 A.原子半径:r(Y)>r(Z)>r(X) B.W的氢化物的稳定性比X的最简单氢化物的稳定性弱 C.W分别与Y、Z形成的化合物所含的化学键类型相同 D.Y的最高价氧化物对应的水化物碱性比Z的强 |
|||
答案 |
B | |||
| 题号 | 6 |
|
||
出处 |
2019惠州调研 | |||
| 题干 | 实验室可利用下列微生物电池将污水中的乙二胺[H2N(CH2)2NH2]转化为无毒无害的物质并产生电能(M、N均为石墨电极)。有关该电池工作时的说法中错误的是 A.M极的电势比N极的电势低 B.正极电极反应式:O2+4e-+4H+=2H2O C.电池总反应为:H2N(CH2)2NH2+ 4O2=N2 + 2CO2 +4H2O D.每消耗5.6升O2时,通过质子交换膜的质子数为NA 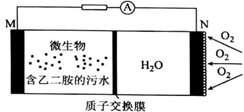 |
|||
答案 |
D | |||
| 题号 | 7 |
|
||
出处 |
2019惠州调研 | |||
| 题干 | 常温下,青蒿素是一种无色针状晶体,易溶于有机溶剂,难溶于水,熔点约为156.5℃,易受湿、热的影响而分解。某实验小组对青蒿素的提取和组成进行了探究。 Ⅰ.提取流程:  ⑴“破碎”的目的是_______________________________________。 ⑵操作a和操作b的名称分别是_________、___________。 ⑶操作a用到的玻璃仪器有玻璃棒、_____________________。 ⑷操作a所用青蒿必须干燥且不宜加热,原因是_______________________________。 Ⅱ.燃烧法测定最简式: 实验室用下图所示装置测定青蒿素(烃的含氧衍生物)中氧元素的质量分数。 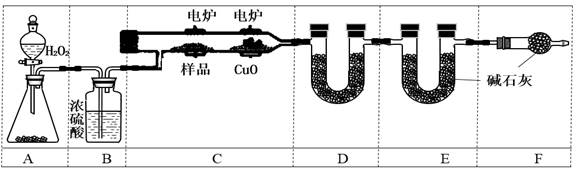 ⑸实验前至少称量_________个质量数据。 ⑹装置D中所盛固体可以是____(用对应符号填空);(a.生石灰b.CaCl2 c.CuSO4 d.碱石灰) F的作用是________________ _______。 ⑺A中固体分别用MnO2、KMnO4时产生等量O2,消耗H2O2的物质的量之比为______。(生成的O2全部放出,与KMnO4反应的H2O2经过酸化) ⑻燃烧m g青蒿素,图中D、E的质量分别增重a g、b g,则青蒿素中氧元素的质量分数可表示为_________________(只写计算式,用含有m、a、b的符号来表示,不化简)。 |
|||
答案 |
⑴扩大接触面积,便于青蒿素被乙醚浸出 ⑵过滤、蒸馏 ⑶漏斗、烧杯 ⑷青蒿素易受湿、热的影响而分解 ⑸3 ⑹b 防止空气中的H2O和CO2被E吸收而影响实验结果 ⑺2∶1(或2) ⑻  |
|||
| 题号 | 8 |
|
||
出处 |
2019惠州调研 | |||
| 题干 | 能源开发、环境保护、资源利用等是化学应用的重要方向。回答下列问题: ⑴催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。 已知:N2(g) + O2(g)=2NO(g) △H1=+180.5 kJ · mol-1; 2C(s)+ O2(g)=2CO(g) △H2=-221.0 kJ · mol-1; C(s)+ O2(g)=CO2(g) △H3=-393.5 kJ · mol-1 则尾气转化反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H =________________。 ⑵CO2可通过反应CO2(g)+CH4(g)  2CO(g)+2H2(g)来制取H2。在1.0L密闭容器中充入CO2、CH4各1mol,发生上述反应,测得CH4的平衡转化率与温度压强的关系如图a所示 2CO(g)+2H2(g)来制取H2。在1.0L密闭容器中充入CO2、CH4各1mol,发生上述反应,测得CH4的平衡转化率与温度压强的关系如图a所示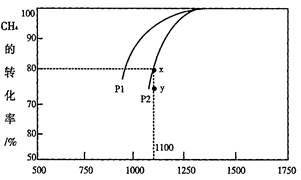 ① 由图a可知,压强P1______P2(填“大于”或“小于”),该反应的△H_______0(填“大于”或“小于”) ② 当压强为P2时,y点的υ(正)____ υ(逆) (填“大于”、“小于”或“=”);y点对应温度下,该反应的平衡常数K=___________(保留四位有效数字)。 ③ 实验表明,温度高于1250℃时,容器中c(CO2)>c(CH4),请结合两种反应物的性质分析可能的原因:_______________________________________________。 ⑶  汽车尾气分析仪对CO的含量分析是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质中自由移动。 汽车尾气分析仪对CO的含量分析是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质中自由移动。① 请写出负极反应式:_______________________,②该仪器工作时,O2-移向_______极(填写a或b)。 |
|||
答案 |
⑴-746.5 kJ · mol-1 ⑵ ①小于大于 ②大于 163.8 ③CH4在高温下分解使其浓度减小,CO2较稳定 ⑶CO2+4H2 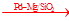 CH4 + 2H2O(用箭号不作为扣分,不写条件扣1分) CH4 + 2H2O(用箭号不作为扣分,不写条件扣1分)⑷①CO + O2-―2e-=CO2 ②a |
|||
| 题号 | 9 |
|
||
出处 |
2019惠州调研 | |||
| 题干 | 我国科学家研制的第二代“彩虹鱼”万米级深海着陆器所用的金属材料主要是钛合金。以钛铁矿(成分:FeTiO3及少量Fe2O3、FeO等杂质)为主要原料制钛的流程如下: 已知:①钛在常温下不与强酸、强碱反应; ②Ti4+易水解生成TiO2+, TiO2+进一步水解可得H2TiO3。 ⑴ “废气”中含有少量空气污染物,其分子式为________。 ⑵ “150-200℃溶煮”时生成Ti(SO4)2和TiOSO4且有气体产生,写出生成TiOSO4反应的化学方程式_______________________________________________。 ⑶ 沉淀池中加入Fe时,开始无气泡,溶液由棕黄色变浅绿色,片刻后有无色无味气体产生。写出Fe参与的离子反应方程式____________________________。 ⑷ 已知FeSO4在水中的溶解度曲线如图所示,由此可知在沉淀池由溶液获得目标物质的方法是______________。 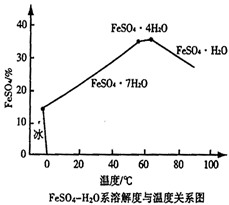 ⑸ “加热煮沸”操作的主要目的是_____________。 ⑹ 简述“精炼”阶段,从Ti、Mg混合物获得Ti的实验方案是_____________________________。 |
|||
答案 |
⑴SO2 ⑵ 2FeTiO3 + 6H2SO4 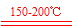 Fe2(SO4)3 + SO2↑+ 2TiOSO4 + 6H2O Fe2(SO4)3 + SO2↑+ 2TiOSO4 + 6H2O⑶Fe + 2Fe3+=3Fe2+ ,Fe + 2H+ =Fe2+ +H2↑ ⑷ 蒸发浓缩,冰水浴中冷却,过滤(3分) ⑸ 使反应液升温并充分混合;促进Ti4+、TiO2+水解生成H2TiO3 ⑹将混合物投入足量稀盐酸中充分反应后,过滤、洗涤、干燥 |
|||
| v福建省实践教学工作室 蔡实践 设计制作 v |