 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| �人��2019����б�ҵ�����µ��в��������ۺ��Ծ� | |
|---|---|
| �����������⣺11 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
2019�人���� | |||
| ��� | ������(��Ҫ�ɷ�ΪFe2O3��FeO������Fe)�Ʊ�����F3O4��������ʾ��ͼ���£�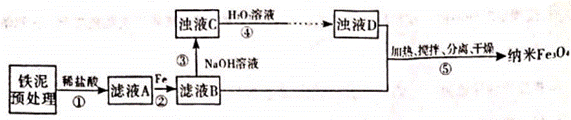 ��������������� ��A.Ϊ��߲���ٵķ�Ӧ���ʣ��ɲ�ȡ���衢���µȴ�ʩ ��B.������У���Ҫ��Ӧ�����ӷ���ʽ��2Fe3++Fe===3Fe2+ ��C������У���Ӧ��ɺ�ʣ���H2O2�����ȥ ��D������У������롱�����IJ����й��ˡ�ϴ�� |
|||
�� |
C | |||
| ��� | 2 |
|
||||||||||||||||||||
���� |
2019�人���� | |||||||||||||||||||||
| ��� | ���ô�����Ʒ��ָ�����Լ����ʵ���ܴﵽʵ��Ŀ�ĵ���
|
|||||||||||||||||||||
�� |
D | |||||||||||||||||||||
| ��� | 3 |
|
||
���� |
2019�人���� | |||
| ��� | ij�о���С��Ϊ��̽��ʯ���ͷֽ������������ʵ�鷽��������˵���������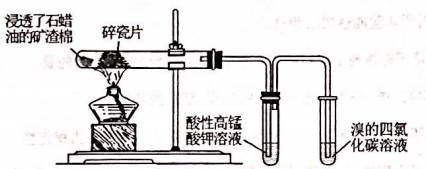 ��A.ʯ������ʯ�ͼ�ѹ����IJ��� ��B.���Ƭ�ӿ���ʯ���͵ķֽ� ��C.���Ը��������Һ��ɫ˵����������ϩ ��D.������Ȼ�̼��Һ��ɫ����Ϊ�����˼ӳɷ�Ӧ |
|||
�� |
C | |||
| ��� | 4 |
|
||
���� |
2019�人���� | |||
| ��� | ��NA�ǰ����ӵ�������ֵ������˵����ȷ���� ��A.��״���£� 4 4.8 LCHCI3�к�����ԭ�ӵ���ĿΪ6NA ��B.1mol������(C6H12O6)���Ӻ��е��ǻ���ĿΪ5NA ��C.7gLi�ڿ�������ȫȼ��ת�Ƶĵ�����Ϊ2NA ��D.0.5moV/L NH4NO3��Һ�к��е�NH4+��ĿС��0.5NA |
|||
�� |
B | |||
| ��� | 5 |
|
||
���� |
2019�人���� | |||
| ��� | ��֮�乲��һ��̼ԭ�ӵĻ������Ϊ�ݻ������1��4-��������[2.2]����Ľṹ��ʽΪ ������˵����ȷ���� ������˵����ȷ������A.1mol���л�����ȫȼ����Ҫ4molO2 ��B.���л�����HCOOCH=CH2��Ϊͬ���칹�� ��C.���л���Ķ��ȴ�����3�� ��D.���л�������ԭ�Ӿ�����ͬһƽ�� |
|||
�� |
B | |||
| ��� | 6 |
|
||
���� |
2019�人���� | |||
| ��� | ����������Ԫ��X��Y��Z��W��ԭ������������������Y��Zλ��ͬһ���塣X����̬�⻯�ﳣ�����������ZYW2����ˮ���ҷ�Ӧ���ɹ۲쵽Һ�����������ɣ����д̼�����ζ�������ݳ��������ʹƷ����Һ��ɫ������˵����ȷ���� ��A.����⻯��ķе㣺Z>Y ��B.ԭ�Ӱ뾶��W>Z>Y>X ��C.��ZY2ͨ��ʯ����Һ���ȱ�����ɫ ��D.��ZYW2��ˮ��Ӧ�����Һ�еμ�AgNO3��Һ�а�ɫ�������� |
|||
�� |
D | |||
| ��� | 7 |
|
||
���� |
2019�人���� | |||
| ��� | ������.�� 10m0.1 mol/L CuCl2��Һ�еμ�0.1 mol/L Na2S��Һ�μӹ����У�lgc(Cu2+)��Na2S��Һ���(V)�Ĺ�ϵ��ͼ��ʾ������˵���������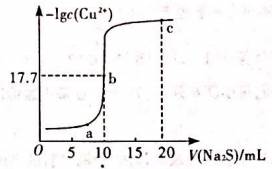 ��A.Ksp(CuS)��������Ϊ10��35 ��B.�����ϸ������Һ�������ϵʽc(S2��)��e(Cu2+)=Ksp(CuS) ��C.a��b��c�����У���ˮ�����c(H+)��c(OH��)�Ļ���С��Ϊb�� ��D.c����Һ�У�c(Na+)>c(Cl��)>c(S2��)>c(OH��)>c(H+) |
|||
�� |
A | |||
| ��� | 8 |
|
||||
���� |
2019�人���� | |||||
| ��� | ��������(C12O)�Ǵ�����������������Ȼ����䲿���������£�
 2NaCl +2NaHCO3+ C12O 2NaCl +2NaHCO3+ C12O ��������װ�����ʵ���Ʊ�����C12O����̽��������ʵ����ʡ�  (1)װ��A������X������Ϊ___________�� (2)�����������������װ������˳����A��___________(ÿ��װ������һ��)�� (3)װ��F��ʢװ�Լ�������Ϊ___________�� (4)A�з�Ӧ�����ӷ���ʽΪ___________�� (5)��D���ռ�����Һ̬����ʱֹͣ��Ӧ����Ƽ�ʵ��֤��B�в��������к���NaHCO3��___________�� (6)ʵ����ɺ�ȡE���ձ�����Һ�μ�Ʒ����Һ������Һ��ɫ���ÿ��������ʵ��̽����Һ��ɫ��ԭ��  ��a=___________�� ��������ʵ��ó��Ľ�����___________�� |
|||||
�� |
(1)��Һ©���� (2)FBCDE���� (3)����ʳ��ˮ����NaCl��Һ�� (4)MnO2+4H++2Cl-  Mn2++Cl2��+2H2O������ (5)ȡB�й����������Թ��У�������ˮ�ܽ⣬�μӹ���BaCl2��Һ�����ã�ȡ�ϲ���Һ����һ�Թ��У��ٵμ�Ba(OH)2��Һ���а�ɫ�������ɡ�������(6)5.0���� Mn2++Cl2��+2H2O������ (5)ȡB�й����������Թ��У�������ˮ�ܽ⣬�μӹ���BaCl2��Һ�����ã�ȡ�ϲ���Һ����һ�Թ��У��ٵμ�Ba(OH)2��Һ���а�ɫ�������ɡ�������(6)5.0���� ��(7)������������ͬʱ����Һ�ļ���Խǿ������������ҺƯ������Խ���� |
|||||
| ��� | 9 |
|
||
���� |
2019�人���� | |||
| ��� | ��ҵ�������̿�(��Ҫ�ɷ�ΪMnO2������������FeCO3��Al2O3��SiO2)Ϊԭ����ȡ�����̵Ĺ����������£�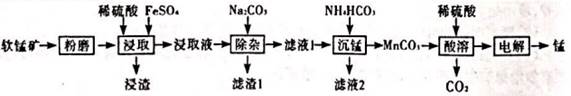 (1)���̿�ĥ����Ŀ����___________�� (2)������������Ҫ�ɷ���___________�� (3)����⡰ûȡҺ������Fe2+������ȡ"ʱMnO2������Ӧ�����ӷ���ʽΪ___________�� (4)�ڡ����̡������У�������Na2CO3����NH4HCO3����ԭ����___________�� (5)�������ܡ������Һ��Ϊ���Һ������ͼ1װ�õ��Ӧ����___________���ӽ���Ĥ(�����������)�������ĵ缫��ӦʽΪ___________�� 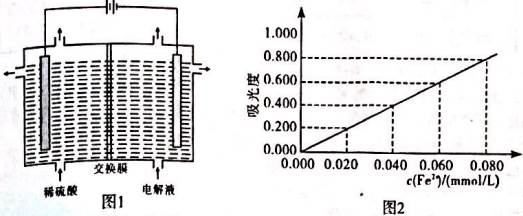 (6)Ϊ������á����� 1������ⶨ������AlԪ�صĺ�����������·����� �ٽ�mg����������amL��Һ�� ��ȡ����������Һ��EDTA�ζ������Һ��Fe3+��Al3+��Ũ��֮��Ϊb mmol/L�� ����ȡ����������Һ��Fe3+�������ǰ�(����Һ�п���ȫ�����NH3OH+��Cl��)��ԭFe2+�����ӷ���ʽΪ___________�� �ܽ���������Һ��������ȷ�����������Ϊ0.400(�������Fe2+��Ũ�ȹ�ϵ����ͼ2��ʾ)������Ʒ��AlԪ�ص���������Ϊ___________(�ú���ĸ�ı���ʽ��ʾ)�� |
|||
�� |
(1)�ӿ��ȡ���ʡ� (2)�������� (3)MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O������ (4)Na2CO3��Һ���Խ�ǿ���ᵼ�����������������(���ʽ̼����)������ (5)��������2H2O-4e-=4H++O2�������� (6)2Fe3++2NH3OH+=2Fe2++4H++N2��+2H2O������ 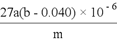 ��100% ��100% |
|||
| ��� | 10 |
|
||
���� |
2019�人���� | |||
| ��� | ��������������ɴ�����Ⱦ����Ҫ���ʡ��о���������ķ�Ӧ������������������Ⱦ����Ҫ���塣�ش��������⣺ (1)��֪NO2(g)===N2O4(g)��������H=��55.3kJ/mol N2O5 (g)=== NO2 (g)+  O2(g)��������H=+53.1 kJ/mol O2(g)��������H=+53.1 kJ/mol ��N2O5 (g)=== N2O4 (g)+2 O2(g)�������� ��H=___________ kJ/mol (2)����ϩ(C2H4)��Ϊ��ԭ������(NO)������������ͼ1������Ӧ��n(NO)�Un(O2)=2�U1�����ܷ�Ӧ�Ļ�ѧ����ʽΪ___________�����������¶ȡ�������(����ɸ�д�������������)�Ĺ�ϵ��ͼ2��Ϊ�ﵽ�������Ч����Ӧ���õ�������___________��  (3)T�¶�ʱ���ݻ�Ϊ 2L�ĺ����ܱ������з�����Ӧ��2NO(g)+O2(g)  2NO2(g)����H<0��ʵ���ã�v��=v(NO)����=2v(O2) ����=k��c2(NO)��c(O2)��v��=(NO2) ����=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO)��n(O2)����� 2NO2(g)����H<0��ʵ���ã�v��=v(NO)����=2v(O2) ����=k��c2(NO)��c(O2)��v��=(NO2) ����=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO)��n(O2)����� �� ���ٴ�0��2s�ڸ÷�Ӧ��ƽ������v(NO)=___________mol/(L��s)�� ��T1�¶�ʱ��ѧƽ�ⳣ��K=___________mol��1��L(�������3λ��Ч����)�� �ۻ�ѧƽ�ⳣ��K�����ʳ���k����k������ѧ��ϵ��K=___________�������������¶ȸı�ΪT2ʱ��k��=k������T2___________T2(�>������<����=") ����֪2NO(g)+O2(g)  2NO2�ķ�Ӧ����Ϊ�� 2NO2�ķ�Ӧ����Ϊ����һ��NO+NO  N2O2���� ����ƽ�� N2O2���� ����ƽ���ڶ���N2O2+O2��2NO2��������Ӧ ����������ȷ����___________(����)�� ����A.v(��һ��������Ӧ) ����C.�ڶ����Ļ�ܱȵ�һ���ĸ� ����D.�ڶ�����N2O2��O2����ײ100%��Ч |
|||
�� |
(1)-2.2������ (2)6NO+3O2+2C2H4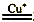 3N2+4CO2+4H2O������350�����ҡ�������3.0% 3N2+4CO2+4H2O������350�����ҡ�������3.0%(3)��0.03��������363�������� 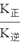 ����������>������BC ����������>������BC |
|||
| ��� | 11 |
|
||
���� |
2019�人���� | |||
| ��� | ���仯���������ǵĽ�������������������ء���ش��������⣺ (1)��̬��ԭ�Ӽ۵��ӹ����ʾʽΪ___________�����һ�����ܱ����___________(�� ��"��С��)�� (2).�ǻ���ʯ[Ca(PO4)3OH]�������е���Ҫ�����������ǻ�(��OH)����ԭ�ӵ��ӻ���ʽΪ___________��PO43���Ŀռ乹��Ϊ___________���û���������Ԫ�ص縺��������___________�� (3)P4O6�ķ��ӽṹ��ֻ���е�������ÿ��ԭ�ӵ�����㶼����8���ӽṹ����÷����к��еĹ��ۼ���Ŀ��___________�� (4)�����������(H3PO3)����Ԫ�ص����ֺ����ᡣ��������NOH��Ӧֻ����NaHPO3��NaH2PO3�����Σ���H3PO3�ĽṹʽΪ___________����Ϊ___________Ԫ�ᣬԭ����___________�� (5)ȷ����Ӽ���ˮ�����ɶ����ᣬ��ijһ���εĽṹ����ͼ��ʾ�� 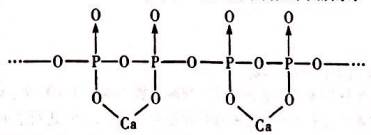 ��ͼ��֪�ö�������ε�ͨʽΪ___________�� (6)������һ�ֳ�Ӳ��ĥͿ����ϣ���������ͼ��ʾ�����ܶ�Ϊ��g/cm3����NA�ǰ����ӵ�������ֵ������ԭ�ӵ���λ��Ϊ___________����������Ϊ___________pm��  |
|||
�� |
(1).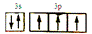 ������ ������ (2)sp3�� ���������Ρ�O(����Ԫ��) (3)12���� (4) 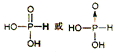 �������� �� �������� �� һ��H3PO3������ֻ�������ǻ����������ǻ��ϵ������롡���� (5)(CaP2O6)n������ (6)4����  ��1010 ��1010 |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |