 ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳�
��¼ ע��
ע�� ��ҳ
��ҳ ������
������ �ҵ��Ծ���
�ҵ��Ծ��� �༭��
�༭�� �Ծ���
�Ծ��� ���˲˵�
���˲˵� ��ѧ����
��ѧ���� ʵ������
ʵ������ �˳�
�˳� |
| �ҵ��Ծ��� | �༭�� | ������� | �½��Ծ� | ���˲˵� | ������� |
|---|
| 2018�����ʵ���⾫ѡ��1�� | |
|---|---|
| �����������⣺9 | �����ر��Ծ����������Ծ����� �����ݾ��������ҵ��Ծ������� ���ݾ������Ծ��༭���� |
| ��� | 1 |
|
||
���� |
�� | |||
| ��� | ���������(H2NCOONH4)��һ�ְ�ɫ���壬�dz�����ʵ��ҩƷ�����ɸ����NH3�����CO2���κα����·�Ӧ�õ���ÿ����1.0g��������立ų�2.05kJ���������ش��������⣺ (1)ʵ���ҿ�ѡ������װ��(I~V)�Ʊ������NH3��CO2�� 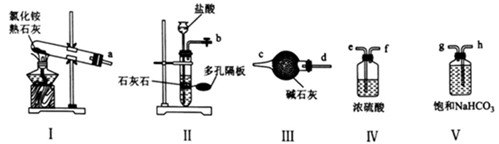 ����װ��I�����Ʊ�������NH3ʱ���ӿ�a��________________(��ӿ���ĸ)������װ��I�з�����Ӧ�Ļ�ѧ����ʽΪ________________________�� ���Ʊ�������CO2ʱ���������������ҵķ����ӿ�����˳��Ϊ________________(��ӿ���ĸ) (2)һ���Ʊ���������淋ĸĽ�ʵ��װ������ͼ��ʾ�� 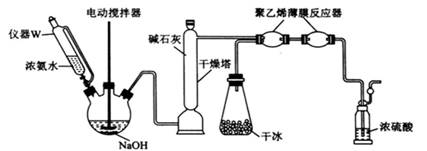 ��������W�����Һ©�����ŵ���________________________���øɱ�װ�ô���(1)���Ʊ�������CO2װ�õ��ŵ���________________________�� �ڡ���Ĥ��Ӧ�����з�����Ӧ���Ȼ�ѧ����ʽΪ________________________��ʢŨ�����װ�õ�������________________________________(�о�2��)�� ����ϵ������ˮ���������������ɵ������________________________(�ѧʽ)�� |
|||
�� |
��1����d�� 2NH4Cl+Ca(OH)2CaCl2+2NH3��+2H2O����bhgef���� ��2����ƽ��ѹǿ����ʹŨ��ˮһֱ˳������������ƿ��װ�ü�������CO2���辻������(��������¶ȵ����������NH3��CO2��ƽ��ת���ʣ��𰸺������ɣ������� ��2NH3(g)+CO2(g)===H2NCOOONH4(s)����H=-159.90kJ��mol−1������ ����δ��Ӧ�İ�������ֹ������ˮ�������뷴Ӧ����ͨ���۲��Ƿ������ݵ��ڵ��백ˮ�����ʵ�(��������������ŵ㼴�ɣ����� ��(NH4)2CO3(��NH4HCO3)������ |
|||
| ��� | 2 |
|
||||||||
���� |
�� | |||||||||
| ��� | ��������(NaNO2)��һ����Ҫ�Ļ���ԭ�ϣ�ijѧϰС��ͨ������ʵ���Ʊ��������ƣ����ⶨ���Ʊ��������ƵĴ��ȡ� I����������װ���Ʊ�NaNO2 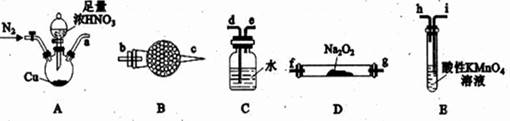 ��֪����2NO+Na2O2=2NaNO2����NO�ܱ�����KMnO4������NO2��MnO4-����ԭΪMn2+����ش��������⣺ (1)������ͼ�е�װ���Ʊ�NaNO2��������˳��Ϊa��__________(������������Сд��ĸ��ʾ)�� (2)ʵ�鿪ʼʱ����ͨһ��ʱ��N2��Ŀ����__________�� (3)װ��B��ʢ���Լ�������Ϊ__________��װ��C��������__________�� (4)װ��E�з�����Ӧ�����ӷ���ʽΪ____________________�� �ⶨ����ʵ�����Ʊ���NaNO2��Ʒ(��NaNO3����)�Ĵ��ȡ�����D��������Ʒag�ܽ�����Ƴ�250mL��Һȡ25.00mL����ƿ�У���bmol��L−1���Ը��������Һ�ζ����յ㡣�ظ������ζ��������Σ�����������±���
(6)����ʵ��������ܵ��³����ϱ��еڶ���ʵ�����ݵ���__________(����ĸ���)�� a.�ζ�ʱ�в������Ը��������Һ������ƿ�� b.������Ʒ��Һǰ����ƿδ������ c.�ζ�ǰ���Ӷ������ζ����Ӷ��� (7)����������Ʒ��NaNO2����������Ϊ__________(�ú�a��b�Ĺ�ϵʽ��ʾ)�� |
|||||||||
�� |
(1)d��e��b��c��f����g����g����f����i������ ��2���ų�װ���еĿ�������ֹNO������ΪNO2������ ��3����ʯ�һ���ˮ�Ȼ��ơ�������NO2ת��ΪNO������ ��4��5NO+3MnO+4H+===5NO+3Mn2++2H2O������ ��5����Һ����ɫ��Ϊ��ɫ�����Ϻ�ɫ�����Ұ���Ӳ���ɫ���� ��6��c������ ��7��34.5b/a��100�������� |
|||||||||
| ��� | 3 |
|
||
���� |
�� | |||
| ��� | FeCl3��һ�ֳ��õľ�ˮ������ѧ�о���С��ס��ҷֱ�����ͼװ���Ʊ���ˮFeCl3��֤����Ʒ��û��FeCl2����֪��ˮFeCl3�ڿ������׳��⣬������������ I��С���������ͼʵ��װ�����Ʊ���ˮFeCl3��(ÿ�����߿��ʾһ����Ԫװ��) 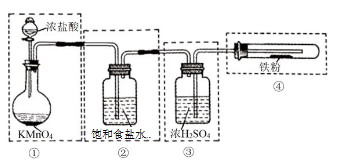 (1)������������������������װ�ܵĴ���_____________�� II��С����������װ����װ�Ʊ���ˮFeCl3��װ��: 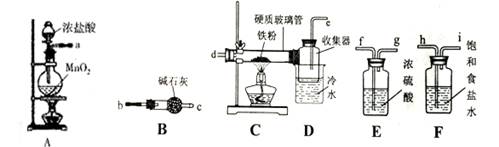 (2)A�з�����Ӧ�����ӷ���ʽΪ_______________�� (3)װ�ýӿڵ�����˳��Ϊ__________(��a��b��c����i��ʾ):��Ӧ��ʼǰӦ�ȵ�ȼ____���ƾ���(�A����C��)�� (4)װ��B������_________________�� (5)�����ȥE��Fװ�ã����ܵĺ����___________�� (6)֤����Ʒ��û��FeCl2�IJ���____________�� |
|||
�� |
��1�����е��ܸ�Ϊ�����̳��������Թܿڼ�һ�������ܻ��һ����ˮ���������β������װ�� ��2��MnO2+4H++2Cl−Mn2++Cl2��+2H2O ��3��a��hi��fg��de��b�� A�� ��4����ֹ��Ӧ����������е�ˮ��������Dװ����ʹ��ˮFeCl3���⣬����β������ֹ������Ⱦ���� ��5�������ȥE��Fװ�ã����ܻᷢ����ӦFe+2HCl===FeCl2+H2������C�м��������������Ļ�����壬������ը ��6��ȡ������Ʒ�ڱ������У��ô�������������ȡʣ��Ĺ������Թ�ˮ�У�������ˮ�ܽ⣬�����е���K3[Fe(CN)6]��Һ����Һ������������˵����Ʒ��û��FeCl2 |
|||
| ��� | 4 |
|
||
���� |
�� | |||
| ��� | ����������һ�ֹ�ҵ�Σ���������������Ӧ�ù㷺��������ͼ��ʾװ�ã��г�װ����ʡ�ԣ���ҩƷ��̽���������������ᷴӦ���������ɷ֡� ��֪����NO��NO2��2OH−===2NO��H2O������Һ�����¶ȣ�NO2��21�桢NO���C152�� 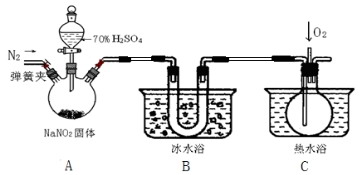 ��1����ӦǰӦ���ɼУ���ͨ��һ��ʱ�䵪�����ų�װ���еĿ�����Ŀ����__________�� ��2����ʵ��װ������ȱ���ǡ� ___________________________�� ��3���ڹرյ��ɼУ���Һ©������������70%�����A�в�������ɫ���塣 ��ȷ��A�в��������庬��NO�����ݵ�������____________________________�� ��װ��B��������_______________________________�� ��4��ͨ������ʵ��̽�����̣��ɵó�װ��A�з�Ӧ�Ļ�ѧ����ʽ��_______________�� ��5����ˮ����(N2H4��H2O)��һ����Ҫ�Ļ���ԭ�ϣ���ҽҩ��ũҵ��ȼ���϶����Ź㷺��Ӧ�á�Ŀǰ���ҹ�����ˮ���¾��������ط���������NaClO��Һ��NaOH��Һ������[CO(NH2)2]��Ӧ�Ƶô��£�N2H4�������ɴ��·�Ӧ�Ļ�ѧ����ʽΪ_______________�� �ڻ������ʱ�����£�N2H4��Ϊȼ�ϣ��������������������������������ʣ�д����Ӧ����ʽ_______�� |
|||
�� |
��1����ֹ�������ɵ�NO����ȫ������NO2����ɶ�A�з�Ӧ���������鲻��ȫ ��2����β������װ�� ��3��C�г��ֺ���ɫ���塡����ʹNO2��ȫҺ�� ��4��2NaNO2+H2SO4===Na2SO4+NO2��+NO��+H2O���� ��5��NaClO+CO(NH2)2+2NaOH===N2H4��H2O+Na2CO3+NaCl���� 2N2H4 +2NO2===3N2+4H2O |
|||
| ��� | 5 |
|
||
���� |
�� | |||
| ��� | ˮ�ϲ�������(FeC2O4��xH2O)������﮵�ص�ԭ�ϡ�������ˮ�������ֽ⡣ij��ѧ��ȤС��Բ���������һЩ���ʽ���̽�����ش���������: (1)��ˮ�ϲ������������������ᡣ�ֱ�ȡ2mL����Һ��3֧�Թ��У�����ʵ�顣��֤��ˮ�ϲ��������д���Fe2+���Լ���____(�����)�� ����A��KSCN��Һ���������������� B��K3[Fe(CN)6]��Һ���������������� C������KMnO4��Һ (2)Ϊ�ⶨˮ�ϲ��������нᾧˮ��������ʯӢ������(�����˿���K1��K2)(��Ϊװ��A)���أ���Ϊm1g������Ʒװ��ʯӢ�������У��ٴν�װ��A���أ���Ϊm2g������ͼ���Ӻ�װ�ý���ʵ�顣 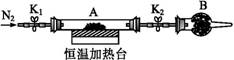 ʵ�鲽������: ����a����K1��K2������ͨ��N2�������� b�����¼���װ��Aһ��ʱ�� ����c��ͣ�ϼ��ȣ���ȴ�����¡��������� d���ر�K1��K2������A; ����e.��������������������Ϊm3g �����ٲ���ʵ�鲽��eΪ__________(��ʵ�������Ҫ��)�� �����ڲ���b������e����ͨ��N2��Ŀ����___________________�� (3)Ϊ̽�����������ķֽ�����(2)���Ѻ��ص�װ��A������ͼ��ʾ���ֵ�װ��(���ظ�ѡ��)����ʵ�顣��K1��K2������ͨ��N2����ּ��ȡ�ʵ���ʯӢ�������й��������һ���д��Եĺ�ɫ����� 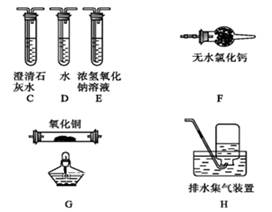 ������ʵ��װ���У��������ӵĺ���˳��ΪA��_______________�� ������֤��������CO���ɵ�������________________�� ������д�������������ȷֽ�Ļ�ѧ����ʽ________________�� |
|||
�� |
��1��B���� ��2���ظ�����a~d���裬ֱ��A���ء�����װ��A�е�ˮ�������ߣ�ͬʱ��ֹFeC2O4������������ ��3��C��E��C��F��G��C��H������Gװ�ú�ɫ�����죬����C�г���ʯ��ˮ����ǡ�3FeC2O4Fe3O4+4CO��+2CO2�� |
|||
| ��� | 6 |
|
||||||||||||
���� |
�� | |||||||||||||
| ��� | �뵼�幤ҵ��Ҫ�ߴ��裬�ֹ��к���SiO2��Fe2O3��CuO��C�����ʣ��ᴿ��ķ����Ƚ϶࣬�����������(��һ������)�ԭ�������Ȼ����ԭ��Ӧ�ý�Ϊ�㷺��������ʵ����ģ�ҵ����������ԭ���Ļ���ԭ���� 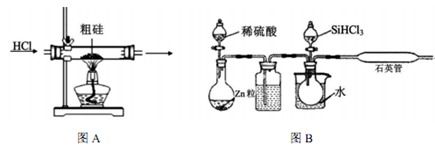 ��֪����Si+3HCl 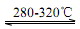 SiHCl3+H2(��Ҫ��Ӧ) SiHCl3+H2(��Ҫ��Ӧ) Si+4HCl 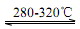 SiCl4+2H2(��Ҫ��Ӧ) SiCl4+2H2(��Ҫ��Ӧ) 2NaCl+H2SO4(Ũ)Na2SO4+2HCl�� �ڵ������Ҫ������IJ����������±���
(2)����װ����ʵ���ҿ������Ʊ�HCl�������_____(����ĸ����)�� 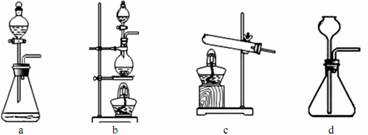 (3)��1100��1200�������£�����ͼB��ʯӢ���п��Ի�ù裬д���÷�Ӧ�ķ���ʽ_______�����ձ���ˮ��������__________________________����װ��ʹ��ʯӢ�ܶ�������ͨ�����ܵ�ԭ����_________�� (4)��������ԭ����SiHCl3��ͼB���ƹ裬����֮����_______________(����ش�һ�㼴��)�� (5)SiCl4��������ӦҲ�ܵõ��裬����Ӧ�����¶Ȳ�ͬ���ڹ�ҵ����������������л����SiCl4���������������Ӧ������Ϊ��õķ��뷽����______________�� (6)��ҵ����������Ȼ����ԭ���ƹ裬��ԭ�����£�  �÷���������������ԭ���Ƚϣ���ȱ���������������ֱ���_________________�� �÷���������������ԭ���Ƚϣ���ȱ���������������ֱ���_________________�� |
|||||||||||||
�� |
��1����ȥ�ֹ���SiO2��Fe2O3��CuO�����ʡ��� ��2��a��b ��SiHCl3+H2 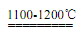 Si+3HCl������ Si+3HCl������ ��3������SiHCl3���Ա�ʹ֮�����������ʯӢ�ܡ�������Ӧ�¶Ƚϸߣ���ͨ�������ܳ��ܸø��¡����� ��4��û�н���β������������ ��5�������� ��6��ʹ�����ж����壻��������ԭ����HCl��H2����ֱ��ѭ�����ã���Լ�˳ɱ��������Ȼ����ԭ����û�п�ѭ�����õ�ԭ�ϡ����� |
|||||||||||||
| ��� | 7 |
|
||||||
���� |
�� | |||||||
| ��� | ���������[(NH4)2Fe(SO4)2]�Ƿ�����ѧ�е���Ҫ�Լ����ڲ�ͬ�¶��¼��ȷֽ���ﲻͬ�������ͼʵ��װ�ã��г�װ����ȥ������500��ʱ������������A�е�������������ֽ���ȫ��ȷ���ֽ����ijɷ֡�  ��1��Bװ�õ�������_________________________________________�� ��2��ʵ���У��۲쵽C������������D���а�ɫ�������ɣ���ȷ��������һ����_______���������д��D�з�����Ӧ�����ӷ���ʽ______________________����ȥ��C���ܷ�ó�ͬ������____________����ǡ�����ԭ����____________________________�� ��3��A�й�����ȫ�ֽ���Ϊ����ɫ��ĩ��ijͬѧ���ʵ����֤����������ΪFe2O3��������FeO���������ɱ������ݡ����Լ�����������Ʒ��ѡ��
��5���������ʵ��������������������500��ʱ��������������ȫ�ֽ�Ļ�ѧ����ʽ_______________�� |
|||||||
�� |
(1)����������Ƿ���ˮ���� (2)SO2�� SO2+H2O2+Ba2+===BaSO4��+2H+��������SO3Ҳ�а�ɫ�������ɡ� (3)���裺ȡ����A�в��������Թ��У���������ϡ���ᣬ�����ʹ����ȫ�ܽ⣻����Һ�ֳ����ݣ��ֱ�μӸ��������Һ��KSCN��Һ�������εμ�K3Fe(CN)6��Һ��KSCN��Һ�����������𰸣������������������Һ����ɫ������KSCN��Һ���죨����K3Fe(CN)6��Һ��������KSCN��Һ���죬�����������𰸣� (4)3x+y=z (5)2(NH4)2Fe(SO4)2Fe2O3+2 NH3��+N2��+4SO2��+5H2O |
|||||||
| ��� | 8 |
|
||||
���� |
�� | |||||
| ��� | �����ڼ��������¿ɻ�ԭ����ͭ����������ˮ�����⣬����̼�������ij��ѧС��������ͼװ��̽���䷴Ӧ��� 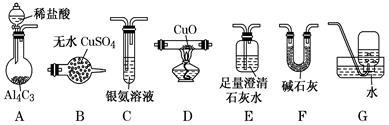 [��������]��CO����������Һ��Ӧ��CO��2[Ag(NH3)2]����2OH��==2Ag����2NH��CO��2NH3�� ��Cu2OΪ��ɫ������Ag+��Ӧ���ܷ�����Ӧ��Cu2O��2H��==Cu2+��Cu��H2O�� ��1��װ��A�з�Ӧ�Ļ�ѧ����ʽΪ___________________________________________�� ��2�������������װ�ô����ҵ�����˳��ΪA��__________________��(����ĸ���) ��3��ʵ���еμ�ϡ����IJ���Ϊ______________________________________________�� ��4����֪��������к���CO����װ��C�пɹ۲쵽��������________________��װ��F������Ϊ_________________________________________�� ��5������Ӧ������װ��D���Թ��й���ȫ����Ϊ��ɫ�� �����ʵ��֤����ɫ�����к���Cu2O��________________________________________�� ����֤����ɫ�������Ƿ���Cu����ͬѧ�������ʵ�飺��������ɫ�����м�������0.1mol��L−1AgNO3��Һ��������Һ�������ݴ��жϺ�ɫ�����к���Cu����ͬѧ��Ϊ�÷�������������֤����ͬѧ�Ľ��ۣ������������¶Ա�ʵ�飬��ɱ������ݡ�
|
|||||
�� |
��1��Al4C3��12HCl===3CH4����4AlCl3������ ��2��F��D��B��E��C��G���� ��3���ȴ�Һ©���ϿڵIJ�����(����ʹ��Һ©���ϿڵIJ������İ��۶�©���ϵ�С��)���ٽ���Һ©�������������ʹϡ���Ỻ�������Թ��� ��4���к�ɫ��������(���Թ�������������)������ȥ�����е�HCl�����ˮ������ ��5��ȡ������ɫ���壬��������ϡ���ᣬ����Һ��Ϊ��ɫ����֤����ɫ�����к���Cu2Oȡ����Cu2O�������Թ��У���������0.1mol��L−1AgNO3��Һ |
|||||
| ��� | 9 |
|
||
���� |
�� | |||
| ��� | ij��ѧ̽��ѧϰС����������ͼ��װ��(���̶ֹ�װ������ȥ)�ⶨij��ɫͭ������Ʒ�Ļ�ѧʽ���������²��������ʵ�顣 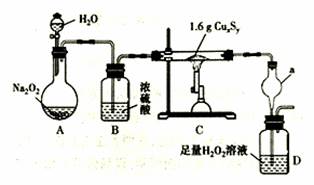 ����һ��������ͼ��ʾװ�ã���������1.6gCuxSy�������������ٱ仯���õ���ɫ�����һ����ʹƷ����Һ��ɫ�����塣 ���������D��������Һ���������̽��д��������D����Һ����ȴ������250mL��Һ��ȡ25.00mL��Һ������2-3�η�̪��Һ���ζ�������0.1mol��L−1 NaOH��Һ20.00mL�� ��ش��������⣺ ��1��Aװ���з�����Ӧ�Ļ�ѧ����ʽΪ_______________________��ֹͣ���Ⱥ������ͨ��һ��ʱ���O2����Ŀ����________________________�� ��2������a������Ϊ________________��װ��D�з�Ӧ�Ļ�ѧ����ʽΪ_________________________�� ��3���������������Һʱ����IJ������������������ձ��⣬����_____���жϵζ��յ��������_________�� ��4�����������ṩ�����ݿɼ���ó���ͭ����Ļ�ѧʽΪ_______________�� ��5����ͬѧ��Ϊ�ɽ�װ��D��Ϊװ��������ʯ�ҵĸ���ܣ�ͨ���ⶨ��Ӧǰ�����ܵ�������������Ԫ�صĺ���������Ϊ�˷���(���������������)��ԭ����____________________________�� |
|||
�� |
��1��2Na2O2+2H2O===4NaOH+O2����ʹ���ɵ�SO2ȫ����H2O2��Һ���ա��� ��2����ֹ������SO2+H2O2===H2SO4������ ��3��250mL����ƿ����ͷ�ιܡ����������һ��NaOH��Һʱ����Һ��Ϊdz��ɫ��30���ڲ���ɫ������ ��4��Cu2S������ ��5��������������SO2���������ҿ����е�CO2��ˮ��������ʹ��������� |
|||
| v����ʡʵ����ѧ�����ҡ���ʵ����������� v������ |